DNA依赖性蛋白激酶催化亚单位(DNA-PKcs)在非同源末端连接中起着核心作用,这是人类检测和修复DNA双链断裂(DSB)的两个主要途径之一。DNA-PKcs在修复病理性DSB方面非常重要,这使得DNA-PKcs抑制剂与DSB诱导放疗和化疗相结合,成为有吸引力的癌症治疗药物。许多已经开发的DNA-PKcs选择性抑制剂显示出治疗各种癌症的潜力。有鉴于此,英国剑桥大学的Tom L. Blundell、Shikang Liang等研究人员,揭示抑制剂对DNA修复蛋白DNA-PKcs调节的结构基础。
本文要点
1)研究人员报道了从HeLa细胞核提取物中天然纯化的人类DNA-PKcs与腺苷-5′-(γ-硫)-三磷酸(ATPγS)和四种抑制剂(wortmannin、NU7441、AZD7648和M3814)的冷冻电镜结构,包括正在进行临床试验的候选药物。
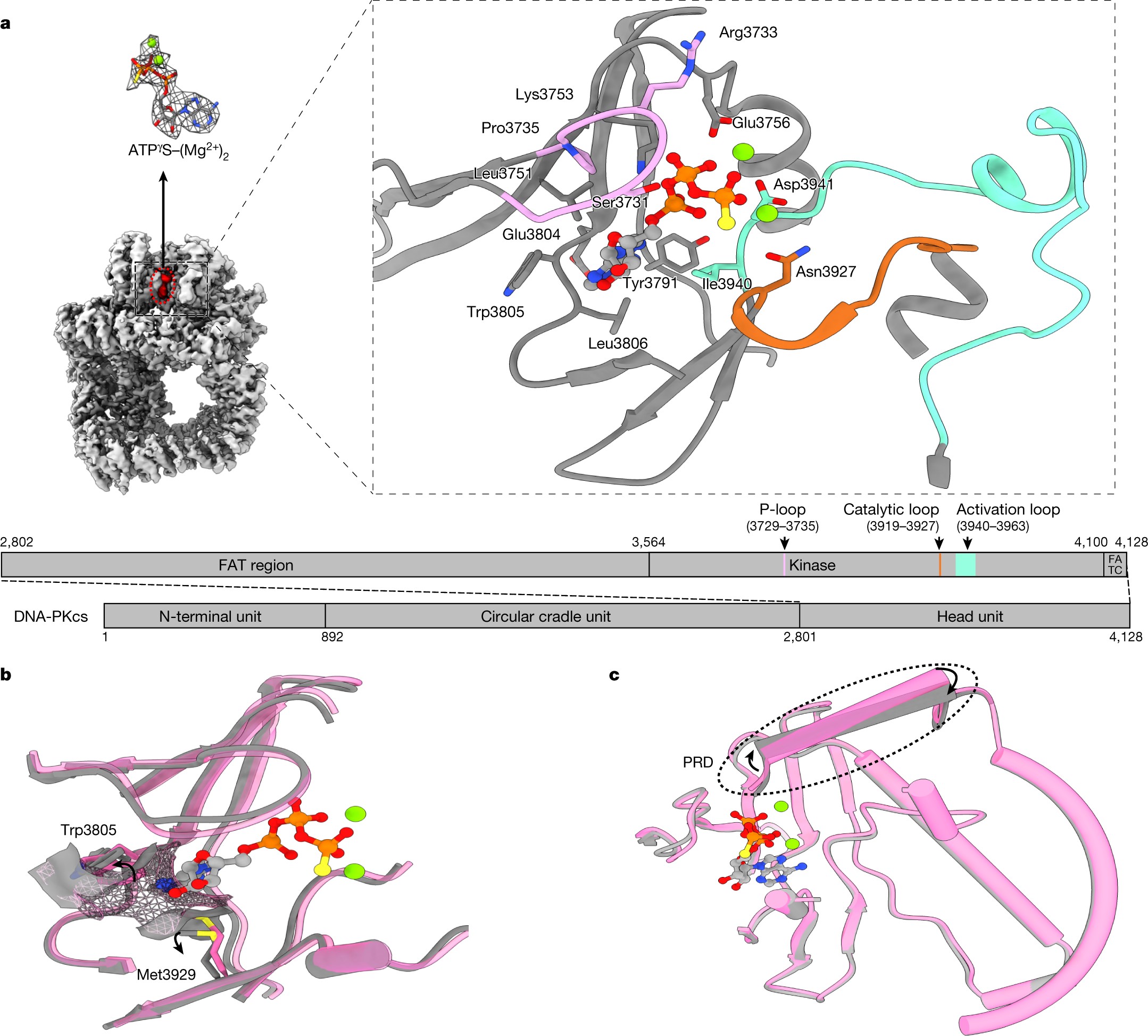
2)这些结构揭示了ATP在催化前与活性部位结合的分子细节,并提供了对竞争性抑制剂的作用方式和特异性的深入了解。
3)值得注意的是,配体的结合导致PIKK调节域(PRD)的移动,从而揭示了p环和PRD构象之间的联系。
4)对DNA依赖性蛋白激酶全酶的电泳迁移率测定和冷冻电镜研究进一步表明,配体的结合对全酶复合物的组装没有负向的异构作用或抑制作用,抑制剂通过与ATP的直接竞争发挥作用。
本文研究描述的结构有望极大地帮助未来针对DNA-PKcs的合理药物设计工作,并表明冷冻电镜在结构指导药物开发中对大型和挑战性的目标具有潜力。
参考文献:
Shikang Liang, et al. Structural insights into inhibitor regulation of the DNA repair protein DNA-PKcs. Nature, 2021.
DOI:10.1038/s41586-021-04274-9
https://www.nature.com/articles/s41586-021-04274-9


















