补体调理素作用是纳米医学所面临的最大挑战之一。注射入血液后,纳米颗粒会立即被补体蛋白C3调理,进而导致其被吞噬细胞清除,影响靶向功能和释放过敏毒素。虽然一些表面聚合物,如聚乙二醇(PEG)等能够降低补体调理素作用,但目前大多数类型的纳米颗粒都仍会受到补体调理素作用的影响,特别是当其连接有靶向部分时。为了改善补体的不利作用,宾夕法尼亚大学Jacob S. Brenner和Jacob W. Myerson将哺乳动物补体激活的两个天然调节因子(RCAs),即因子H和因子I共轭到纳米颗粒的表面。
本文要点:
(1)在体外,实验将因子H或I偶联到聚乙二醇包被的纳米颗粒上后发现,该策略能够降低C3调理作用,并显著减少吞噬细胞对纳米颗粒的摄取。在脓毒症诱导的小鼠肺损伤模型中,因子I的偶联能够消除肺内血管内吞噬细胞对纳米颗粒的吸收,从而使纳米颗粒的血药浓度持续升高更长的时间。
(2)对于通过偶联抗ICAM抗体以靶向到肺内皮的纳米颗粒而言,因子I偶联会使其分布的细胞类型从吞噬细胞转向为内皮细胞。与此同时,因子I偶联也能够消除多种纳米颗粒所引发的严重类过敏反应,防止系统性毛细血管渗漏,并维持向内脏器官和大脑的血液流动。综上所述,这一研究表明将RCAs偶联到纳米颗粒上能够帮助纳米药物克服补体造成的不利影响,进而有效改善其在临床中的应用前景。
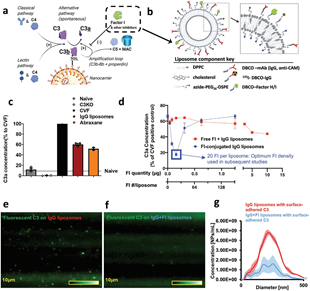
Zhicheng Wang. et al. Combating Complement’s Deleterious Effects on Nanomedicine by Conjugating Complement Regulatory Proteins to Nanoparticles. Advanced Materials. 2022
DOI: 10.1002/adma.202107070
https://onlinelibrary.wiley.com/doi/10.1002/adma.202107070



















