过度激活的T细胞和过度产生的促炎细胞因子会形成一个自我放大的信号循环,进而不断加剧失调的炎症反应,并推动自身免疫性疾病(如艾滋病)的发展。苏州大学殷黎晨教授开发了一种基于表达PD-L1的巨噬细胞膜(PRM)包裹的聚乳酸-羟基乙酸共聚物纳米粒子(PLGA NPs)的免疫工程化纳米诱饵(NDs),并将其用于介导实现艾滋病炎症级联反应的多靶点阻断。
本文要点:
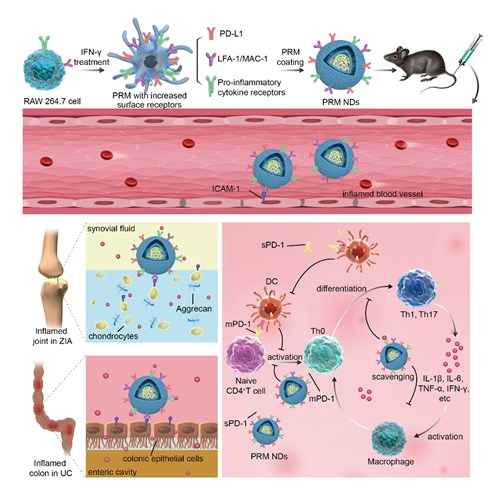
(1)研究发现,从IFN-γ处理的RAW 264.7细胞中提取的PRM表面粘附分子受体和促炎细胞因子受体的水平会有升高,因此系统给药PRM NDs后,其在炎症组织中具有更高的积累水平,并且对多种促炎细胞因子的清除能力也更强。
(2)更重要的是,IFN-γ会诱导PRM上PD-L1的显著表达,使PRM NDs能够结合CD4+ T细胞表面的mPD-1或中和游离的sPD-1,进而重构PD-1/PD-L1抑制轴,抑制CD4+ T细胞活化,恢复免疫耐受。研究表明,PRM NDs可在酵母聚糖A诱导的关节炎小鼠模型和硫酸右旋糖酐钠诱导的溃疡性结肠炎小鼠中实现有效的抗炎和免疫抑制作用,进而减轻自身免疫损伤。综上所述,该研究可为实现细胞膜基NDs的免疫工程提供新的参考,并为通过多靶点免疫调节以治疗艾滋病提供重要的借鉴。
Mengying Hou. et al. Immuno-Engineered Nanodecoys for the Multi Target Anti-Inflammatory Treatment of Autoimmune Diseases. Advanced Materials. 2022
DOI: 10.1002/adma.202108817
https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.202108817



















