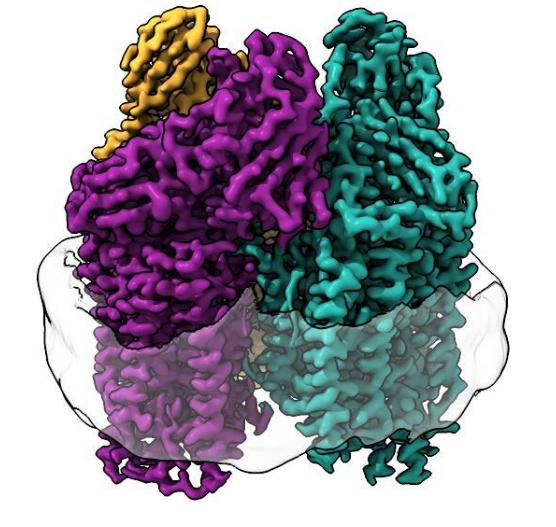
微粒甲烷单加氧酶(pMMO)是好氧甲烷菌进行甲烷有氧代谢的关键酶,目前无论是生物化学转化角度还是生物技术应用角度,人们都对理解这个反应的机理非常感兴趣,但是通常纯化这种结合在膜上的金属酶的过程中导致其失活。
有鉴于此,西北大学Amy C. Rosenzweig等报道通过将pMMO重新在脂质纳米盘中重构,发现双层脂质环境重构导致酶催化活性重新恢复。
具体通过分辨率达到2.14-2.46 Å的冷冻电镜表征晶体结构表征,发现在脂质中重构的pMMO除了发现稳定作用的脂质、PmoA、PmoC结构单元中以往未曾发现的结构,还发现在PmoC结构与相邻疏水空腔之间存在Cu结合位点(这个位点以往研究中未曾发现)。
参考文献
Christopher W. Koo, Frank J. Tucci, Yuan He, Amy C. Rosenzweig*, Recovery of particulate methane monooxygenase structure and activity in a lipid bilayer, Science 2022, 375 (6586), 1287-1291
DOI: 10.1126/science.abm3282