在细胞内构建人工动态结构以对细胞器进行干扰是一种调节细胞行为和命运的有效策略,并可为治疗提供新的方法。天津大学仰大勇教授开发了一种由细胞内K+介导、可在细胞内动态组装的DNA四面体,并将其用于实现有效的线粒体干扰和调控活细胞的能量代谢。
本文要点:
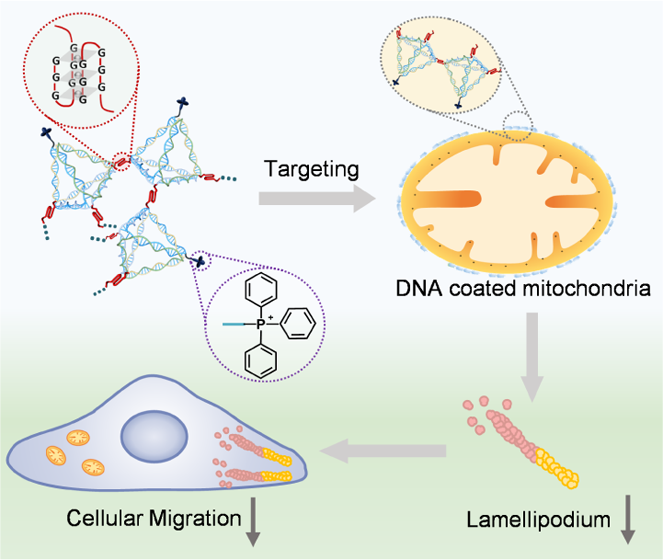
(1)实验利用三苯基膦(TPP)对该DNA四面体中的一个顶点进行修饰以用于线粒体靶向,并利用富含鸟嘌呤的序列对其他三个顶点进行栓系,以实现K+介导的分子间G-四联体的形成以及随后DNA四面体的组装,进而在细胞质中形成聚集体。该DNA聚集体能够特异性靶向线粒体,并作为物质沟通的聚阴离子屏障以对线粒体的有氧呼吸功能和相关的糖酵解过程产生显著抑制作用,从而减少细胞内三磷酸腺苷(ATP)的生成。
(2)ATP的缺乏会阻碍片状伪足(细胞运动所必需的)的形成,因此可以对细胞的迁移产生明显的抑制作用。实验结果表明,癌细胞的迁移能力会被抑制50%。综上所述,该工作为通过内源性分子介导的外源性人工结构在活细胞内的动态组装来调控细胞器提供了一种新的策略,其在精准生物医学领域中具有广阔的应用前景。
Feng Li. et al. Dynamic Assembly of DNA Nanostructures in Living Cells for Mitochondrial Interference. Journal of the American Chemical Society. 2022
DOI: 10.1021/jacs.2c00823
https://pubs.acs.org/doi/10.1021/jacs.2c00823



















