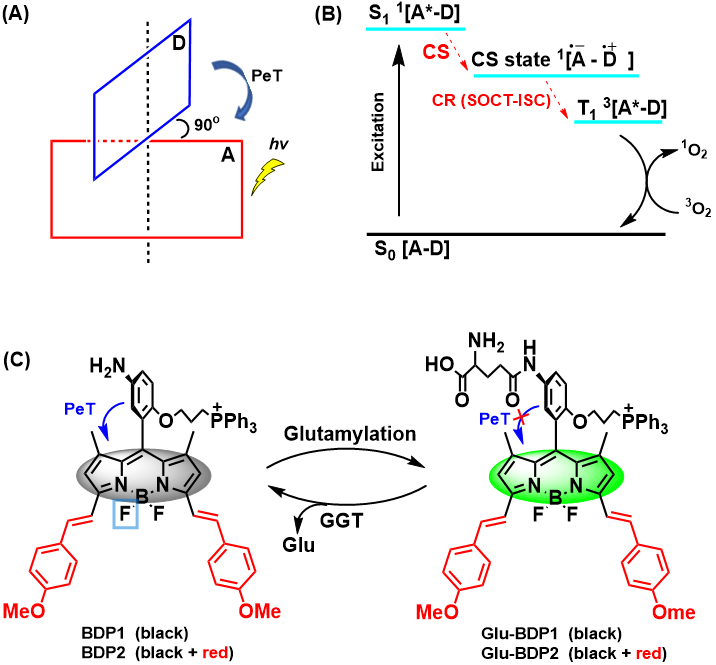
基于自旋轨道电荷转移体系间交叉机理,山西大学郭炜教授和霍莹莹副教授构建了两种吸收最大值为506 nm/660 nm的无重原子光敏剂BDP1/BDP2,并将其用于光动力治疗(PDT)。
本文要点:
(1)具有长三重态寿命、高单线态氧量子产率和线粒体靶向等特性的光敏剂对癌细胞具有很高的光毒性。此外,PDT促进的细胞凋亡可以通过两种PSs伴随线粒体自噬激活而产生的荧光关闭响应来监测,从而实现及时的治疗反馈,避免治疗过少或过度。
(2)此外,这种设计策略也使得研究者可以通过将γ-谷氨酰转肽酶的底物(γ-谷氨酰基)与BDP1/BDP2的烷氧基苯胺单元相连接而构建得到可激活的光敏剂GluBDP1/Glu-BDP2。实验结果表明,它们能够在择性地杀死癌细胞而非正常细胞,进而在不损害健康组织的情况下有效地消融肿瘤。
Junfeng Miao. et al. Heavy Atom-Free, Mitochondria-Targeted, and Activatable Photosensitizers for Photodynamic Therapy with Real-Time InSitu Therapeutic Monitoring. Angewandte Chemie International Edition. 2022
DOI: 10.1002/anie.202201815
https://onlinelibrary.wiley.com/doi/10.1002/anie.202201815



















