通过生物分子纳米结构进行靶向免疫调节,特别是对树突细胞(DC)的靶向免疫调节为实现有效的癌症治疗带来了新的希望。然而,如何通过模拟天然配体来激活免疫细胞信号转导和构建高性能的激动剂仍然是亟需解决的严峻挑战。国家纳米科学中心王浩研究员和安红维副研究员构建了一种基于多肽的纳米CD40激动剂(PVA-CD40),其具有预先设计的界面拓扑结构,能够有效和持久地激活淋巴结DCs,进而实现增强的免疫治疗效果。
本文要点:
(1)实验通过将“CD40锚定臂”和“组装驱动马达”两个功能肽进行点击共轭而实现了PVA-CD40的现场制备。由此产生的多价界面会迅速触发受体寡聚和下游信号。研究表明,与CD40抗体相比,一针注射PVA-CD40所诱导的DC成熟期可达到2.3倍。
(2)将PVA-CD40与抗PD-1抗体联合治疗后,B16F10和4T1小鼠肿瘤模型的肿瘤生长均会受到抑制,存活率高达37%,而临床相关的CD40单抗和抗PD-1联合治疗组的小鼠则均无存活。综上所述,在体内构建类抗体超结构能够为调节免疫反应持续时间以达到最佳治疗效果提供一个有效的策略。
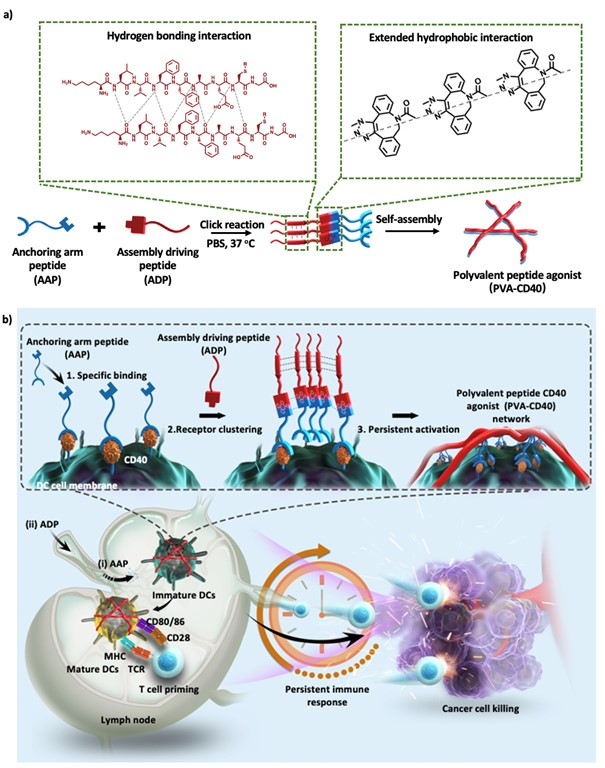
Muhetaerjiang Mamuti. et al. Polyvalent peptide CD40 nano-agonist for targeted modulation of dendritic cells and amplified cancer immunotherapy. Advanced Materials. 2022
DOI: 10.1002/adma.202109432
https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.202109432



















