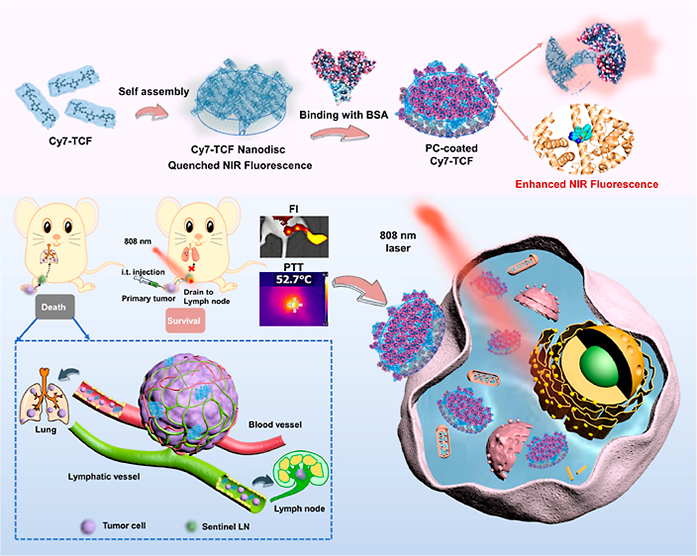
近红外(NIR)光热转换(PTAs)试剂具有较大的刚性π扩展平面结构,其在生理环境中会因强的分子间偶极或π-π相互作用而导致其发射被猝灭。这种聚集引起的猝灭效应也会极大地阻碍了其在成像指导的光热治疗中的应用。有鉴于此,青岛科技大学李志波教授和周现锋教授设计一种生物蛋白冠(PC),一旦其在PTA纳米聚集体上以优选方向稳定,就可以产生具有高量子产率(6.2%)的近红外荧光,且不会影响其光热性能。
本文要点:
(1)实验结果和计算模型均表明,其荧光增强机制是由于纳米PTA与白蛋白发生高亲和力结合,进而调控PTA的分子构象和聚集状态所导致的。
(2)白蛋白PC包覆的PTA聚集物可通过高时空分辨率成像以在成像指导下对哨位淋巴结中的肿瘤细胞进行光热治疗,进而显著抑制肺转移。研究表明,这种治疗方法能够与手术切除原发肿瘤相结合以有效延长动物生存期,因此有望在晚期转移性癌症的治疗中实现临床应用。
Xueluer Mu. et al. Lighting up Self-Quenching Nanoaggregates with Protein Corona for Simultaneous Intraoperative Imaging and Photothermal Theranostics of Metastatic Cancer. Analytical Chemistry. 2022
DOI: 10.1021/acs.analchem.2c01462
https://pubs.acs.org/doi/10.1021/acs.analchem.2c01462



















