基于核酸的结构因其灵敏和选择性检测疾病生物标志物的能力而彻底改变了临床诊断。能够识别核酸和非核酸靶标的设计序列生成的进展推动了它们作为化学和生物探针的发展。核酸检测中一般会涉及到靶标扩增来放大信号,然而,靶标扩增仅适用于核酸,限制了分析物范围。基于此,美国西北大学Chad A. Mirkin等人介绍了一种在基于 CRISPR-Cas 的检测中生成放大信号的新方法。
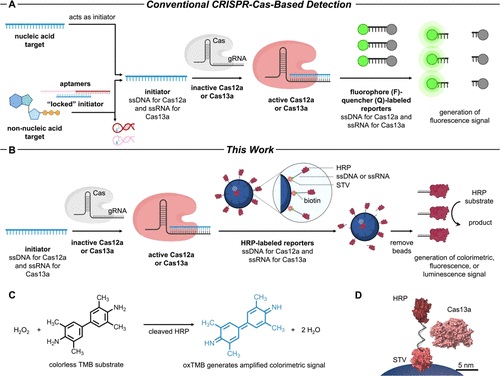
本文要点:
(1)目标识别激活 CRISPR-Cas 复合物,导致辣根过氧化物酶 (HRP) 标记的寡核苷酸从微珠表面催化裂解。释放到溶液中的 HRP 可以通过比色、荧光或发光方法进行监测,产生高达 75 倍的开启信号和低至 10 fM 的检测限 (LOD)。与使用传统荧光团/猝灭剂报告基因的基于 Cas 的检测相比,该策略将 LOD 提高了 30 倍。
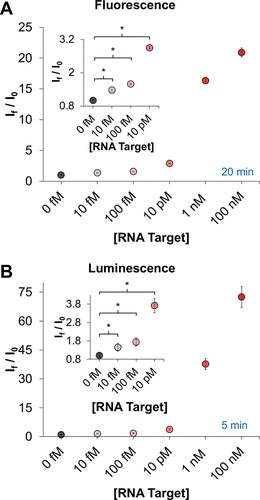
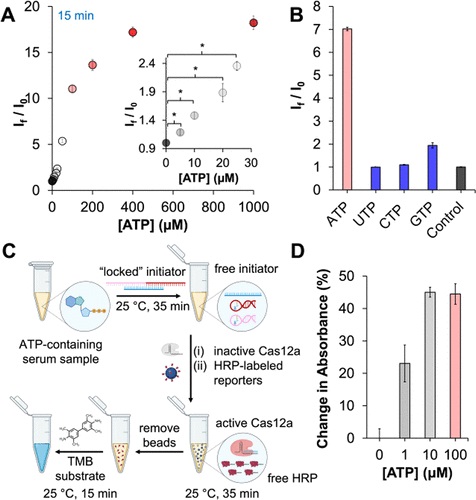
(2)作为概念验证,在临床相关浓度、无 PCR 及室温(25°C)条件下,作者用肉眼快速(<1 小时)检测 SARS-CoV-2 病毒的核酸标记物。结果表明可以对探针组进行编程,使其在存在非核酸靶标的情况下被识别和激活。具体来说,与适配体结合的三磷酸腺苷 (ATP) 可以激活 CRISPR-Cas 并触发比色读数,从而能够以与几种市售试剂盒相当的灵敏度分析人血清样品中的 ATP。总之,该策略提供了一个简单而灵敏的平台来检测目标扩增不方便或不可能的分析物。
参考文献:
Devleena Samanta, Sasha B. Ebrahimi, Namrata Ramani, and Chad A. Mirkin. Enhancing CRISPR-Cas-Mediated Detection of Nucleic Acid and Non-nucleic Acid Targets Using Enzyme-Labeled Reporters. J. Am. Chem. Soc. 2022
DOI:10.1021/jacs.2c07625
https://doi.org/10.1021/jacs.2c07625



















