乏氧是实体瘤的显著特征之一。乏氧激活的前药(HAPs)能够有选择性地杀死乏氧细胞,进而可将乏氧从缺点转化为实现精确治疗的优势。胶质瘤作为最常见且最不可治愈的神经系统肿瘤,其乏氧微环境更为显著,有望用于HAPs治疗。然而,乏氧不足和血脑屏障(BBB)的阻碍也会严重限制HAPs的激活效果和生物利用度。有鉴于此。大连理工大学彭孝军院士设计合成了一种新型纳米颗粒iRGD@ZnPc+TPZ,其表面包覆有作为HAP的替拉扎明(TPZ)和作为光敏剂的酞菁锌(ZnPc),能够达到精准抑制胶质瘤的目的。
本文要点:
(1)研究发现,iRGD@ZnPc+TPZ能在胶质瘤模型中突破血脑屏障,实现深度穿透和有效保留,这也与iRGD介导的受体靶向和主动转运有关。
(2)ZnPc被肿瘤细胞内化后,其在辐射下能有效地消耗瘤内O2以产生活性氧,不仅能够起到抑瘤作用,还能强化乏氧以激活TPZ,放大其化疗效果。实验结果表明,光敏剂增强的乏氧能够激活HAPs以抑制胶质瘤的生长。综上所述,该研究提供了一种增敏激活HAPs的新策略,有望用于胶质瘤的临床治疗。
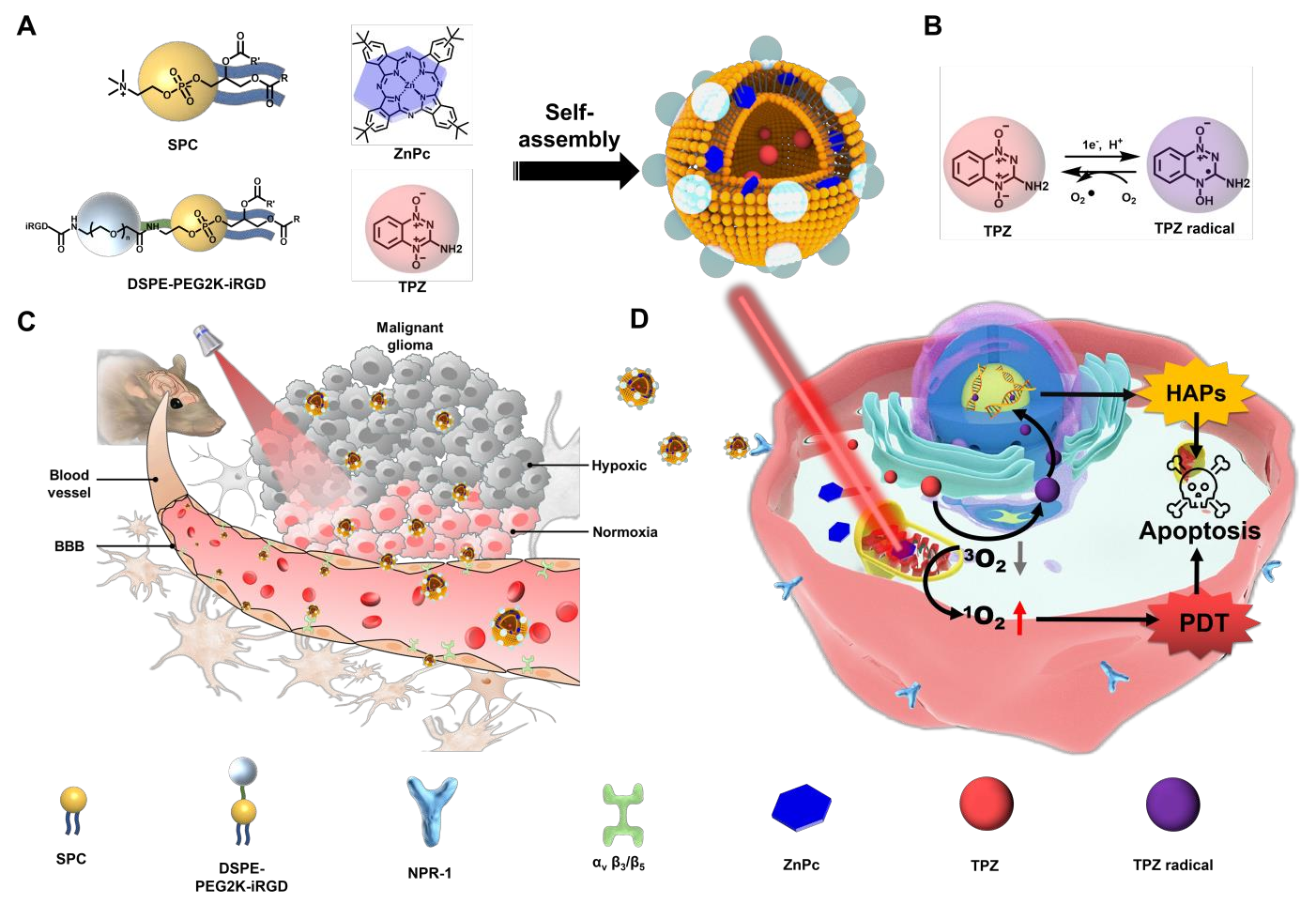
Han Zhang. et al. Precise gliomas therapy: Hypoxia-activated prodrugs sensitized by nanophotosensitizers. Biomaterials. 2022
https://www.sciencedirect.com/science/article/abs/pii/S0142961222004100



















