肿瘤干细胞(CSCs)是肿瘤细胞的亚群,其具有致瘤性、多种分化潜能以及可自我更新等特性,是肿瘤复发和转移的动力来源。然而,由于CSCs生长迅速,且突变率快,因此如何靶向CSCs仍然是癌症治疗所面临的一项主要难题。北京科技大学姜建壮教授、王天宇教授、中科院生物物理研究所秦燕研究员和丁芳助理研究员开发了一种靶向CSCs的光动力治疗(PDT)策略,其依赖于CSCs中更为丰富的核糖体。
本文要点:
(1)在癌细胞中,带正电的纳米颗粒与带负电的核酸结构之间的相互作用能够实现纳米颗粒的核糖体靶向和CSCs靶向。研究表明,氨基卟啉(m-TAPP)与短肽(Fomc-L3-OMe)共组装后可形成具有良好生物相容性和光活性的纳米粒子(NPs),其在低pH值的肿瘤微环境中带正电荷,可有效地进入癌细胞核糖体,接近癌细胞的细胞核,从而富集在快速扩增的CSCs中。
(2)实验通过证明肿瘤细胞和组织中CSCs标志物CD44、CD133和核糖体数量发生显著降低而充分验证了m-TAPP组合物对CSCs的抑制作用。在光照射下,NPs能够诱导ROS产生,引起癌细胞核糖体的发生破坏性损伤以及诱导细胞凋亡,从而阻止肿瘤生长。综上所述,该研究利用基于小有机分子的组合不仅实现了核糖体降解诱导的癌细胞凋亡,也为实现靶向CSCs的PDT提供了新的借鉴。
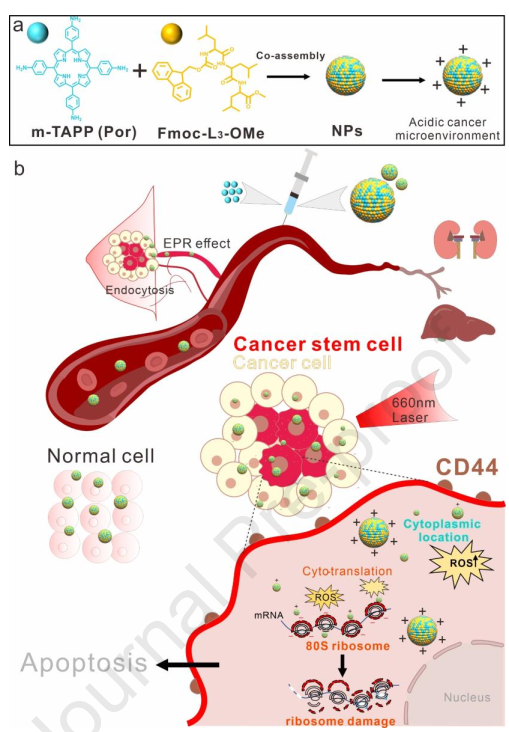
Jian Wang. et al. Amino porphyrin-peptide assemblies induce ribosome damage and cancer stem cell inhibition for an enhanced photodynamic therapy. Biomaterials. 2022
https://www.sciencedirect.com/science/article/pii/S0142961222004525



















