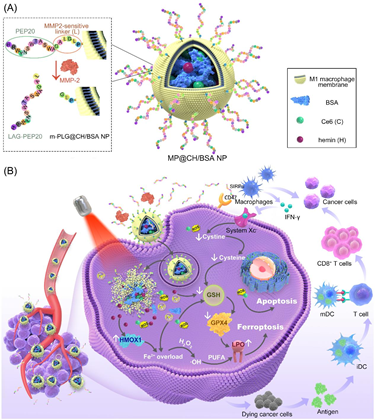
光动力疗法(PDT)可通过产生细胞毒性活性氧诱导癌细胞发生凋亡,但其治疗效果也会受到癌细胞内固有/诱导性抗凋亡机制和肿瘤乏氧微环境(TME)的阻碍。此外,PDT所诱导的抗肿瘤免疫激活效果也并不令人满意。为了解决这些障碍,山东大学翟光喜教授和杨小叶研究员构建了一种新型的仿生纳米平台,以用于精确递送光敏剂Ce6、hemin和PEP20 (CD47抑制肽),从而实现氧气增强的PDT、铁死亡激活和CD47-SIRP α封锁。
本文要点:
(1)Hemin的类过氧化氢酶活性可缓解TME乏氧,改善PDT。研究表明,该纳米平台可通过经典模式(谷胱甘肽过氧化物酶4通路失调)和非经典模式(诱导Fe2+过载)激活铁死亡。此外,除了hemin具有消耗谷胱甘肽和上调血红素氧合酶表达的作用外,研究者也发现Ce6可通过经典和非经典模式增强铁死亡激活。
(2)通过结合PEP20介导的CD47-SIRPα阻断和PDT介导的T细胞活化,该纳米平台能够显著增强抗癌免疫,有效抑制原发肿瘤的生长和转移。这也是首次有研究发现PEP20具有增强铁死亡的作用。综上所述,该研究充分揭示了PDT- -铁死亡激活的相互作用机制,并将免疫治疗与铁死亡激活连接起来,为开发癌症治疗的新型组合模式奠定了理论基础。
Zhijing He. et al. Oxygen-boosted biomimetic nanoplatform for synergetic phototherapy/ferroptosis activation and reversal of immune-suppressed tumor microenvironment. Biomaterials. 2022
https://www.sciencedirect.com/science/article/abs/pii/S0142961222004720



















