光动力治疗(PDT)已发展成为一种对抗耐多药(MDR)癌症的有效策略。然而,活性氧(ROS)的短半衰期和有限的扩散都会严重影响PDT的治疗效果。为了解决这一问题,柏林自由大学Rainer Haag和中国药科大学钟伊南研究员开发了一种肿瘤靶向纳米平台,它可以精确地将靶向线粒体和内质网(ER)的 PDT制剂递送到所需位点,以实现双细胞器靶向型PDT。
本文要点:
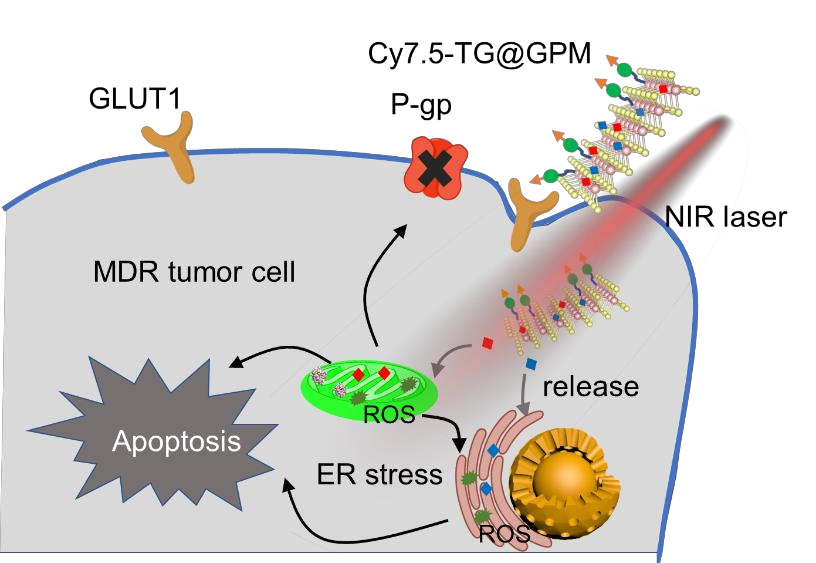
(1)实验利用葡萄糖修饰的超支化聚甘油(hPG)对二硫化钼(MoS2)纳米片进行功能化,然后负载靶向细胞器的PDT制剂,从而构建了该纳米平台。研究,该纳米平台(Cy7.5-TG@GPM)可以介导实现MDR细胞内化的增强内化和PDT制剂的精准亚细胞定位,进而在近红外(NIR)光照射下原位触发ROS生成,以增强PDT和逆转MDR,以在HeLa耐多药肿瘤小鼠模型中实现显著的肿瘤抑制。
(2)研究者通过对线粒体和ER靶向PDT的协同作用机制进行研究后发现,ROS诱导的内质网应激不仅能够激活CHOP促凋亡信号通路,还可与ROS诱导的线粒体功能障碍进行合作,以触发线粒体释放细胞色素C,诱导细胞死亡。此外,线粒体功能障碍也会减少ATP的产生,从而有助于逆转MDR。综上所述,这种具有NIR响应特性以及靶向肿瘤和亚细胞细胞器能力的纳米平台能够为实现有效的MDR癌症治疗提供一种新的策略。
Shaohui Xu. et al. Dual Tumor- and Subcellular-targeted Photodynamic Therapy Using Glucose Functionalized MoS2 Nanoflakes for Multidrug-Resistant Tumor Ablation. Biomaterials. 2022
https://www.sciencedirect.com/science/article/pii/S0142961222004847



















