线粒体功能障碍和氧化损伤是心肌缺血-再灌注损伤(MI/RI)的重要病理机制。因此,开发抗氧化药物来缓解MI/RI也具有重要的临床意义。有鉴于此,苏州大学程亮教授、安徽农业大学孙冬冬教授和山东第一医科大学Cundong Fan设计了具有近红外(NIR)-II光声成像性能的金-硒核壳纳米结构(AS-I/S NCs),并将其用于治疗MI/RI。
本文要点:
(1)缺血心肌靶向肽(IMTP)和线粒体靶向抗氧化肽SS31修饰的AS-I/S NCs能够靶向心肌细胞,进而通过抑制线粒体膜电位(MMP)消耗和恢复ATP合酶活性以显著抑制氧气-葡萄糖缺乏-恢复(OGD/R)诱导的H9c2细胞心脏毒性。此外,SS31修饰的AS-I/S NCs也能够实现对活性氧(ROS)的线粒体靶向抑制,随后通过抑制凋亡和氧化损伤以调节MAPKs和PI3K/AKT通路,减轻经OGD/R处理的H9c2细胞的氧化损伤。
(2)实验结果表明,体内给药AS-I/S NCs后可显著改善MI/RI大鼠的心肌功能和血管生成,进而通过抑制心肌凋亡和氧化损伤减轻心肌纤维化。此外,AS-I/S NCs在体内也具有良好的安全性和生物相容性。综上所述,该研究构建的线粒体靶向型硒-金纳米复合材料能够通过抑制ROS介导的氧化损伤和调节MAPKs和PI3K/AKT通路来治疗MI/RI,有望发展成为一种潜在的MI/RI治疗策略。
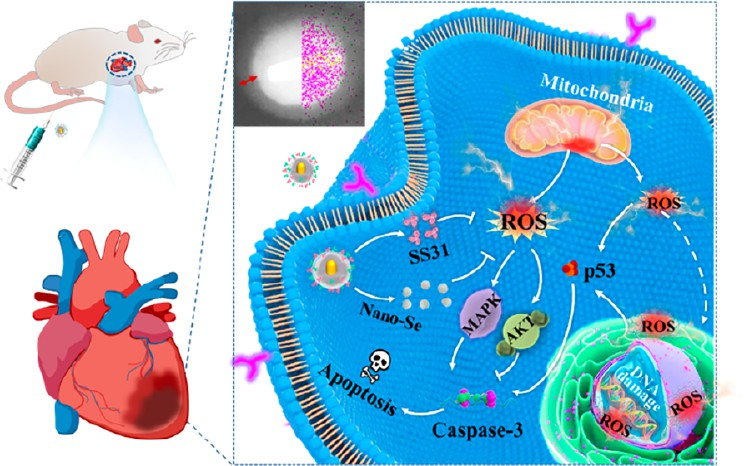
Yu Sun. et al. Light-Activated Gold−Selenium Core−Shell Nanocomposites with NIR-II Photoacoustic Imaging Performances for Heart-Targeted Repair. ACS Nano. 2022
DOI: 10.1021/acsnano.2c07311
https://pubs.acs.org/doi/10.1021/acsnano.2c07311



















