目前基于适配体的治疗作用机制主要依赖于占用驱动药理学来调节蛋白质的功能。湖南大学谭蔚泓院士团队报道了一种通过适体利用细胞蛋白酶体降解系统降解蛋白质以用于癌症治疗的新机制。
本文要点:
(1)实验室揭示了一种DNA核酸适体(以下简称c-Met-Ap)与间充质-上皮转换因子(c-Met)的胞外结构域结合后,选择性诱导c-Met在Y1003和Y1349位点上发生磷酸化。Y1003的磷酸化能够募集E3泛素连接酶(casitas B-lineage lymphoma),进而导致c-Met在蛋白酶体中发生泛素化和降解。
(2)在A549荷瘤BALB/c小鼠中,c-Met-Ap可诱导c-Met的异二聚伙伴蛋白和c-Met信号轴下游效应蛋白的降低,进而有效抑制肿瘤生长。综上所述,该研究揭示了一种新型、可操作的适配体治疗机制,能够为开发高效的抗癌药物开辟一条新的途径。
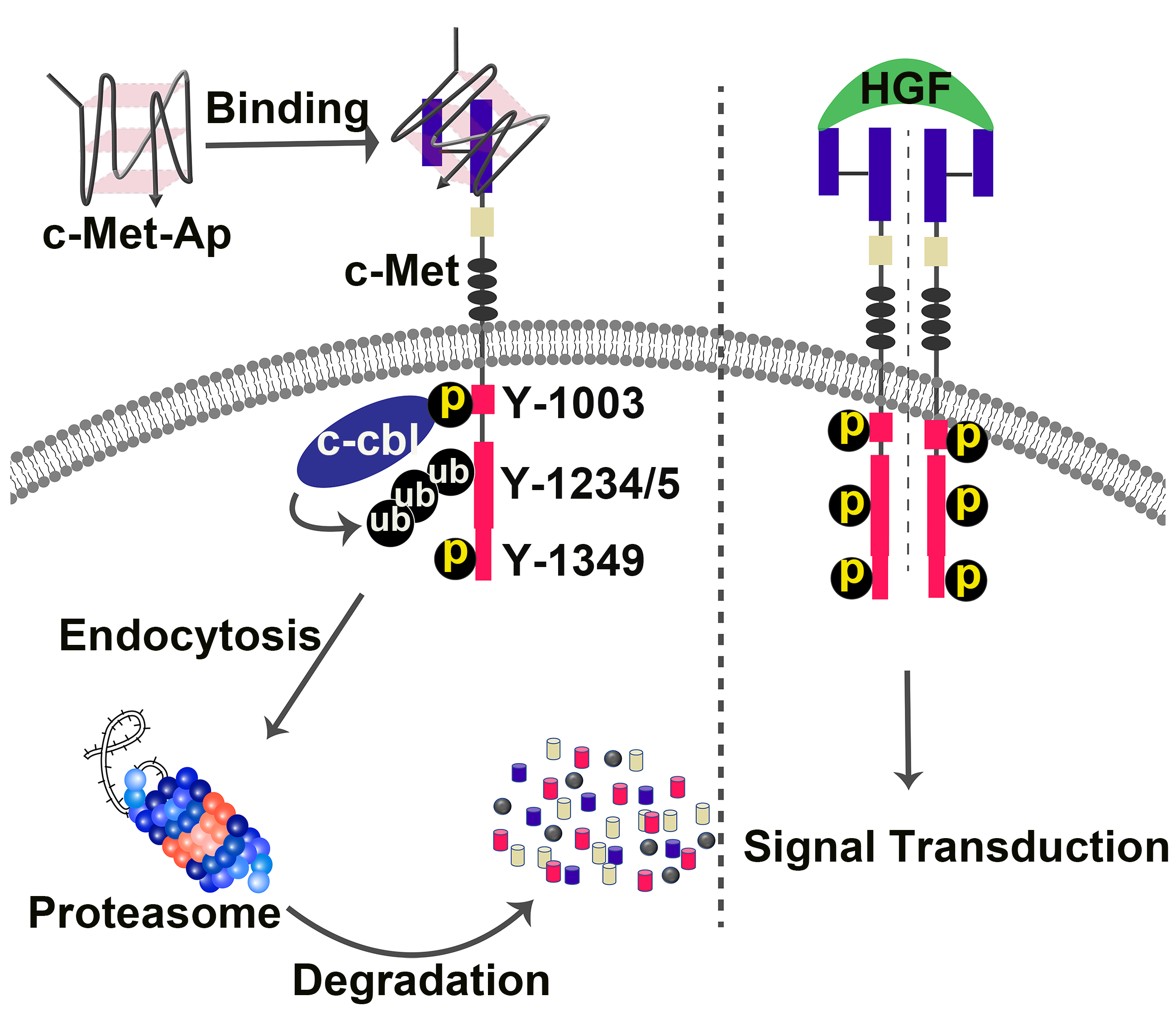
Kun Chen. et al. Aptamer Inhibits Tumor Growth by Leveraging Cellular Proteasomal Degradation System to Degrade c-Met in Mice. Angewandte Chemie International Edition. 2022
DOI: 10.1002/anie.202208451
https://onlinelibrary.wiley.com/doi/10.1002/anie.202208451



















