通过静脉给药的方式向肿瘤递送药物所面临的主要障碍是生物污染、调理作用以及巨噬细胞和网状内皮吞噬细胞对于药物的快速清除作用。用隐身包裹层对纳米颗粒进行掩盖能够部分克服这些障碍,但它也影响纳米材料与肿瘤细胞的相互作用。有鉴于此,得克萨斯大学休斯顿健康科学中心Sunil Krishnan构建了一种智能金纳米颗粒(GNRs),它能自发地从血流中的惰性材料转化为肿瘤内的活性纳米颗粒,进而穿透细胞,并有效地实现放疗增敏。
本文要点:
(1)实验利用可切割肽的聚乙二醇包裹层对带正电荷、能够穿透细胞的GNRs进行包裹,以屏蔽细胞对GNRs的吞噬作用。在没有外部触发器的情况下,该包裹层会被结直肠癌的肿瘤微环境中的蛋白酶(组织蛋白酶B)剪切掉,从而暴露产生未聚乙二醇化的GNR,进而被癌细胞有效内化,并转化为固定的GNR小簇。
(2)实验通过血液学、生化和组织病理学分析证明了在肿瘤中选择性暴露GNRs的策略能够降低脱靶毒性,在辐照后可显著延缓肿瘤生长,提高荷瘤小鼠存活率。综上所述,该研究有效解决了实现纳米颗粒有效递送和细胞内化所面临的多重障碍,能够为合理设计GNRs以实现临床放疗增敏应用提供重要的借鉴和参考。
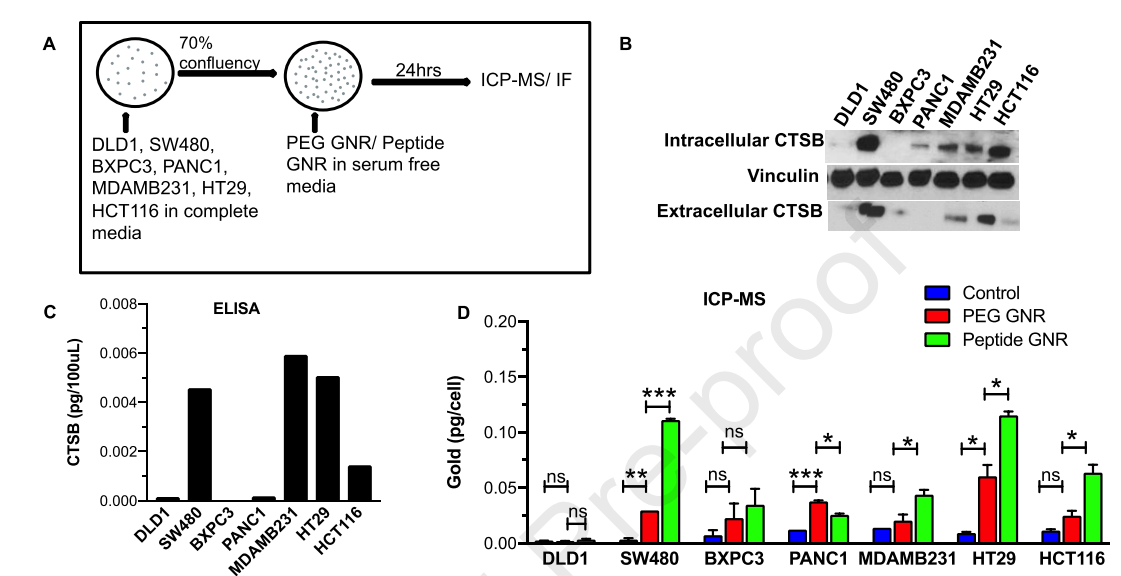
Subhiksha Raghuram. e al. Uncloaking cell-impermeant gold nanorods via tumor microenvironmental cathepsin B facilitates cancer cell penetration and potent radiosensitization. Biomaterials. 2022
https://www.sciencedirect.com/science/article/pii/S0142961222005270



















