癌症治疗目前仍面临着治疗效果、准确性和复杂性等方面的重大挑战。作为一种非侵入性的治疗手段,光动力疗法(PDT)因其良好的治疗效果、灵活性和低毒性而受到广泛欢迎。然而,在癌症治疗过程中,PDT也存在效率低、肿瘤特异性差和治疗深度有限等缺点。虽然研究者付出了很大的努力来提高性能,但PDT的整体效率和生物安全性仍不明确,使其无法满足迫切的临床需求。有鉴于此,中山大学梅林教授、邓文斌教授、香港城市大学孙红燕教授和广东工业大学张华堂副教授综合了以往PDT策略的优点,开发了一种靶向癌症、可激活、具有高生物安全性的光敏剂。由于该光敏剂具有良好的自组装能力,因此研究者也将其构建为多功能纳米光敏剂(MBNPs),并以“all-in-one”模式应用于体内癌症光诊治疗。
本文要点:
(1)研究成功地验证了MBNPs的作用机制,并将其应用于细胞和体内癌症PDT。基于独特的癌症微环境,MBNPs可以实现在肿瘤内的精准分布、积累和有效激活,并释放亚甲基蓝以作为一种强效光敏剂而用于光治疗。
(2)PDT结果表明,MBNPs具有优异的肿瘤特异性、显著的PDT疗效和极低的毒性。同时,实验也进一步利用体内近红外荧光和光声成像协同指导PDT治疗。综上所述,基于MBNPs的PDT治疗具有很好的生物安全性,在未来的临床研究应用具有重要的潜力。
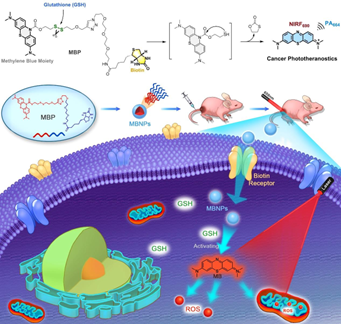
Ke Cheng. et al. Self-assembled Nano-Photosensitizer for Targeted, Activatable, and Biosafe Cancer Phototheranostics. Biomaterials. 2022
https://www.sciencedirect.com/science/article/pii/S0142961222005567



















