目前可用的多发性硬化症(MS)治疗方法减少了对免疫系统不同靶点的神经炎症反应,但会导致严重的副作用,在减缓疾病进展方面疗效有限。基于此,罗马二大N. Poerio和圣心大学G. Di Sante等人在体外评估了一类新型纳米颗粒-脂质体的免疫调节潜力,脂质体由双层磷脂酰丝氨酸(PSCho/PS)组成,外层为磷脂酰丝氨酸,内层为磷脂酰酸(PSCho/PA),单独存在或存在于髓磷脂碱性蛋白(MBP)肽(残基85-99)(PSCho/PS-MBP和PSCho/PA-MBP)。
本文要点:
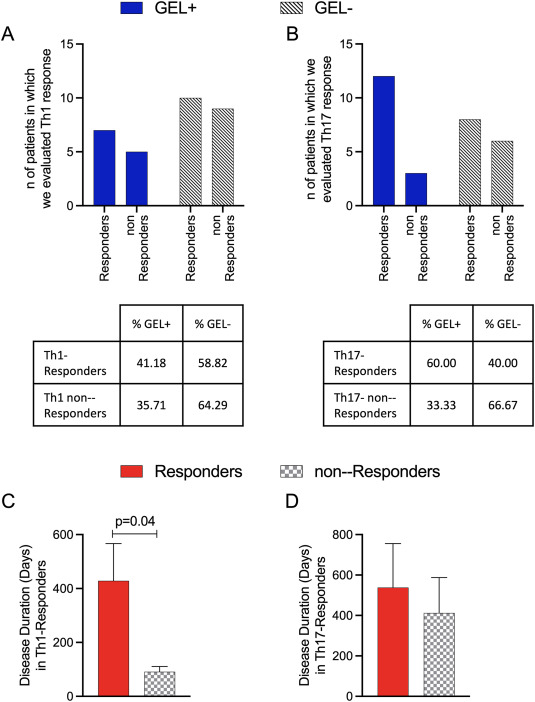
(1)PSCho/PS在促巨噬细胞和抗炎巨噬细胞(M1和M2)中均能有效内化,而PSCho/PA在M2中的内化效果优于M1。PSCho/PS脂质体能够抑制先天促炎细胞因子IL-1β的分泌。PSCho/PS脂质体增加Tregs,减少Th1和Th17 细胞,而PSCho/PA脂质体不能抑制促炎T细胞和促进免疫调节表型(Treg)。在M2标志物基础表达高的MS患者中,PSCho/PS脂质体上调Treg细胞的能力更明显。PSCho/PS脂质体在疾病持续时间超过3个月的MS患者中更有效地减少Th1(而不是Th17)细胞。

(2)另一方面,在MRI上钆增强病变活跃的MS患者以及单核细胞中M1相关标记物基础表达高的MS患者中,Th17 细胞的下调很明显。对MBP驱动的Th1/Th17/Treg反应的调制也观察到了同样的结果。
(3)这些观察结果表明,早期MS与M1的一种硬连线pro-Th1表型相关,该表型在疾病过程中稍后丢失。另一方面,急性炎症事件反映了M2表型的暂时下降,但在PSCho/PS脂质体治疗后可恢复。因此,这些数据表明单核/巨噬细胞可能在MS过程中发挥重要的调节功能,提示PSCho/PS和PSCho/PS- mbp作为抑制促炎免疫反应和促进其调节分支的新治疗工具。
参考文献:
M. Tredicine, F. Ria, N. Poerio, M. Lucchini, A. Bianco, F. De Santis, M. Valentini, V. De Arcangelis, M. Rende, A.M. Stabile, A. Pistilli, C. Camponeschi, V. Nociti, M. Mirabella, M. Fraziano, G. Di Sante. Liposome-based nanoparticles impact on regulatory and effector phenotypes of macrophages and T cells in multiple Sclerosis patients. Biomaterials 2022
DOI:10.1016/j.biomaterials.2022.121930
https://doi.org/10.1016/j.biomaterials.2022.121930



















