尽管免疫检查点阻断(ICB)治疗在癌症治疗方面取得了一系列的成功,但基于ICB的三阴性乳腺癌(TNBC)免疫治疗仍然存在免疫抑制性肿瘤微环境(ITM)的问题。为了突破TNBC免疫治疗的瓶颈,上海交通大学汪登斌教授和同济大学张兵波研究员设计了一种自级联的单分子前药,其由酸性激活的阿霉素和caspase-3响应性肽偶联的聚集诱导发光分子(AIEgen)光敏剂所组成。
本文要点:
(1)该前药不仅能在酸性肿瘤微环境中主动释放阿霉素,还能激活凋亡相关的caspase-3。随后,激活的caspase-3会反过来触发光敏剂的释放和原位聚集。研究发现,该单分子前药能够表现出与体内小分子类似的肾脏清除特性,而聚集的AIEgens能够在肿瘤内有效保留,以实现对肿瘤的长期荧光成像和可重复光动力治疗(PDT)。
(2)研究发现,PDT可促进TNBC细胞的免疫原性细胞死亡和树突状细胞的成熟。实验结果表明,可重复的PDT联合ICB治疗能够进一步促进细胞毒性T淋巴细胞的增殖和瘤内浸润,有效抑制肿瘤的生长和肺转移。综上所述,该研究构建的前药能够作为一种逆转ITM并促进ICB介导的TNBC免疫治疗的自级联化疗-PDT策略。
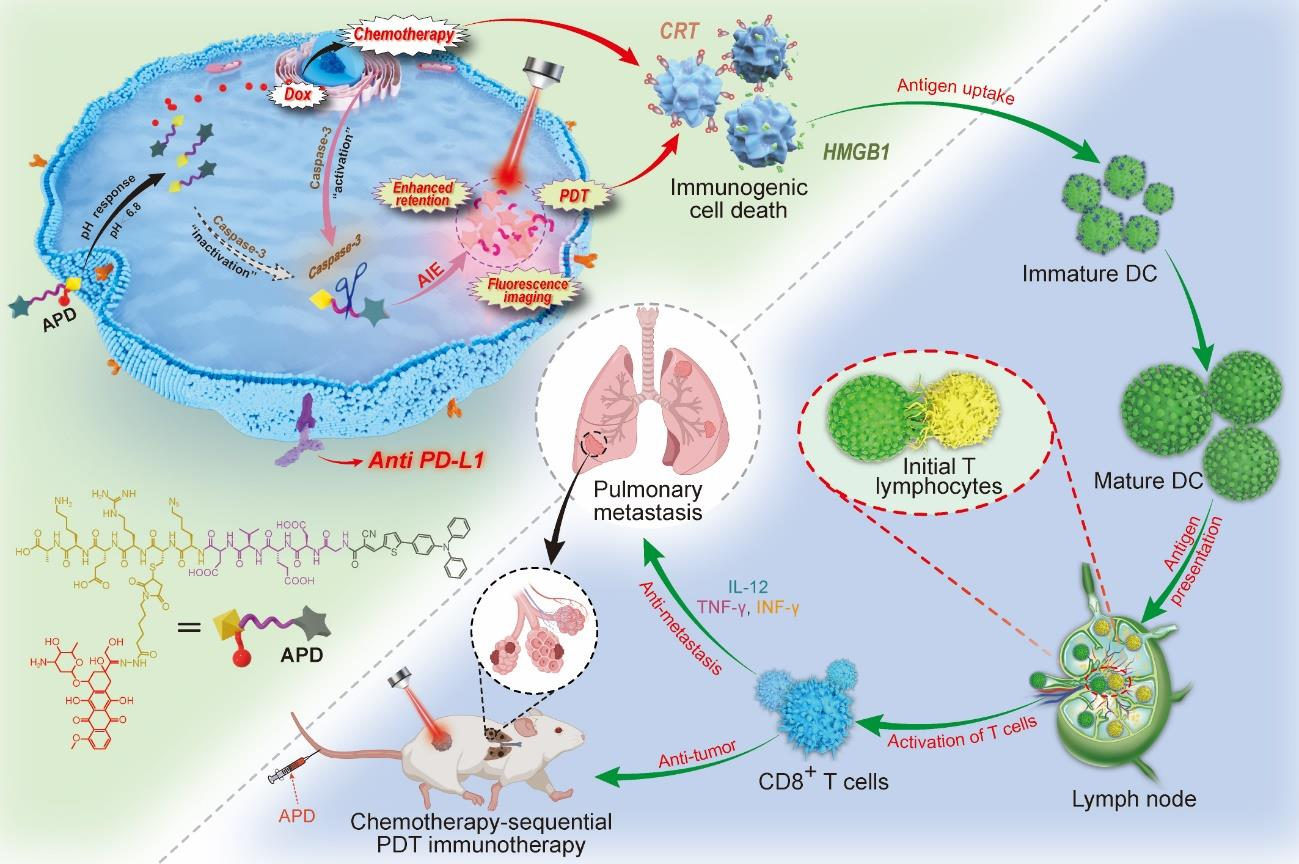
Defan Yao. et al. A self-cascaded unimolecular prodrug for pH-responsive chemotherapy and tumor-detained photodynamic-immunotherapy of triple-negative breast cancer. Biomaterials. 2022
https://www.sciencedirect.com/science/article/pii/S0142961222005609



















