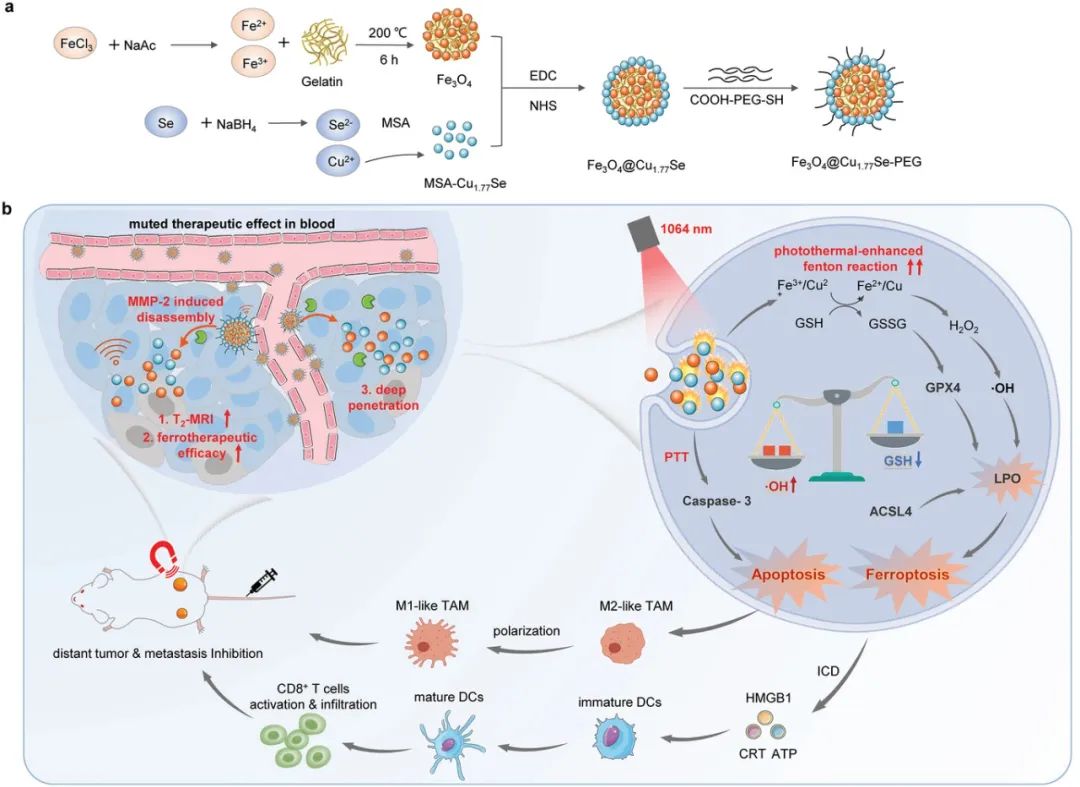
尽管铁疗法在癌症治疗中大有可为,但目前的铁疗法存在抗肿瘤铁死亡功效受损和对肿瘤特异性低的问题。鉴于此,华中科技大学张研等人报道了一种蛋白酶可激活的纳米酶 (Fe3O4@Cu1.77Se) 用于光声和肿瘤增强磁共振成像 (MRI) 引导的二次近红外光热铁死亡癌症治疗。
本文要点:
1)Fe3O4@Cu1.77Se在生理条件下保持稳定,但会分解以增加反应性肿瘤内铁供应,通过 Fenton 反应增加羟基自由基的产生和响应肿瘤微环境中过表达的基质金属蛋白酶而消耗 GSH,导致肿瘤细胞铁死亡的放大以及增强的T2加权MRI对比度。进一步与第二次近红外光照射结合以产生局部热不仅触发有效的光热治疗和光声成像,而且更重要的是,增强芬顿反应以促进铁性肿瘤细胞死亡。
2)这种协同作用导致肿瘤相关巨噬细胞从促进肿瘤的M2型极化为杀死肿瘤的M1型,并诱导肿瘤细胞的免疫原性细胞死亡,进而促进树突状细胞的成熟和细胞毒性T细胞的浸润。肿瘤中的淋巴细胞,有助于显著抑制肿瘤。本研究提出了一种新型可激活铁纳米治疗诊断学,用于时空控制抗肿瘤铁死亡反应。
参考文献:
Qin, W., et al., Protease-Activatable Nanozyme with Photoacoustic and Tumor-Enhanced Magnetic Resonance Imaging for Photothermal Ferroptosis Cancer Therapy. Adv. Funct. Mater. 2022, 2209748.
https://doi.org/10.1002/adfm.202209748


















