开发对巨噬细胞极化具有免疫调节作用的纳米系统对于靶向巨噬细胞的免疫治疗而言具有重要意义。有鉴于此,南京林业大学夏兵教授、南京大学沈萍萍教授和格罗宁根大学Hélder A. Santos证明了与荧光、亲脂性和阳离子罗丹明110分子偶联的靶向线粒体的牛血清白蛋白(BSAs)可以有效地增强巨噬细胞促炎表型的基因表达,并相应地抑制其抗炎表型的基因表达。
本文要点:
(1)研究发现,多孔硅纳米载体可进一步促进这些靶向线粒体的BSAs在体内外的免疫调节性能,并伴有促炎介质的分泌,包括肿瘤坏死因子α、一氧化氮和活性氧(ROS)等。同时,BSA包覆层还可以改善多孔硅纳米内核对巨噬细胞的生物相容性。
(2)机制研究表明,多孔硅纳米载体可以有效地将靶向线粒体的BSA递送到巨噬细胞中,进而通过干扰线粒体呼吸链以产生线粒体ROS,触发促炎转化的下游信号转导通路。实验结果表明,该多孔silicon@BSA纳米系统具有良好的生物安全性、多种负载能力以及较强的促炎调节作用,在癌症或病毒/细菌相关的感染性疾病的联合化疗免疫治疗方面具有重要的应用潜力。
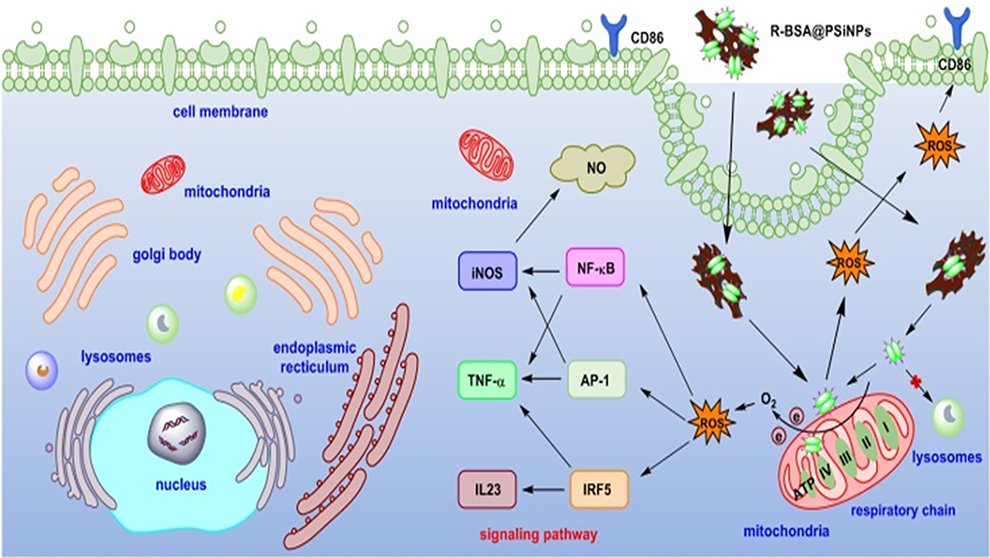
Jialiang Li. et al. Porous Silicon Nanocarriers Boost the Immunomodulation of Mitochondria-Targeted Bovine Serum Albumins on Macrophage Polarization. ACS Nano. 2023
DOI: 10.1021/acsnano.2c07439
https://pubs.acs.org/doi/10.1021/acsnano.2c07439



















