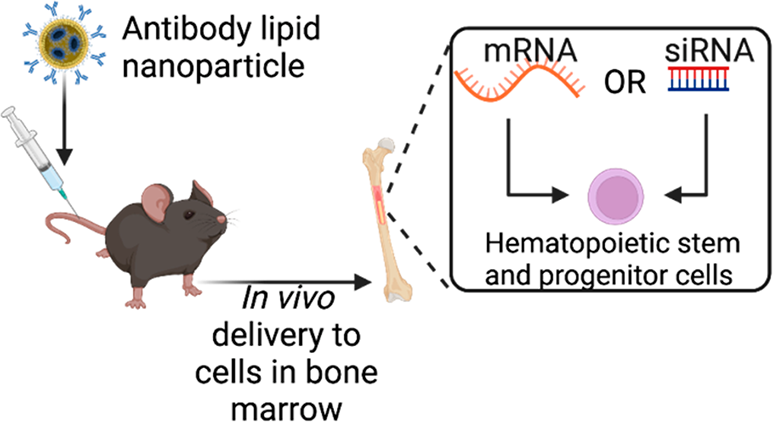
体外自体造血干细胞(HSC)基因疗法是一种能够治疗血液病的新方法。然而,由于制造较为复杂和潜在的毒性问题,这些疗法仍存在一些局限性。有鉴于此,麻省理工学院Daniel G. Anderson开发了一种靶向c-kit (CD117)抗体的脂质纳米颗粒(LNP),其在单次静脉注射后可以将RNA (siRNA和mRNA)递送到啮齿动物体内的造血干细胞。
本文要点:
(1)研究表明,这种靶向递送系统不需要通过干细胞收集、培养和动员造血干细胞来增强递送。
(2)实验结果表明,以1 mg kg−1剂量递送Cre重组酶mRNA可以促进对体内几乎所有(约90%)造血干细胞和祖细胞(HSPCs)的基因编辑,并使得编辑细胞保持其干性和功能,以产生高水平的编辑成熟免疫细胞。
Dennis Shi. et al. In Vivo RNA Delivery to Hematopoietic Stem and Progenitor Cells via Targeted Lipid Nanoparticles. Nano Letters. 2023
DOI: 10.1021/acs.nanolett.3c00304
https://pubs.acs.org/doi/10.1021/acs.nanolett.3c00304



















