肝纤维化是一种慢性疾病,目前临床上还没有有效的治疗方法。CRISPR/Cas9等基因编辑系统在生物医学领域中表现出了巨大的应用潜力。然而,由于RNA探针不稳定以及需要进入细胞核等问题的限制,如何递送核糖核蛋白成为了一项极具挑战性的难题。近年来,结构导向内切酶(SGN)已被证明能够作为一种由核酸酶和稳定的DNA探针所组成的高效基因编辑系统,其可以通过靶向核外特定的mRNA来调节蛋白质的表达。有鉴于此,中国药科大学赵灵之研究员、徐澍研究员、彭娟娟研究员和卞金磊副教授将SGN偶联到纳米胶束上,构建了一种新型的递送系统。
本文要点:
(1)在所制备的材料中,由于内切酶和探针被限制在40 nm的纳米胶束内,因此这两种组分之间的碰撞机会大大增加,使得mRNA在被探针捕获后会被立即切割,从而产生空间诱导的核苷酸识别-切割加速效应。
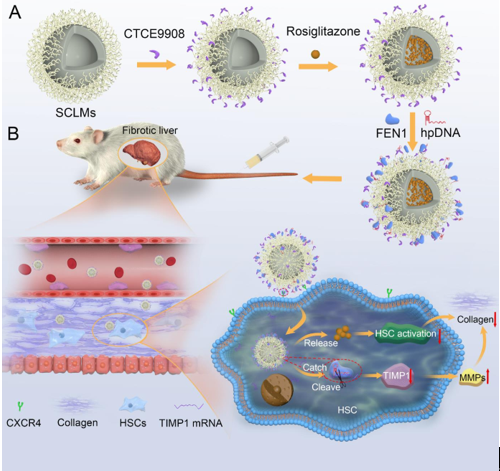
(2)该递送系统可向肝星状细胞共递送SGN和罗格列酮药物,以分别下调组织金属蛋白酶-1的表达和使肝星状细胞失活,从而治疗肝纤维化。实验结果表明,该系统可通过促进胶原降解和抑制胶原生成的双向调控作用以成功逆转小鼠肝纤维化,由此证明了SGN系统具有作为基因药物的重要功能。
Jiayu Gu. et al. Reversal of hepatic fibrosis by the co-delivery of drug and ribonucleoprotein-based genome editor. Biomaterials. 2023
https://www.sciencedirect.com/science/article/pii/S0142961223001412



















