金属调节的细胞死亡策略已被广泛用于抗肿瘤治疗,如铜死亡、铁死亡和化学动力学治疗(CDT)等。准确和特异性地提高癌细胞中的金属离子水平是提高其治疗指数的关键。深圳大学林静教授构建了一种基于Croc染料- Fe2+纳米探针的可编程型可控光热诱导的CDT递送系统。
本文要点:
(1)具有多种富电子铁螯合基团的Croc能够形成精确的1:1(化学计量)Croc-Fe2+配合物,并稳定维持Fe2+的价态。在“酸性和近红外(NIR)光”的“双钥匙”刺激下,CFNPs可以在癌组织中实现对pH响应的可视化和Fe2+的准确释放。此外,酸性肿瘤微环境也能够激活CFNPs的近红外荧光/光声成像和光热等性能。
(2)在外源近红外光照射下,CFNPs能够在体内精确可视化Croc-Fe2+复合物的递送,并通过光热引发Fe2+释放,从而实现肿瘤CDT。综上所述,该研究利用多尺度动态成像技术,以可编程的方式实现了Fe2+时空可控释放,揭示了肿瘤pH值、光热效应、CDT等多米诺骨牌效应,并能够在疾病微环境中对治疗全景进行有效反馈。
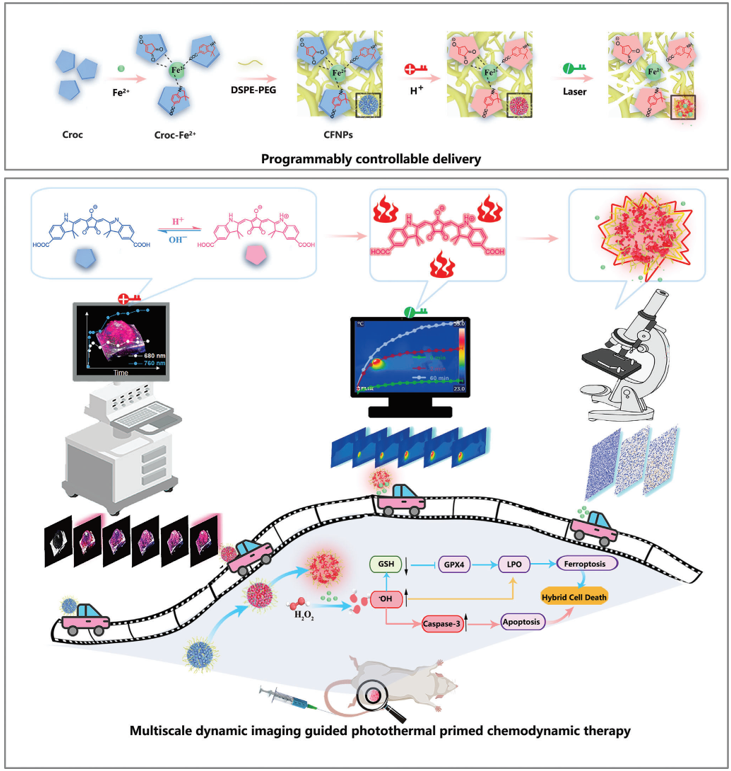
Xinming Zhang. et al. Programmably Controllable Delivery of Metastable Ferrous Ions for Multiscale Dynamic Imaging Guided Photothermal Primed Chemodynamic Therapy. Advanced Materials. 2023
DOI: 10.1002/adma.202210876
https://onlinelibrary.wiley.com/doi/10.1002/adma.202210876



















