纳米载体辅助的声动力治疗(SDT)能够有效克服声敏剂所存在的局限性问题,在深部肿瘤的靶向治疗方面具有巨大的应用潜力。然而,基于纳米载体的体内SDT仍然会受到其固有毒性和非特异性载物释放等问题的限制。有鉴于此,仁川大学Min Suk Shim、Won Jong Rhee、嘉泉大学Young Tag Ko和梨花女子大学Minjong Lee开发了一种可生物还原外泌体,并将其用于安全、肿瘤特异性地递送靶向线粒体的声敏剂[三苯膦偶联的Ce6(T-Ce6)]和糖酵解抑制剂(FX11)。
本文要点:
(1)实验将带有由氧化还原切割的二硒胺连接子的脂质嵌入到外泌体中,使其能够响应肿瘤微环境中过表达的谷胱甘肽以实现药物释放。可生物还原外泌体能够在肿瘤细胞的还原性环境中促进其有效载荷的细胞质释放。在超声照射下,它们可显著增强药物释放和声动力效应。研究发现,在线粒体靶向积累的T-Ce6能够在US照射下有效地破坏细胞的线粒体,进而加速细胞凋亡。
(2)此外,FX11也能够显著抑制细胞的能量代谢,增强靶向线粒体的SDT的抗肿瘤作用。实验结果表明,可生物还原外泌体能够通过结合靶向线粒体的SDT和能量代谢靶向治疗的方式有效抑制小鼠肿瘤的生长,且不会产生明显的全身毒性。综上所述,这项研究能够为利用双重刺激响应性外泌体包封声敏剂以实现安全的靶向声动力癌症治疗提供新的见解。
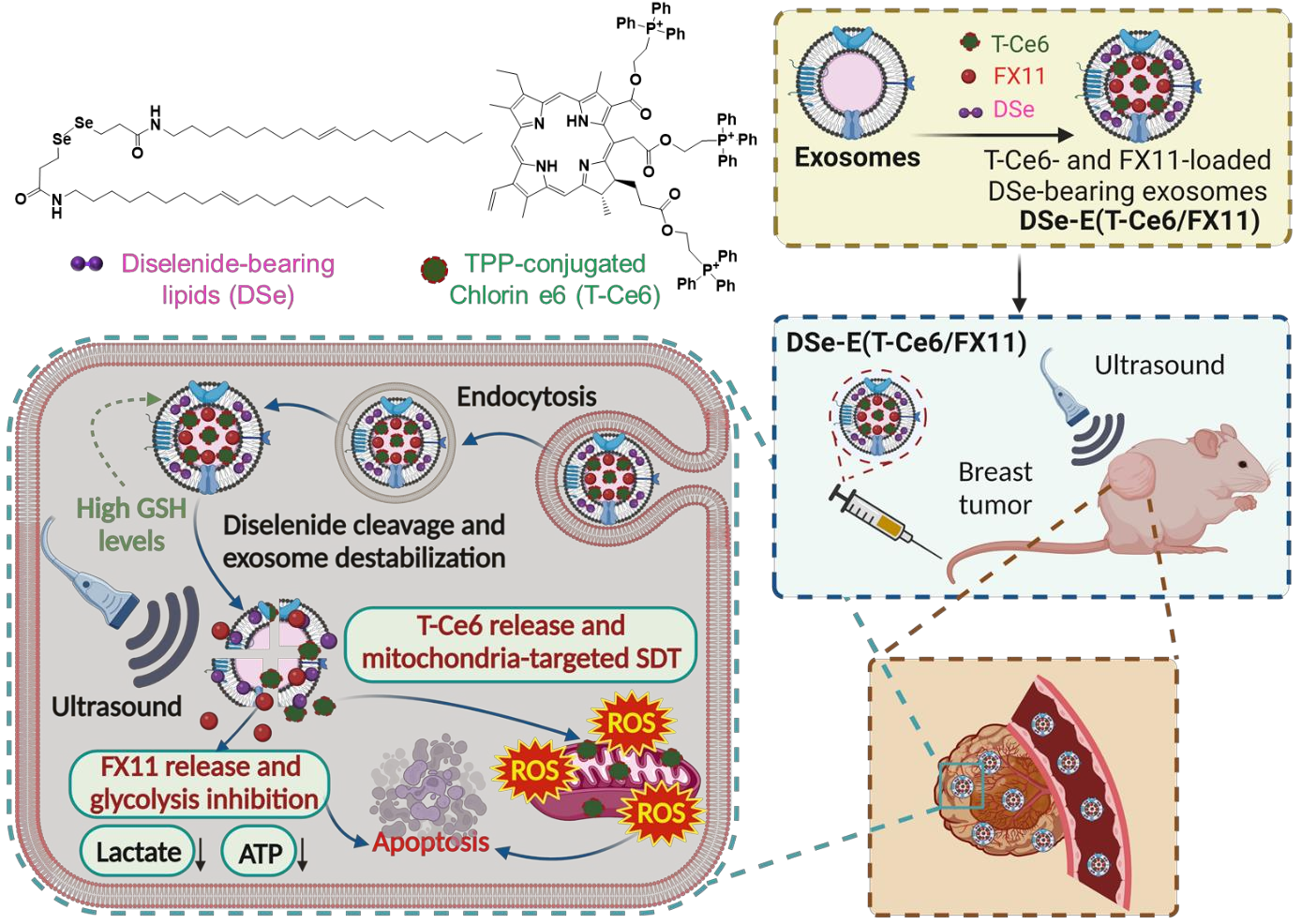
Thuy Giang Nguyen Cao. et al. Bioreducible exosomes encapsulating glycolysis inhibitors potentiate mitochondria-targeted sonodynamic cancer therapy via cancer-targeted drug release and cellular energy depletion. Biomaterials. 2023
https://www.sciencedirect.com/science/article/pii/S0142961223002508



















