为了研究肿瘤靶向型光激活化疗的应用潜力,莱顿大学Sylvestre Bonnet和大连理工大学孙文教授将手性钌抗癌药物Λ/Δ-[Ru(Ph2phen)2(OH2)2]2+通过M和H残基与金属的直接配位作用结合到含RGD的Ac-MRGDH-NH2肽上。
本文要点:
(1)该设计策略能够产生两个环金属肽的非对映异构体,Λ-[1]Cl2和Δ- [1]Cl2。在黑暗环境中,钌螯合肽具有三重作用。首先,它可阻止其他生物分子与金属中心配合;其次,它的亲水性会使得[1]Cl2具有两亲性,进而使其能够在培养基中自组装成纳米颗粒;第三,它可通过与整合素的强结合(Λ-[1]Cl2与αIIbβ3的结合,Kd = 0.061 μM)以作为肿瘤靶向模块,进而在体外实现受体介导的偶联物摄取。对A549、U87MG和PC-3人癌细胞二维(2D)单层和U87MG三维(3D)肿瘤球体的光毒性研究表明,[1]Cl2的两种异构体具有强光毒性,其光指数高达17。
(2)机制研究表明,这种光毒性是由光动力治疗(PDT)和光激活化疗(PACT)等作用相结合所产生的。在皮下U87MG胶质母细胞瘤小鼠模型的体内研究表明,[1]Cl2可在注射12小时后在肿瘤中有效积累,并在绿光照射下表现出比非靶向类似物钌络合物[2]Cl2更强的杀瘤作用。综上所述,该研究表明具有光敏功能的整合素靶向型钌基抗癌化合物在脑癌的体内治疗方面具有重要的应用潜力。
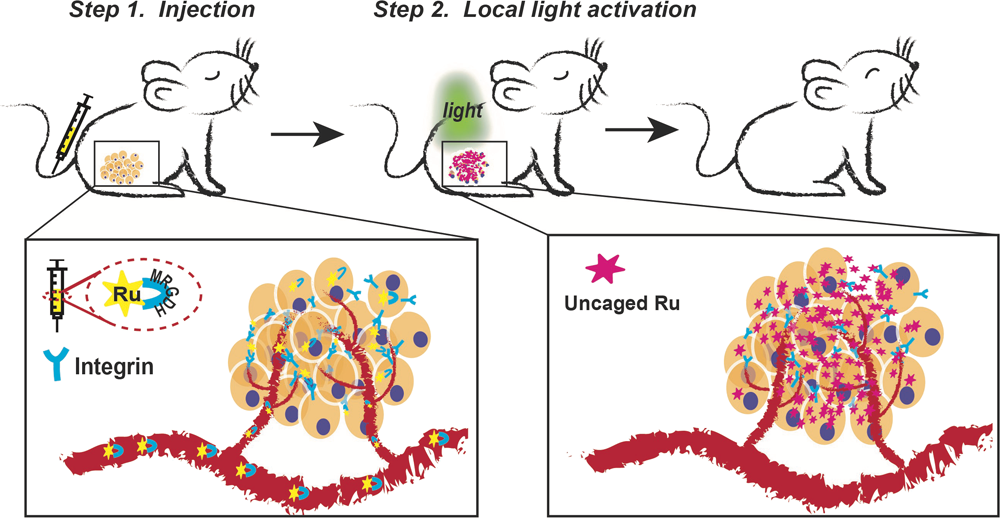
Liyan Zhang. et al. Cyclic Ruthenium-Peptide Conjugates as Integrin Targeting Phototherapeutic Prodrugs for the Treatment of Brain Tumors. Journal of the American Chemical Society. 2023
DOI: 10.1021/jacs.3c04855
https://pubs.acs.org/doi/10.1021/jacs.3c04855



















