肿瘤光学治疗具有操作方便、耐药性低且时空可控等优点,但在肿瘤细胞可及性和间歇性光激发等方面仍面临挑战。有鉴于此,西南交通大学李孝红教授提出了一种利用持续发光(PL)激发光热治疗(PTT)、并同时实现热泳推动的运动以及PL触发NO释放的策略,该PL发射可通过超声刺激进行充电,适用于深部肿瘤治疗。
本文要点:
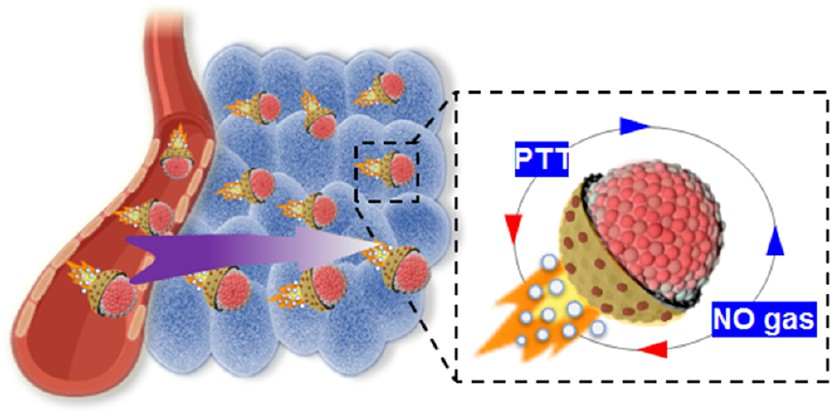
(1)实验将机械发光(ML)SrAl2O4:Eu2+纳米点(SAOE)和PL纳米点ZnGa2O4:Cr3+纳米点(ZGC)沉积在介孔硅材料上以制备得到mSZ纳米粒子(NPs),随后利用聚多巴胺(PDA)对其进行包覆,并进一步负载NO供体,构建了具有Janus结构的mSZ@PDA-NO NPs。研究发现,SAOE纳米点的ML发射带与ZGC的激发带重叠,并且该持续性近红外(NIR)发射可以被超声反复激活。
(2)作为内部近红外光源的PL发射能够产生热泳力和NO气体推动力,从而驱动Janus NPs的运动。与660 nm和808 nm的间歇性近红外光刺激相比,超声激活的NPs的持续运动可增强其细胞摄取、实现持久的PTT和提高细胞内NO水平,从而能够在不使用任何化疗药物的情况下显著抑制肿瘤细胞。此外,超声激活的持续运动也能够促进PTT/NO治疗药物在肿瘤内的积累和分布。与利用外部近红外光照射的治疗模式相比,该策略能够表现出更高的肿瘤生长抑制效率,并实现更长的动物生存期和更高的肿瘤内NO水平。综上所述,该研究能够为激活PL发射和构建PL激发的纳米马达以用于深层组织光学治疗提供一个新的有效策略。
Zhanlin Zhang. et al. Ultrasound-Chargeable Persistent Luminescence Nanoparticles to Generate Self-Propelled Motion and Photothermal/NO Therapy for Synergistic Tumor Treatment. ACS Nano. 2023
DOI: 10.1021/acsnano.3c04906
https://pubs.acs.org/doi/10.1021/acsnano.3c04906



















