由于实体肿瘤的中心细胞具有恶性程度更高和侵袭性更强等特点,因此提高治疗药物的肿瘤穿透性和在肿瘤中心激活免疫反应对于肿瘤治疗而言具有重要的意义。有鉴于此,南京大学宋玉君教授、南京师范大学于海佳教授、南京市第一医院何帮顺教授和南京中医药大学Jingjing Yang构建了聚多巴胺包覆、携带负载CRISPR-Cas9质粒的脂质体(Lipo-P)的大肠杆菌Nissle 1917(EcN),并将其用于增强对深部肿瘤的免疫治疗,以同时激活先天性免疫和适应性免疫。
本文要点:
(1)通过靶向乏氧以在肿瘤中心聚集后,Lipo-P会因对活性氧(ROS)响应的连接子被还原而发生分离,进而通过消耗Hsp90α以降低癌细胞的热抗性。随后,聚多巴胺可在近红外光照射下通过诱导光热治疗实现有效的肿瘤消融。
(2)实验结果表明,温和的光热疗法可以诱导免疫原性细胞死亡,而细菌感染也能够在肿瘤组织中引发先天性免疫。综上所述,该研究设计的细菌辅助方法能够为治疗深部肿瘤提供一种光热增敏的免疫治疗策略。
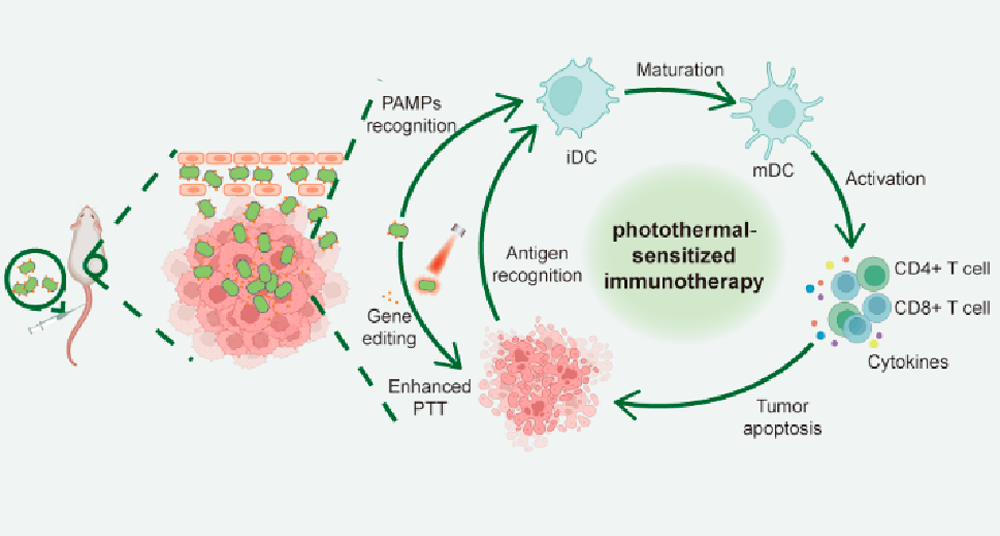
Wen Luo. et al. Deep Tumor Penetration of CRISPR-Cas System for Photothermal-Sensitized Immunotherapy via Probiotics. Nano Letters. 2023
DOI: 10.1021/acs.nanolett.3c02061
https://pubs.acs.org/doi/10.1021/acs.nanolett.3c02061



















