嵌合抗原受体(CAR) T细胞为血液系统恶性肿瘤的治疗带来了一场新的变革。然而,由于肿瘤微环境(TME)的免疫抑制特性会影响CAR T细胞的浸润能力,因此CAR T细胞对实体瘤的治疗效率仍然较低。莫纳什大学G. P. Risbridger和彼得·麦卡伦癌症中心R. A. Taylor评估了Lewis Y抗原(LeY)特异性CAR T细胞在前列腺癌患者源性异种移植(PDX)模型中的疗效。
本文要点:
(1)在体外,LeY CAR T细胞可直接杀死雄激素受体(AR)阳性或AR-null PDXs衍生的类器官。在体内,单独使用LeY CAR T细胞的治疗组的肿瘤生长没有减少,而之前接受了单次卡铂治疗的LeY CAR T细胞治疗组的肿瘤负荷会发生降低。研究发现,卡铂对TME具有促炎作用,能够改变癌症相关成纤维细胞表型、增强细胞外基质降解和重新引导M1巨噬细胞的分化,从而可以增强CAR T细胞的早期和持久的浸润。
(2)在对卡铂敏感性较低的PDX模型中,CAR T细胞浸润会受到抑制。然而,随着T细胞活化的增加,肿瘤负荷仍然会发生降低。综上所述,该研究证明了卡铂可以改善CAR T细胞治疗的效果,其改善的程度也与诱导的TME变化密切相关。
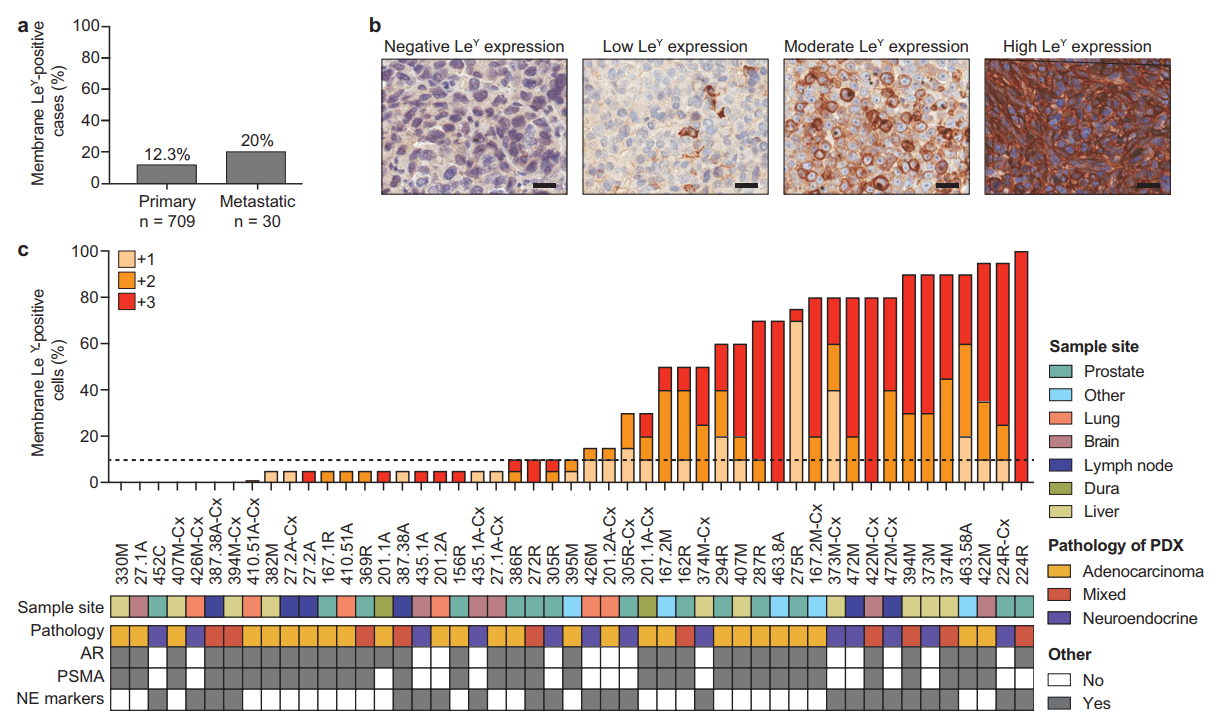
L. H. Porter. et al. Low-dose carboplatin modifies the tumor microenvironment to augment CAR T cell efficacy in human prostate cancer models. Nature Communications. 2023
https://www.nature.com/articles/s41467-023-40852-3



















