传统的肿瘤放疗增敏剂的效果往往会受其对肿瘤微环境(TME)的调节能力不足及其在生物屏障处的细胞摄取不足等问题的限制。有鉴于此,重庆大学罗阳教授、杨纪春副教授和陆军军医大学李建军教授合成了一种细胞外囊泡(EVs)包裹的空心MnO2,并将其用于负载二甲双胍(Met@HMnER),从而开发了一种超高效的放疗(RT)策略,。
本文要点:
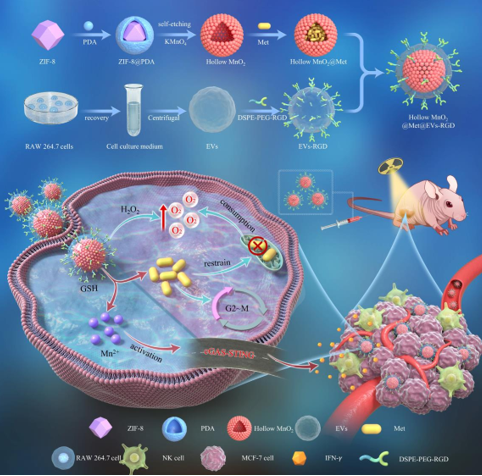
(1)Met@HMnER不仅能催化过表达的H2O2产生O2,还能抑制线粒体的呼吸过程,以减少O2的消耗。这种协同作用能够对细胞内的O2含量起到“开源节流”的作用,极大地缓解TME的乏氧程度,以实现显著的RT增强。此外,靶点修饰的EVs也具有出色的二甲双胍负载能力,并且能够同时增强其对生物屏障的穿透性能。
(2)研究发现,该纳米平台可通过cGAS-STING通路触发实现NK细胞的显著持久的先天免疫激活。研究者也在远端转移和原位复发等模型中进一步验证了该纳米平台能够增强免疫活性,因此有望为增强先天免疫在临床肿瘤治疗中的作用开辟新的途径。
Jichun Yang. et al. Ultra-efficient radio-immunotherapy for reprogramming the hypoxic and immunosuppressive tumor microenvironment with durable innate immune memory. Biomaterials. 2023
https://www.sciencedirect.com/science/article/pii/S0142961223003113



















