哺乳动物细胞的质膜(PM)含有多种脂质、蛋白质和碳水化合物,其对于健康和疾病的系统识别和交流而言至关重要。细胞膜包被技术能够将天然质膜的独特性能赋予被包裹的纳米颗粒表面,使其成为可用于药物递送、免疫调节和疫苗接种的强大平台。然而,目前的包覆方法往往会破坏PM的复杂性和功能性的基本特征,未能充分展现自然系统的显著优势。有鉴于此,南开大学刘书琳教授和伊利诺大学芝加哥分校Wonhwa Cho通过结合仿生和系统性变异的方法优化脂质成分而开发了一种新的脂质包覆方法,并将其用于定制设计纳米载体系统,以实现对药物的精准递送。
本文要点:
(1)研究发现,优化后的脂质所包被的纳米载体在生物利用度、肿瘤靶向性、肿瘤穿透性、细胞摄取和药物释放等方面具有独特的优势。
(2)综上所述,该研究能够为合理设计和优化肿瘤化疗药物的纳米载体提供新的思路,并为通过系统整合其他成分以进一步定制模拟细胞膜的纳米载体奠定重要的研究基础。
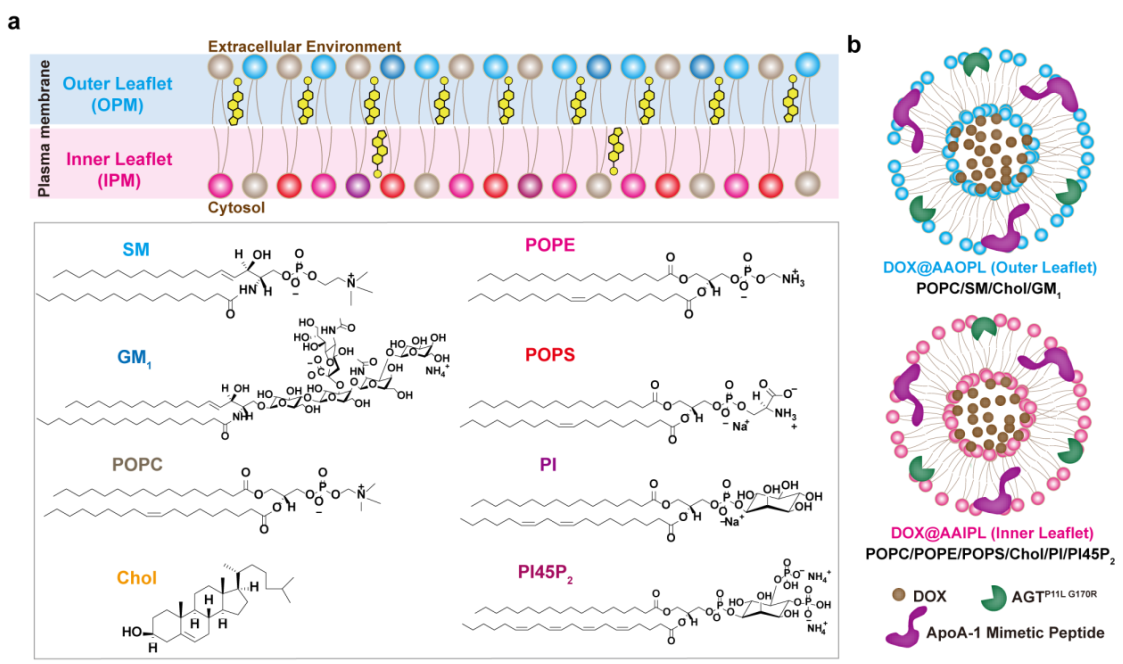
Di Ning. et al. Lipid-Centric Design of Plasma Membrane-Mimicking Nanocarriers for Targeted Chemotherapeutic Delivery. Advanced Materials. 2023
DOI: 10.1002/adma.202306808
https://onlinelibrary.wiley.com/doi/10.1002/adma.202306808



















