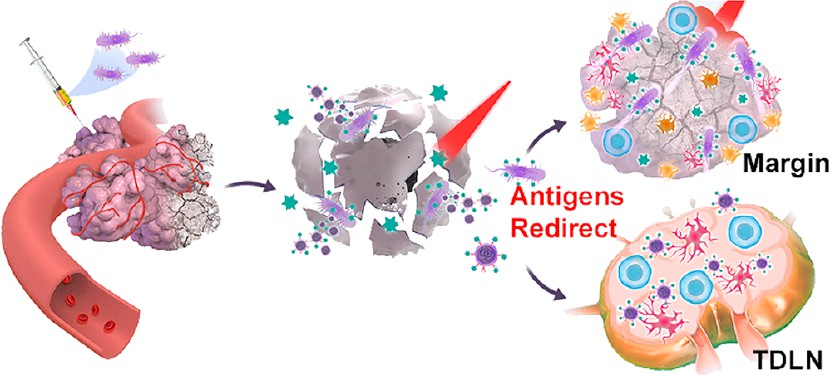
针对恶性肿瘤的癌症疫苗研发已经取得了重大进展。然而,肿瘤内部天然的免疫抑制环境(即肿瘤微环境(TME))仍会严重阻碍肿瘤内部抗原提呈细胞(APCs)对抗原的摄取和提呈,进而导致针对癌症的免疫反应活化效率不足。相反,肿瘤周围组织中的免疫细胞则能够维持其正常功能。有鉴于此,南方医科大学第十附属医院李振华教授和河北大学张金超教授设计了一种增强癌症免疫治疗的新方法,即利用工程光合细菌(PSB)及其外膜囊泡(OMVPSB)捕获抗原并将其转运到肿瘤的外部区域。
本文要点:
(1)实验利用马来酰亚胺修饰PSB(PSB-MAL),其在暴露于近红外(NIR)激光介导的光热治疗(PTT)时可诱导癌细胞死亡和肿瘤抗原的释放。随后,具有NIR趋向性的PSB-MAL能够在NIR激光照射下将这些肿瘤抗原转运到肿瘤外周区域。研究发现,PSB-MAL衍生的OMVPSB-MAL可有效地捕获并递送抗原到肿瘤引流淋巴结(TDLNs)中,以促进TDLNs中成熟且功能完整的APCs的抗原提呈。
(2)PSB-MAL、OMVPSB-MAL和APCs之间复杂的通信网络能够促进肿瘤抗原在肿瘤外周和TDLNs中的高效提呈,显著增加肿瘤内细胞毒性T淋巴细胞(CTL)的浸润,进而能够在黑色素瘤和乳腺癌模型中触发产生强效的抗肿瘤免疫反应。实验结果表明,这一系列级联事件能够增强对肿瘤转移和复发的抑制作用,从而证明了该方法的有效性。综上所述,该研究利用细菌和OMV重定向肿瘤抗原以增强癌症免疫治疗,能够为开发个性化癌症疫苗接种策略提供一条新的途径。
Dandan Han. et al. Redirecting Antigens by Engineered Photosynthetic Bacteria and Derived Outer Membrane Vesicles for Enhanced Cancer Immunotherapy. ACS Nano. 2023
DOI: 10.1021/acsnano.3c01912
https://pubs.acs.org/doi/10.1021/acsnano.3c01912



















