利用巨噬细胞吞噬肿瘤细胞已发展成为一种重要的肿瘤治疗策略。然而,肿瘤微环境中的免疫抑制性M2型巨噬细胞和肿瘤细胞高表达的抗吞噬信号仍会严重影响该策略的治疗效果。有鉴于此,南京大学宋玉君教授开发了一种可基因编辑的钯基生物正交纳米平台(HBPdC),其由CRISPR/Cas9基因编辑系统连接的钯纳米簇和透明质酸表面层所组成。
本文要点:
(1)HBPdC纳米平台具有良好的肿瘤靶向性,能够在肿瘤微环境中引发类芬顿反应,进而产生活性氧以用于化学动力学治疗和实现巨噬细胞的M1型极化,从而直接清除肿瘤细胞,并刺激巨噬细胞的抗肿瘤反应。研究发现,HBPdC可通过基因编辑重编程肿瘤细胞,降低CD47和脂肪细胞质膜相关蛋白的表达,从而促进其被巨噬细胞识别和吞噬。
(2)此外,HBPdC也能够通过生物正交催化诱导分离的前药被激活,从而通过化疗增强肿瘤细胞的死亡。实验结果表明,HBPdC中的Pd纳米团簇能够通过基本代谢途径被充分清除,由此表明其具有良好的生物相容性和生物安全性。综上所述,该研究开发的HBPdC系统能够显著增强巨噬细胞的吞噬作用,其在肿瘤治疗领域中具有广阔的应用前景。
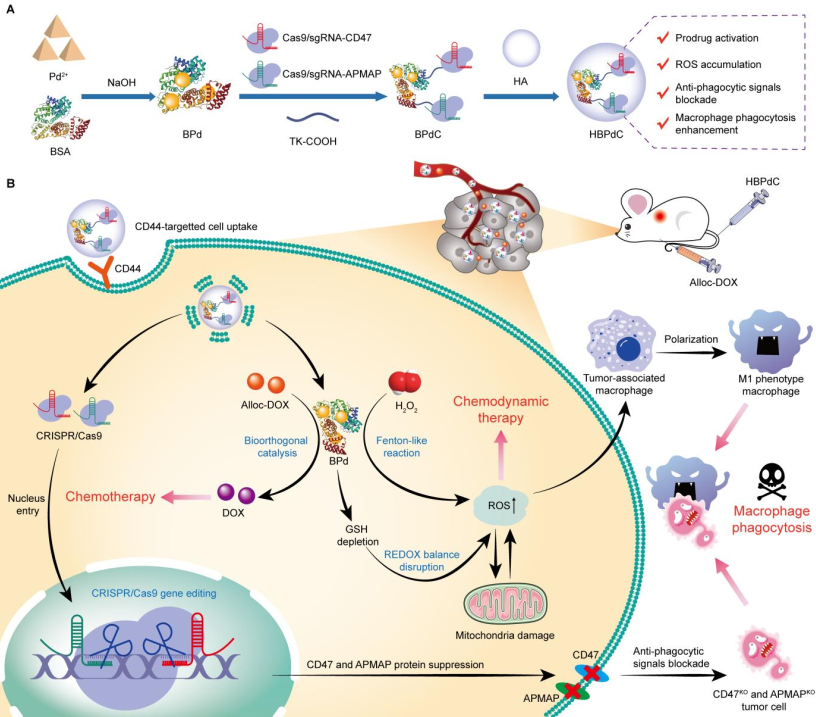
Shujun Feng. et al. A Gene-Editable Palladium-Based Bioorthogonal Nanoplatform Facilitates Macrophage Phagocytosis for Tumor Therapy. Angewandte Chemie International Edition. 2023
DOI: 10.1002/anie.202313968
https://onlinelibrary.wiley.com/doi/10.1002/anie.202313968



















