免疫检查点阻断(ICB)抗体免疫疗法已被证明能够对多种癌症产生临床治疗收益。然而,肿瘤免疫原性缺陷和免疫抑制性的肿瘤微环境仍会严重抑制肿瘤免疫治疗的效果。细胞焦亡是一种细胞程序性死亡形式,可释放肿瘤抗原,激活有效的肿瘤免疫原性,以提高ICB的效率。然而,目前有效的细胞焦亡用于肿瘤治疗的研究有限。有鉴于此,中南大学刘又年教授、邓留教授和华中师范大学朱成周教授开发了一种基于空心碳纳米酶、温和热增强焦亡介导的免疫治疗策略,它可以在肿瘤微环境中特异性地放大氧化应激触发的焦亡,并同步增强焦亡介导的抗癌反应。
本文要点:
(1)经铁和铜原子修饰的空心碳球(HCS-FeCu)具有多种模拟酶活性,其在光激活下可通过活性氧(ROS)-Tom20-Bax-Caspase 3-gasdermin E(GSDME)信号通路诱导细胞焦亡。体内外抗肿瘤实验结果表明,HCS-FeCu纳米酶能够诱导产生显著的细胞焦亡。此外,温和光热激活的细胞焦亡能够联合抗PD-1以增强抗肿瘤免疫治疗。
(2)理论计算结果表明,温和光热可刺激产生高能电子,进而增强HCS-FeCu表面与吸附氧的相互作用,以促进氧分子的活化,从而提高ROS的产生效率。综上所述,该研究工作开发了一种能够有效地将免疫“冷”肿瘤转化为“热”肿瘤的新方法,其对于改善临床免疫治疗而言具有重要意义。
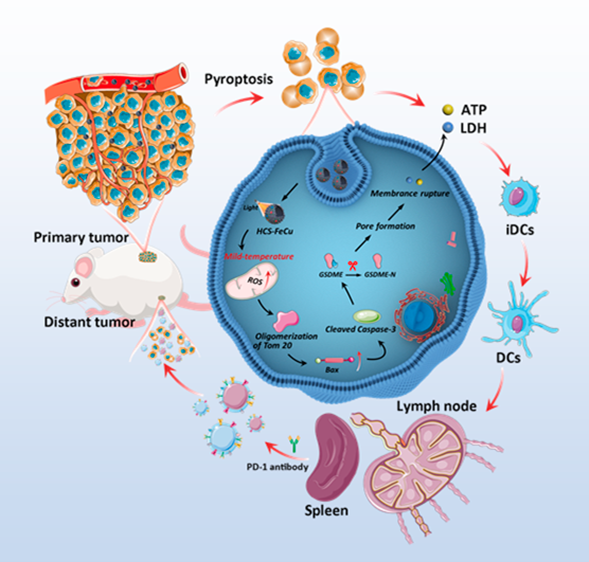
Na Tao. et al. A Mild Hyperthermia Hollow Carbon Nanozyme as Pyroptosis Inducer for Boosted Antitumor Immunity. ACS Nano. 2023
DOI: 10.1021/acsnano.3c07601
https://pubs.acs.org/doi/10.1021/acsnano.3c07601



















