肿瘤相关巨噬细胞(TAMs)与多形性胶质母细胞瘤(GBM)的进展及其对常规化疗的耐药性密切相关。TAMs靶向治疗联合常规化疗有望成为治疗GBM的新策略。然而,血脑屏障(BBB)仍会严重限制该治疗策略的效果。此外,区分不同靶细胞的能力的缺乏也是实现精准治疗所面临的一项严峻挑战。有鉴于此,北京理工大学阮少波教授、黄渊余教授和四川大学高会乐教授构建了一种对组织蛋白酶B(CTSB)响应的程序性脑靶向递送系统(D&R-HM-MCA),并将其用于同时靶向TAMs和GBM。
本文要点:
(1)D&R-HMMCA可通过低密度脂蛋白受体相关蛋白1(LRP1)介导的跨细胞作用穿过BBB。在到达GBM部位后,外部的angiopep-2修饰可通过CTSB响应肽的裂解而从D&R-HM-MCA中分离,从而能够避免由LRP1介导的外排。研究发现,暴露的p-氨基苯基-α-D-吡喃甘露糖苷(MAN)修饰可进一步识别GBM上的葡萄糖转运蛋白1(GLUT1)和TAMs上的巨噬细胞甘露糖受体(MMR)。
(2)D&R-HM-MCA在实现化疗杀伤GBM的同时,也可诱导TAM发生从抗炎M2表型向促炎M1表型的极化,从而增强化疗,并改善抗GBM的免疫反应。实验结果表明,该CTSB响应性脑靶向递送系统不仅可以提高对大脑的递送效率,而且能够实现靶向GBM的化学-免疫联合治疗。综上所述,该研究设计的策略有望为构建具有多功能性的脑靶向递送系统和高效的治疗方案提供新的思路。
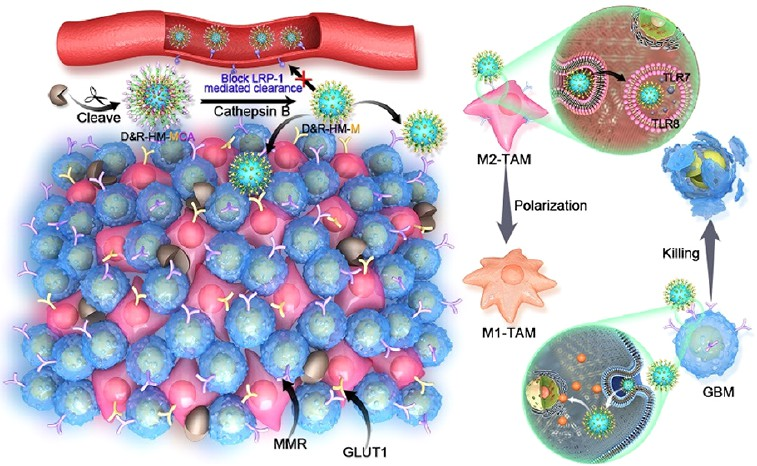
Shaoping Jiang. et al. Cathepsin B‑Responsive Programmed Brain Targeted Delivery System for ChemoImmunotherapy Combination Therapy of Glioblastoma. ACS Nano. 2024
DOI: 10.1021/acsnano.3c11958
https://pubs.acs.org/doi/10.1021/acsnano.3c11958



















