以树突状细胞(DC)为基础的疫苗能够在过继性细胞治疗中增强抗肿瘤免疫的抗原特异性反应。然而,其临床疗效仍会受到MHC I的肿瘤相关抗原(TAAs)呈递较少和淋巴结归巢效率较低等问题的限制。有鉴于此,苏州大学李桢教授将成熟的DC膜包裹在Cu2-xSe纳米粒子(CS NPs)上,合理设计并制备了一种基于DC的纳米疫苗(即DCNV(CSD)纳米疫苗)。
本文要点:
(1)实验从三个方面揭示了CS NPs在DCNV(CSD)纳米疫苗中的重要作用:(1)诱导肿瘤细胞的免疫原性死亡以暴露大量的TAAs;(2)在MHC I的抗原提呈过程中促进TAAs从DC溶酶体逃逸;(3)持续释放微量铜离子以促进T细胞增殖。研究发现,DCNV(CSD)纳米疫苗具有高表达MHC I、CD80、CD86、CCR7和ICAM-1蛋白的特点,这不仅使其具有大量处理过的特异性TAA,也使其能够实现有效的淋巴结归巢。研究发现,小型DCNV(CSD)纳米疫苗的归巢能力优于成熟的DC。
(2)实验结果表明,DCNV(CSD)纳米疫苗可以诱导产生强效的特异性CD8+ T细胞的强烈反应,以实现抗肿瘤免疫治疗,进而能够在高侵袭性胶质母细胞瘤和高转移性黑色素瘤模型中表现出显著的治疗效果。此外,DCNV(CSD)纳米疫苗也可在小鼠脾脏中产生记忆性T细胞(TEM),从而能够有效预防肿瘤的治疗后复发。综上所述,该工作设计了一种利用CS NPs制备高性能DC纳米疫苗以用于肿瘤免疫治疗的通用方法。
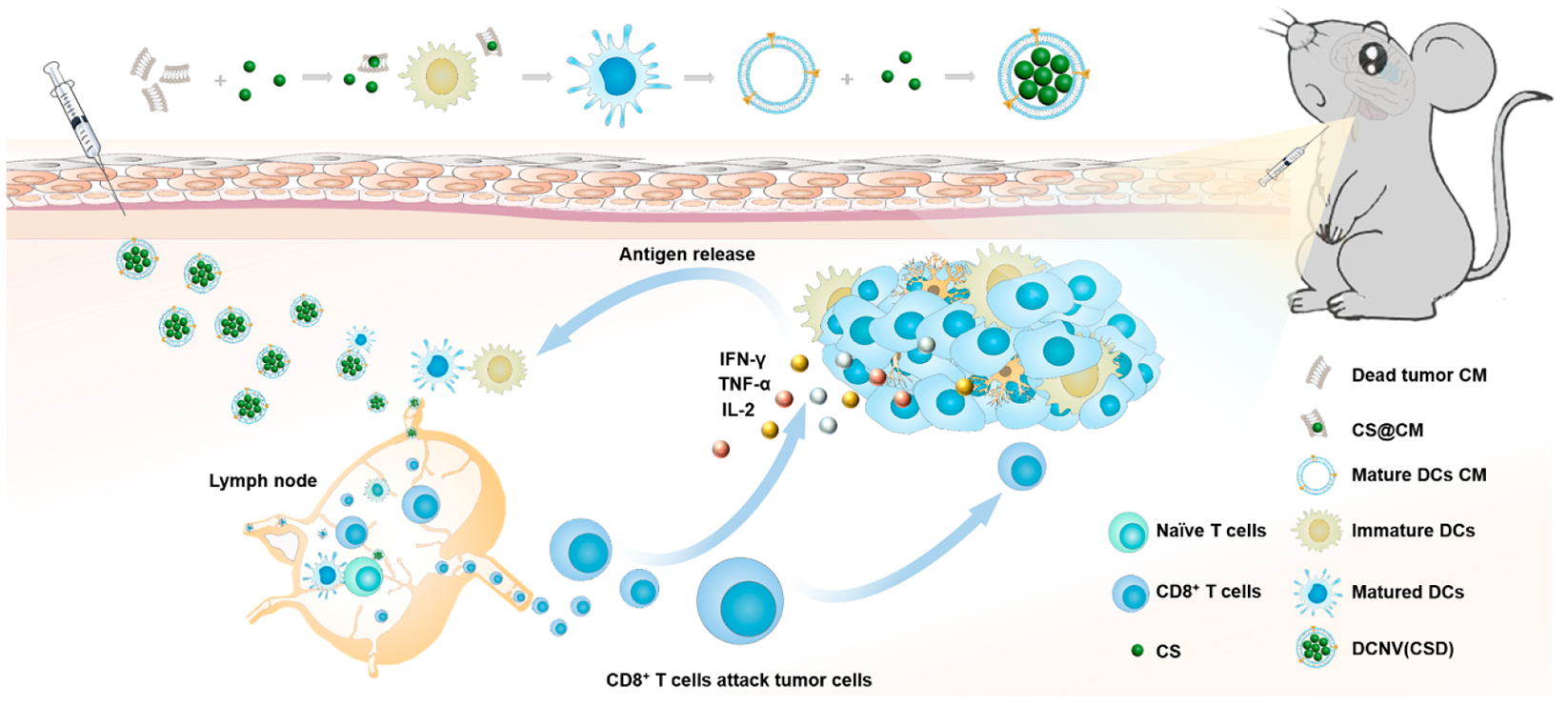
Tingting Wang. et al. Antigen Self-Presented Personalized Nanovaccines Boost the Immunotherapy of Highly Invasive and Metastatic Tumors. ACS Nano. 2024
DOI: 10.1021/acsnano.3c11189
https://pubs.acs.org/doi/10.1021/acsnano.3c11189



















