用于铁死亡治疗的抗癌纳米药物通常依赖于芬顿催化剂的直接递送,以驱动癌细胞的脂质过氧化。然而,细胞内抗铁死亡信号引起的铁死亡抗性仍会严重限制铁死亡的治疗效果。有鉴于此,中国科学院长春应化所曲晓刚研究员和任劲松研究员构建了模拟ATP酶活性的碳化钒MXene纳米酶(PVCMs),其能够通过药理学方式调节核因子e2相关因子2 (Nrf2)程序。Nrf2程序是三阴性乳腺癌(TNBC)细胞的铁死亡防御系统中的主要抗铁死亡介质。
本文要点:
(1)PVCMs具有较高的类ATP酶活性,可以有效地选择性催化ATP发生去磷酸化,以产生ADP。
(2)实验结果表明,PVCMs可通过由能量状态下降启动的级联机制有效地阻碍Nrf2程序,从而响应PVCMs诱导的谷胱甘肽耗竭以选择性地驱动三阴性乳腺癌细胞发生铁死亡。综上所述,该研究能够为利用具有药理活性的纳米酶调节特定的细胞信号和产生治疗所需的药理活性提供一个新的范例。
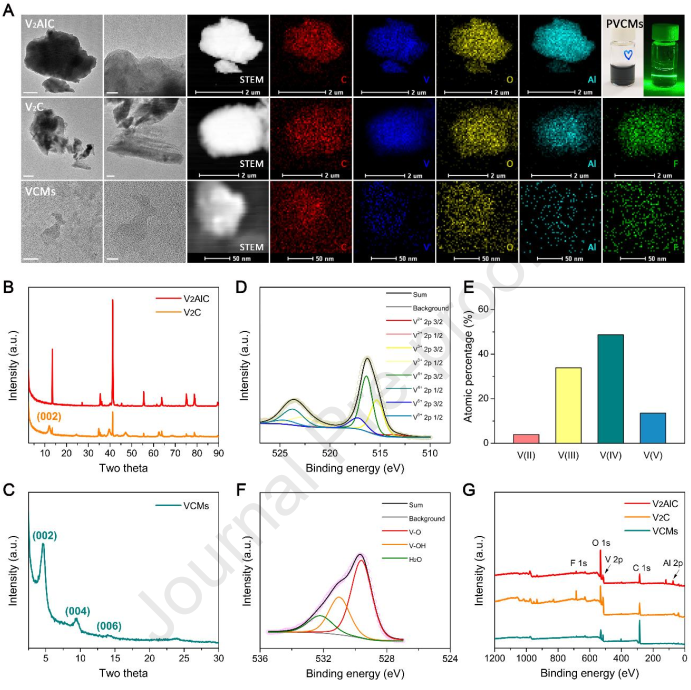
Huan Wang. et al. An ATPase-Mimicking MXene nanozyme pharmacologically breaks the ironclad defense system for ferroptosis cancer therapy. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S0142961224000577



















