NanoLabs编辑部对2019年国内外重要科研团队的代表性重要成果进行了梳理,今天,我们要介绍的是国家纳米科学中心梁兴杰研究员。

梁兴杰课题组致力于研究如何发展生物材料,利用纳米技术提高小分子化合物和生物大分子生物利用度的分子和细胞生物学机制,并探索新型纳米结构促进重大恶性疾病的药物疗效和临床治疗的方法。
课题组正在探寻通过提高药物分子的输运效率来达到显著改善治疗效果或者预防癌症和艾滋病的纳米生物技术,利用生物响应型纳米材料在细胞和组织水平提高药物安全性和治疗效果。
目前实验室主要研究内容如下:
1、纳米生物材料
2、纳米生物技术
3、聚合物纳米颗粒
4、纳米佐剂
5、无机纳米颗粒
6、纳米技术逆转肿瘤细胞耐药性
7、纳米技术用于发展新型纳米药物
下面,我们简要总结了梁兴杰研究员课题组2019年部分研究成果,供大家交流学习。
1)由于相关论文数量较多,本文仅限于通讯作者文章(不包括序言、短篇评述等),以online时间为准。
2)由于学术有限,所选文章及其表述如有不当,敬请批评指正。
3)由于篇幅限制,部分成果未列入编号,仅以发表截图展示。
以下分为四个方面展开:
Part Ⅰ 纳米药物肿瘤治疗与成像
Part Ⅱ 纳米免疫治疗
Part Ⅲ 纳米抗菌应用
Part Ⅳ 其他
Part Ⅰ 纳米药物肿瘤治疗与成像
1. Nature Nanotech.:碳点分散金原子用于治疗癌症
线粒体氧化还原稳态是活性氧和抗氧化剂(如谷胱甘肽)之间的平衡,在许多生物过程(包括生物合成和细胞凋亡)中起着关键作用,因此是癌症治疗的一个潜在靶点。于此,国家纳米中心的梁兴杰研究员与清华大学化学系的李景虹教授合作报道了一种线粒体氧化应激放大器,MitoCAT-g,它由碳点支撑的原子分散金(CAT-g)和表面修饰的三苯膦和肉桂醛组成。
研究结果发现,MitoCAT-g颗粒能特异性靶向线粒体并通过原子经济性消耗线粒体谷胱甘肽,从而放大了由肉桂醛引起的活性氧损伤,并最终导致癌细胞凋亡。结果显示,影像引导介入注射这些颗粒能有效地抑制皮下和原位模型中的肿瘤生长,而没有不良影响。研究表明,MitoCAT-g可放大线粒体中的氧化应激并抑制体内肿瘤的生长,代表了应用与抗癌的一种有前景的药物。
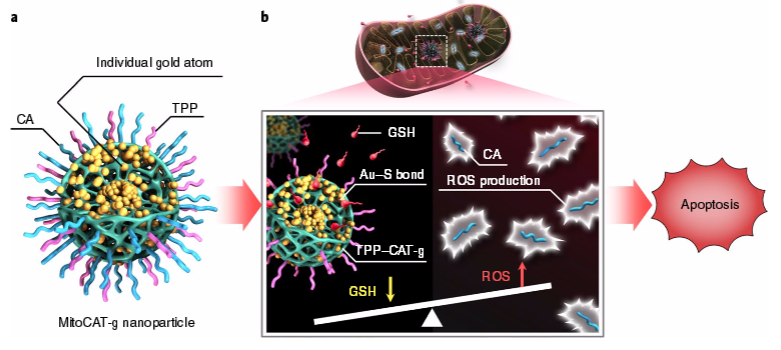
Xingjie Liang et al. Carbon-dot-supported atomically dispersed gold as a mitochondrial oxidative stress amplifier for cancer treatment. Nature Nanotechnology. 2019.
https://doi.org/10.1038/s41565-019-0373-6
2. Science Advances:向阳花一样的多级次纳米药物!
为了增强和控制基于基因干扰的治疗方法而开发有效的基因药物递送系统仍面临巨大挑战。然而,随着纳米技术的蓬勃发展,纳米载体为核酸输送提供了更有效的策略。因此,国家纳米中心梁兴杰研究员课题组开发一种由寡核苷酸序列形成的三链体及其互补链用来介导自组装的超小金纳米颗粒。
向日葵状纳米结构具有较强的近红外(NIR)吸收和光热转化能力。在近红外光照射下下,大尺寸的纳米结构可分解并生成由c-myc癌基因沉默序列修饰的超小纳米颗粒,该序列可直接靶向细胞核。此外,可通过与自组装纳米结构在体内体外的预孵育时间和近红外照射时间点协同来实现基因沉默控制的效果。这项研究为构建用于基因干扰应用的更有效和可定制的纳米载体提供了一种新方法。
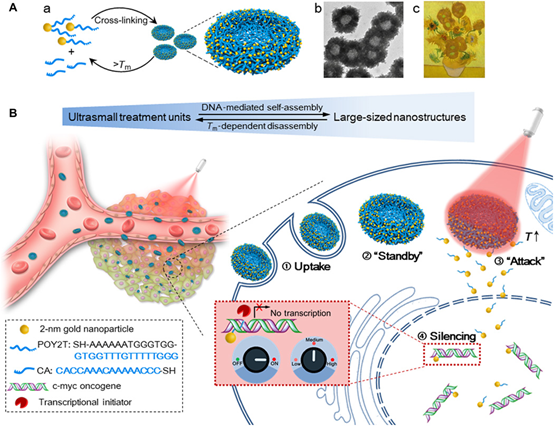
Huo, S.; Gong, N.; Jiang, Y.; Chen, F.; Guo, H.; Gan, Y.; Wang, Z.; Herrmann, A.; Liang, X.-J., Gold-DNA nanosunflowers for efficient gene silencing with controllable transformation. Science Advances 2019, 5 (10), eaaw6264.
https://advances.sciencemag.org/content/5/10/eaaw6264
3. Adv. Sci.:纳米催化自给O2和H2O2以增强化学/化学动力学联合疗法
化学/化学动力学联合疗法是提高抗癌效率的一个非常有前景的策略。但是,大多数实体瘤中的低氧和少量H2O2的微环境严重限制了该治疗方式的疗效。于此,河北大学张金超教授和李振华副教授课题组联合国家纳米中心梁兴杰研究员通过自下而上的方法构建纳米催化药物CaO2 @DOX@ZIF-67。
CaO2 @DOX@ZIF-67可以同时提供O2和H2O2,以提高化学/化学动力疗法。 在肿瘤内的弱酸性环境中,CaO2 @DOX@ZIF-67被分解以快速释放类Fenton催化剂Co2+和化学治疗药物阿霉素(DOX)。未保护的CaO2与H2O反应生成O2和H2O2。产生的O2可缓解肿瘤中的缺氧,并进一步提高DOX的疗效。与此同时,生成的H2O2通过类Fenton反应与Co2+离子反应生成剧毒的•OH,从而提高了化学动力学治疗。
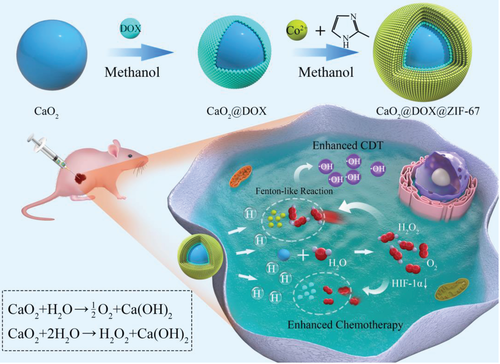
Gao, S., Jin, Y., Ge, K., Li, Z., Liu, H., Dai, X., Zhang, Y., Chen, S., Liang, X., Zhang, J., Self‐Supply of O2 and H2O2 by a Nanocatalytic Medicine to Enhance Combined Chemo/Chemodynamic Therapy. Adv. Sci.2019, 1902137.
https://onlinelibrary.wiley.com/doi/10.1002/advs.201902137
4. Adv. Sci.:酸触发金纳米粒子聚集用于增强的放疗增敏和成像
放射增敏剂用于增强肿瘤的放射治疗效果具有非常好的作用。中国医学科学院放射医学研究所刘鉴峰研究员联合国家纳米中心梁兴杰研究员提出了一种由酸引发的金纳米颗粒(GNPs)在肿瘤内聚集的策略,并将其作为放射增敏剂用于增强肿瘤的放疗效果。
具有酸诱导聚集的GNPs可以增强GNPs在癌细胞和肿瘤中的积累和保留。体内抗肿瘤实验结果表明,GNPs也提高了MCF-7异种移植肿瘤对放疗的敏感性。此外,GNPs的聚集也可以改善了GNPs在体内光声成像的效果。这项研究提供了一种新的策略来实现纳米颗粒的聚合,以提高纳米系统在体内的成像和治疗效果。
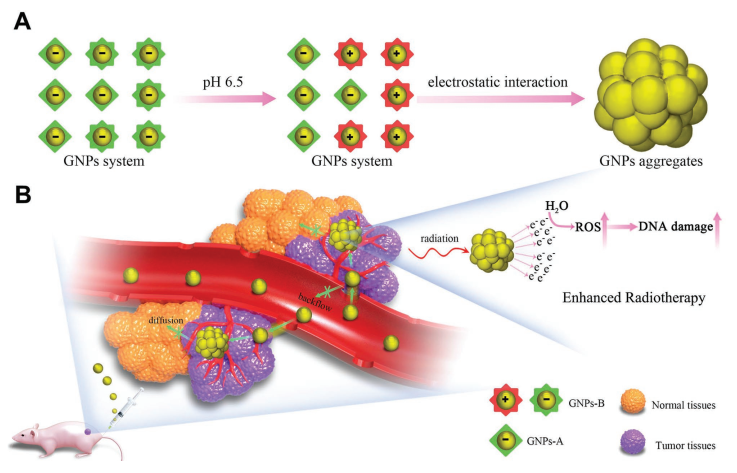
Zhang Y M, Huang F, etal. Enhanced Radiosensitization by Gold Nanoparticles with acid-Triggered Aggregation in Cancer Radiotherapy[J]. Advanced Science, 2019.
https://doi.org/10.1002/advs.201801806
5. Adv. Sci.:透明质酸纳米颗粒用于靶向治疗癌症
靶向药物递送系统(TDDSs)可以实现特异性地肿瘤靶向和药物释放,为克服传统化疗的副作用提供了一种很好的方法。透明质酸(HA)作为一种可选择性靶向CD44的药物,在TDDSs研究中得到了广泛的应用。然而,不同分子量的HA对CD44具有不同的结合能力,这也会产生不同的治疗效果。大连理工大学樊江莉团队和国家纳米科学中心梁兴杰团队合作制备了一种负载了阿霉素(DOX)的二氧化硅/羟基磷灰石(MSNs/HAP)杂化材料(DOX@MSNs/HAP)。
随后将HA和低聚HA(oHA)分别包覆在杂化材料上构建了HA-DOX@MSNs/HAP和oHA-DOX@MSNs/HAP,并研究了它们各自的肿瘤靶向性。结果发现由于oHA对于靶向CD44更加有效,oHA-DOX@MSNs/HAP在肿瘤内具有更高的细胞吸收和药物释放效率,因此其抗癌作用也有显著增强,荷瘤小鼠模型实验也同样证明了这一点。因此,该研究也为今后设计靶向肿瘤的化疗纳米药物递送系统提供了新的思路。
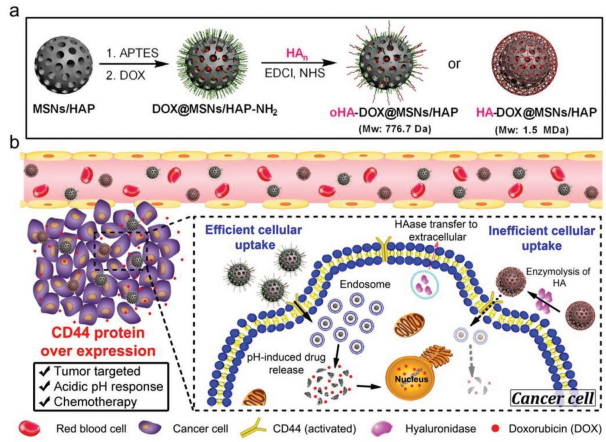
Yao Kang, Jiangli Fan, XingJie Liang, Xiaojun Peng. et al. Oligo Hyaluronan-Coated Silica/Hydroxyapatite Degradable Nanoparticles for Targeted Cancer Treatment. Advanced Science. 2019
https://doi.org/10.1002/advs.201900716
6. Nano Lett.:磁性铁氧纳米材料用于MRI/MPI和磁热治疗
磁热治疗所面临的两个主要难题是定量评估给药期间和给药后的药物分布以及在不损伤周围组织的情况下实现肿瘤的均匀热疗。中科院自动化研究所田捷团队和国家纳米科学中心梁兴杰团队合作开发了一种具有活性生物靶向作用的多模态MRI/MPI诊疗系统用于进行改善的磁热治疗(MHT)。
该系统具有增强的磁共振成像(MRI)和磁粒子成像(MPI)效应,并且研究发现18纳米的氧化铁NPs (IOs)可以作为一种高性能的体外MRI / MPI造影剂。为了提高其递送的均匀性,实验使用肿瘤靶向肽CREKA对18纳米IOs进行修饰使其可以靶向肿瘤。MRI/MPI结果显示,靶向剂可以显著改善纳米颗粒在4T1原位小鼠乳腺癌肿瘤中的递送均匀性。治疗结果显示,通过提高靶向性和递送均匀性可以使得该系统比其他非靶向的IOs具有更好的肿瘤磁热治疗效率。
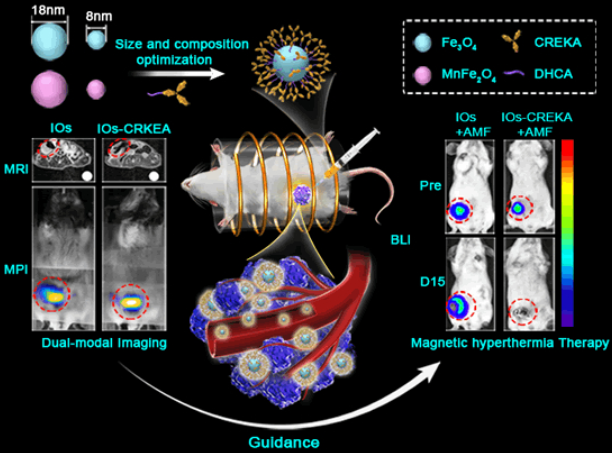
Yang Du, Xiaoli Liu, Qian Liang, Xing-Jie Liang, Jie Tian. Optimization and Design of Magnetic Ferrite Nanoparticles with Uniform Tumor Distribution for Highly Sensitive MRI/MPI Performance and Improved Magnetic Hyperthermia Therapy. Nano Letters. 2019
https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.nanolett.9b00630
另外:

Part Ⅱ 纳米免疫疗法
7. ACS Nano: 铁磁涡旋纳米环介导的微磁热疗对抗肿瘤转移
癌症转移是导致其治疗失败的一个主要原因。中科院自动化研究所杜洋博士、田捷研究员、西北大学樊海明教授和国家纳米科学中心梁兴杰研究员合作报告了一种有效安全的纳米治疗策略,可以根除原发性肿瘤,并抑制其肺部转移,进而控制远处肿瘤的转移和生长。
该铁磁涡旋氧化铁纳米环(FVIO)介导的轻度磁热疗会导致4T1乳腺癌细胞钙网蛋白(CRT)的表达。而CRT的表达会传递“吃我”的信号,进而促进免疫系统对癌细胞的吞噬吸收,诱导有效的免疫原性细胞死亡,并进一步导致巨噬细胞极化。这种温和的热疗法可以有效增强远处肿瘤的CD8+细胞毒性T淋巴细胞的浸润,并有效地使肿瘤对PD-L1检查点阻断治疗敏感而触发免疫治疗。而在与PD-L1阻断治疗进行结合后,CD8+细胞毒性T淋巴细胞的比例可进一步从55.4%提高到64.5%。此外,该联合治疗也可抑制肿瘤的免疫抑制反应,使得骨髓源性抑制细胞(MDSCs)显著下调。这一研究结果表明,FVIO介导的温和磁热疗法可以激活宿主免疫系统,并可通过与PD-L1阻断试剂的有效合作以抑制远处肿瘤的转移扩散和生长。

Xiaoli Liu, Yang Du, Haiming Fan, Jie Tian, Xing-Jie Liang. et al. Ferrimagnetic Vortex Nanoring-Mediated Mild magnetic Hyperthermia Imparts Potent Immunological Effect for Treating Cancer Metastasis. ACS Nano. 2019
https://pubs.acs.org/doi/10.1021/acsnano.9b01979
8. Biomaterials:纳米药物和纳米疫苗的共定位递送用于术后癌症免疫治疗
实体瘤的免疫治疗受到肿瘤免疫原性差和T细胞免疫应答受限的限制,导致患者应答率低。为了提高肿瘤免疫治疗的效率,中国医学科学院王伟伟研究团队联合天津大学董岸杰研究团队及国家纳米科学中心梁兴杰研究团队开发了一种独特的协同联合肿瘤免疫治疗方法,通过共定位递送肿瘤纳米药物(增强肿瘤免疫原性)和纳米疫苗(增强T细胞免疫力)用于术后肿瘤治疗。其中,热响应、负载姜黄素的聚合物纳米颗粒(纳米药物)组装的水凝胶能够完全覆盖原发性肿瘤的手术床,并在时空上传递同源纳米药物和封装的纳米疫苗。
更重要的是,纳米药物有效地诱导了残余癌细胞的免疫原性死亡(ICD),从而增强了肿瘤的免疫原性,并使肿瘤对抗肿瘤T细胞免疫敏感。该肿瘤纳米疫苗由抗原肽、CpG-ODN和阳离子聚合物纳米颗粒组成,能显著触发树突状细胞(DCs)的成熟,并能引起强效的疫苗特异性T细胞免疫反应。采用高度恶性的术后乳腺癌4T1模型,发现联合免疫治疗策略显著增强了全身宿主T细胞免疫水平,促进了肿瘤内CD8+ T淋巴细胞的浸润,从而有效减弱了肿瘤局部复发和肺转移。总的来说,这项工作为术后肿瘤免疫治疗提供了一种先进的协同联合疗法。这种自组装水凝胶能够实现免疫调节纳米药物和疫苗的广泛结合用于癌症免疫治疗。
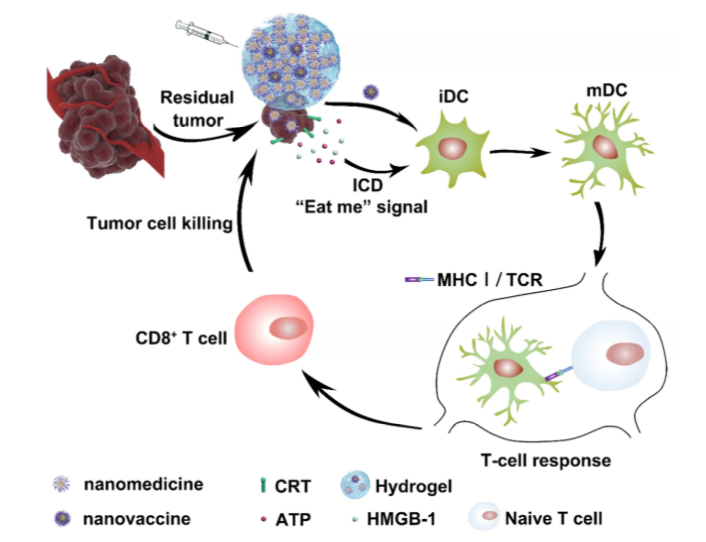
Xiang Liu, Zujian Feng, Changrong Wang, et al. Co-localized delivery of nanomedicine and nanovaccine augments the postoperative cancer immunotherapy by amplifying T-cell responses. Biomaterials, 2019.
https://doi.org/10.1016/j.biomaterials.2019.119649
Part Ⅲ 纳米抗菌应用
9. Nature Commun.:热响应三功能纳米转运体用于治疗多药耐药细菌感染
据世界卫生组织统计,近80%多药耐药(MDR)或极度耐药(XDR)微生物的出现是由于全球过度使用或滥用抗生素而导致的,这些菌株的感染伴随有严重的副作用,如血栓性静脉炎或表皮坏死松解,因此,迫切需要开发一种对多药耐药菌具有高抗菌作用的新策略。近日,国家纳米科学中心梁兴杰研究团队联合重庆大学罗阳研究团队设计了一种巧妙的三功能纳米结构,即TRIDENT(热响应应激药物输送纳米转运体),用于可靠的细菌根除。其强大的抗菌效果归功于将荧光检测与协同化学光热灭活相整合。
其中,近红外辐射产生的升温不仅通过相变机制熔化了纳米转运体,而且不可逆转地破坏了细菌膜以促进亚胺培南的渗透,从而干扰细胞壁生物合成,最终导致细菌快速死亡。体内和体外实验都表明,即使是封装了低剂量的亚胺培南TRIDENT也能根除临床耐甲氧西林金黄色葡萄球菌,而单用亚胺培南的效果是有限的。由于受感染部位的迅速恢复和良好的生物相容性,此抗菌策略可用于对抗多药耐药或极端耐药细菌。
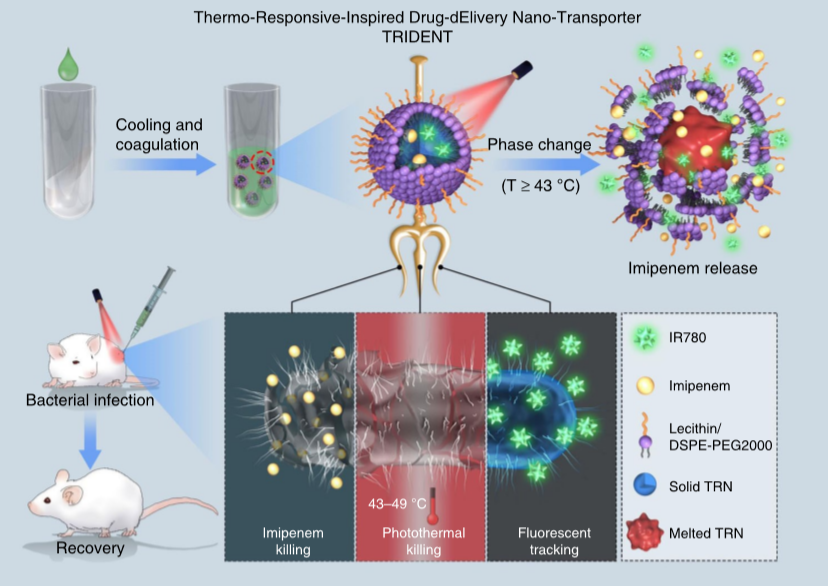
Qing, G., Zhao, X., Gong, N. et al. Thermo-responsive triple-function nanotransporter for efficient chemo-photothermal therapy of multidrug-resistant bacterial infection. Nat Commun 10, 4336 (2019)
https://doi.org/10.1038/s41467-019-12313-3
10. ACS Nano:天然中药纳米结构用于抗菌
传统抗生素的滥用导致了一系列的健康问题,包括抗生素耐药性,严重威胁着人类的健康。因此,寻找广泛的抗菌药物来源和开发多维策略来对抗细菌感染是当务之急。有鉴于此,北京中医药大学雷海民研究员、王鹏龙副教授联合国家纳米中心梁兴杰研究员报道了黄连素(Berberine, BBR)与黄酮苷类化合物(flavonoid glycosides)之间的两种天然自组装模式:纳米颗粒(NPs)和纳米纤维(NFs),它们都主要受静电和疏水作用的控制。
这两种纳米结构具有不同于BBR的抗菌性能。NPs的抑菌活性明显增强,而NFs的抑菌效果远弱于BBR。如此不同的区别可归因于NPs和NFs的不同空间构型和自组装过程。黄酮苷和BBR首先形成一维复合单元,然后自组装成三维纳米结构。随着亲水性葡萄糖醛酸的不断向外迁移,NPs对细菌具有较强的亲和力,从而导致细菌种群的分散和生物膜的减少。此外,体外溶血试验、细胞毒性试验和斑马鱼体内毒性评价表明,所获得的自组装体具有良好的生物相容性。这种超分子自组装策略可应用于其他纳米抗菌药物的构建,从而为细菌感染治疗中自递送药物的开发提供了武器。
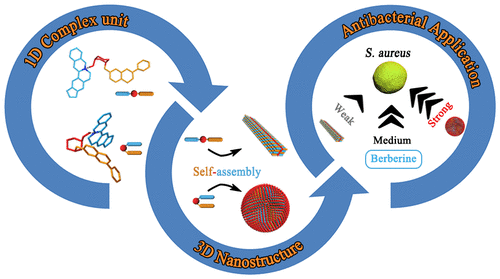
Tong Li, Penglong Wang, Xing-Jie Liang, Haimin Lei, et al. Natural Berberine-Based Chinese Herb Medicine Assembled Nanostructures with Modified Antibacterial Application. ACS Nano 2019 13 (6), 6770-6781
https://doi.org/10.1021/acsnano.9b01346
Part Ⅳ 其他
11. ACS Nano:纳米药物介导递送甲氨蝶呤用于治疗类风湿性关节炎
类风湿关节炎(RA)是最常见的慢性自身免疫性疾病之一。尽管目前对RA的临床治疗取得了相当大的进展,但也存在诸多尚未解决的挑战。罗马第二大学Massimo Bottini团队、国家纳米科学中心梁兴杰团队和广州医科大学郭伟圣团队合作发现RA患者和胶原诱导关节炎(CIA)小鼠的滑膜液和滑膜中均有过表达的SPARC,它会分泌酸性蛋白并且富含半胱氨酸。
基于RA微环境中的SPARC特征和SPARC对白蛋白的高亲和力,实验制备了负载甲氨蝶呤的人血清白蛋白纳米药物(MTX@HSA NMs),并将其作为治疗RA的仿生药物递送系统。在向CIA小鼠静脉注射Ce6标记的MTX@HSA NMs后,荧光/磁共振双模态成像结果表明,相对于游离的MTX分子来说,炎症关节中MTX@HSA NMs的累积量更高,保留时间也更长。体内治疗结果表明,MTX@ HSA NMs能够有效减轻RA,即使剂量减半也比游离的MTX有着更好的疗效和更少的副作用。这一研究通过揭示MTX@ HSA NMs在RA内高效积累的机制,证明其具有提高MTX安全性和治疗效果的能力,也将为开发具有临床转化潜力的创新型抗RA纳米药物提供了新的方向。
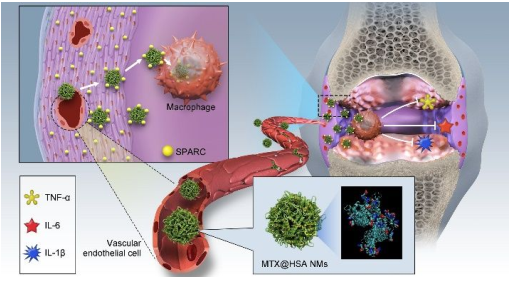
Lu Liu, Massimo Bottini, Weisheng Guo, Xing-Jie Liang. et al. Secreted Protein Acidic and Rich in Cysteine Mediated Biomimetic Delivery of Methotrexate by Albumin-Based Nanomedicines for Rheumatoid Arthritis Therapy. ACS Nano. 2019
https://pubs.acs.org.ccindex.cn/doi/10.1021/acsnano.9b01710
12. Nano Lett:Au NPs尺寸通过破裂高尔基体而对细胞粘附的影响
与纳米材料的蓬勃生产和应用相比,纳米颗粒的毒理学影响及其对组织和器官可能的危害的研究仍处于起步阶段。高尔基体是细胞中最重要的细胞器之一,在细胞内蛋白质加工中起关键作用。高尔基体的结构完整性对其正常功能至关重要,高尔基体紊乱可能导致多种疾病和失调。
在这项研究中,国家纳米中心梁兴杰研究员与河北大学张金超教授等人首次发现金纳米颗粒(Au NPs)诱导了大小依赖性的细胞质钙增加和高尔基体碎裂,这阻碍了正常的高尔基体功能,导致异常的蛋白质加工,并导致细胞黏附力降低,而细胞活力却没有严重受损。另外,在体内诱导了早期的肾脏病理变化。这项工作对纳米颗粒研究具有重要意义,因为它说明了尺寸对金纳米颗粒诱导的高尔基体形态变化及其在体内外的影响的重要作用,这对纳米材料的生物学应用具有重要意义。
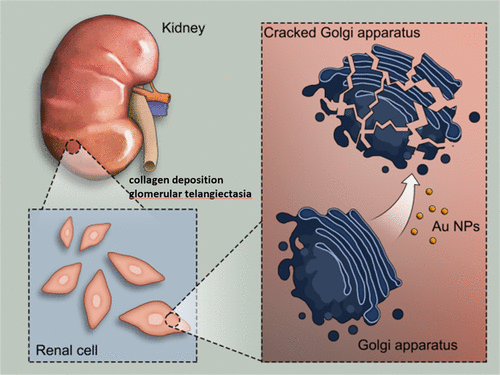
Xiaowei Ma, Jinchao Zhang, and Xing-Jie Liang, et al. Evaluation of Turning-Sized Gold Nanoparticles on Cellular Adhesion by Golgi Disruption in Vitro and in Vivo. Nano Letters 2019.
https://doi.org/10.1021/acs.nanolett.9b02826
梁兴杰研究员简介

梁兴杰,国家纳米科学中心研究员,享受国务院特殊津贴,国家杰青,科技部中青年科技创新领军人才,中国科学院大学-教育部“长江学者”特聘教授。
目前主要从事纳米结构的生物学效应,以及设计构建纳米药物研究其克服临床适用性耐受的作用机制。已在Nature Nanotechnology, PNAS,Cancer Research,ACS Nano, Advanced Materials,Biomaterials等国际重要学术期刊发表论文290余篇,文章引用率超13000次, H-index > 62。现担任《Current Drug Delivery》主编,《Biophysics Reports》和《Biomaterials》副主编,《ACS Nano》、《AdvancedTherapeutics》等杂志顾问委员会编委和编委。
(注:以上简介及文中海报整理自网络及梁兴杰研究员课题组网站)











