通过哈伯-博施(HB)工艺将氮(N2)和氢(H2)合成为氨(NH3)气体在粮食生产和其他化工生产过程中起着至关重要的作用。但是,HB工艺需要大量的能源消耗(占世界能源产量的2%),同时高压和高温的条件使生产NH3的设备非常昂贵。合成氨的研究,特别是在低温低压下的合成氨,一直是化学家们关注的焦点。近日来,国内外多个课题组在电催化以及热催化合成氨相关方向取得了许多进展。这些针对新材料设计和深入机理研究相关工作使得新一代绿色低能耗的合成氨过程变得越来越有希望。
1. JACS: 硅掺杂的铁催化剂用于低温低压下合成氨
近日,美国内华达大学里诺分校Qi An,加州理工学院William A. Goddard III,Alessandro Fortunelli等基于最近报道的完整反应机制开发了一种多级高通量催化剂筛选(HHTCS)方法,加快高效HB催化剂的开发。
本文要点:
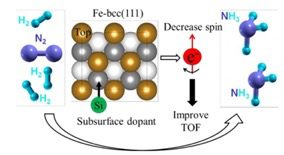
1)作者利用HHTCS方法,从18种非过渡金属(NTM)候选元素中识别出了可以通过表面和次表面掺杂显著提高Fe-bcc(111)(活性最高的Fe晶面)的催化合成氨效率的元素。出乎意料的是,作者筛选出了一种之前未被发现或提出的次表面掺杂剂Si,这同时也表明了次表面Fe原子在N2还原反应中的重要性。
2)作者利用QM模拟中得出了Si掺杂的Fe-bcc(111)的HB过程的完整反应路径,并与动力学Monte Carlo(kMC)模拟相结合来预测TOF,发现在典型的极端HB条件(反应物压力为200 atm,500°C),Si掺杂的Fe-bcc(111)催化剂比纯铁催化剂TOF增加约13倍;在理想HB条件(反应物压力为20 atm,400°C)的条件下,TOF增加约43倍。
3)此外,Si掺杂的Fe催化剂可以在更温和的条件下例如,在500°C时,反应物压力降低至20 atm,或者在温度降至400°C,反应物降至50 atm,达到200 atm/500°C下纯Fe的相同的TOF。
Qi An, et al. Si-doped Fe Catalyst for Ammonia Synthesis at Dramatically Decreased Pressures and Temperatures. J. Am. Chem. Soc. 2020,
DOI: 10.1021/jacs.9b13996
https://doi.org/10.1021/jacs.9b13996
2. JACS:应变钌纳米团簇催化剂用于低温电还原生成氨
Haber-Bosch反应的局限性(特别是高温操作)引发了人们对低温氨合成的新兴趣。N2电还原是一种很有吸引力的替代方法,但由于产氨速率低(大多<10 mmol gcat-1 h-1)、局部电流密度小(<1 mA cm-2)和高选择性的析氢副反应而难以大规模实际应用。
有鉴于此,香港中文大学的Jimmy C. Yu和华中师范大学张礼知教授等人,设计制备了一种应变钌纳米团簇催化剂,可以作为高效的室温电还原合成氨催化剂。
本文要点
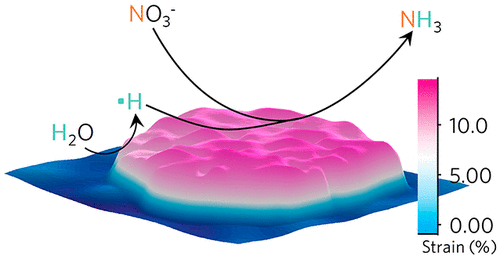
1)设计了Ru/氧掺杂Ru核/壳纳米团簇催化剂用于电催化合成氨。该催化剂催化的室温电还原生成氨具有较高的产氨速率(5.56 mol gcat-1 h-1),高于Haber-Bosch工艺。
2)氧掺杂剂会使Ru晶胞膨胀,从而触发拉伸应变。应变晶胞抑制了HER,但通过消除氢-氢偶合的势垒促进了•H的形成。氢自由基是这种高催化性能的主要贡献者,通过在较低的动力学势垒处将限速步骤的中间体加氢来加快硝酸盐向氨的转化。
3)由于稳定的表面Ru-O配位,在> 120 mA cm-2的电流密度下,应变纳米结构可以在100 h内保持近100%的氨分解选择性。而且该应变纳米团簇在广泛的应用电势下仍具有很高的选择性,并且由于Ru与次表面氧掺杂剂的牢固结合,因此在强电流下表现出了优异的耐久性。
总之,该工作设计制备了一种新型的电催化剂,有助于低温硝酸盐电还原合成氨工艺的进一步发展。
Jie Li et al. Efficient Ammonia Electrosynthesis from Nitrate on Strained Ruthenium Nanoclusters. J. Am. Chem. Soc., 2020.
DOI: 10.1021/jacs.0c00418
https://doi.org/10.1021/jacs.0c00418
3. Angew:利用废气中的一氧化氮直接电化学合成氨
一氧化氮(NO)对环境有害,因此除去废气中的NO具有重要意义。由N2电化学合成氨(EAS)具有低的反应速率和低的法拉第效率(FE)。近日,中科院大连化物所Jianping Xiao,Dehui Deng等报道了一种通过电催化利用废气中的NO合成氨的替代途径。
本文要点:
1)密度泛函理论计算表明,电化学NO还原(NORR)比N2还原(NRR)更具活性。
2)通过基于descriptor的方法,Cu由于其中等的反应活性,被筛选出是NORR生成NH3活性最高的金属催化剂。而且,动力学计算表明,相对于Cu催化剂上的H2,N2O和N2,NH3是最优选的产物。
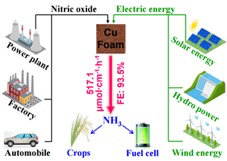
3)实验表明,使用铜泡沫电极,在0.9 V电压下(相对于RHE),EAS达到了创纪录的高达517.1μmol·cm -2·h -1的活性,FE高达93.5%,且在运行100小时后表现出稳定的电催化性能。
该工作提供了一种从废气中去除NO,并且生成NH3的策略。
Jun Long, et al. Direct Electrochemical Ammonia Synthesis from Nitric Oxide. Angew. Chem. Int. Ed. 2020,
DOI: 10.1002/anie.202002337
https://doi.org/10.1002/anie.202002337
4. Angew: 电荷积聚和自旋极化在电催化还原碳基催化剂中的重要作用
工业化固氮是人类社会历史的转折点,支撑着世界近一半人口的生计。近年来,氨作为一种新型的能源载体逐渐引起业界的关注。然而,目前的工业合成氨反应(哈珀法)需要在高温高压进行,而且集中化的合成氨工艺业不适合分布式的农业生产。因此,利用可再生能源在温和的条件下实现电化学氮气还原反应吸引了研究人员广泛的兴趣,它允许按需、现场实现氨气的生产,而原料来自于无处不在的氮气和水。低成本的碳基催化剂是催化电化学N2还原反应(NRR)的理想催化剂。然而,碳基催化剂对NRR的活性来源尚不清楚,在合理设计碳基NRR电催化剂时缺乏准确普适的机理和原则。
近日,天津大学凌涛教授等人合作,基于理论计算和实验观察的结合,系统地评估了硫氧基元素(O, S, Se, Te)掺杂的碳材料作为NRR催化剂的潜力。他们发现杂原子掺杂诱导的电荷积累效应促进了碳原子对N2的吸附,自旋极化增加了第一个质子形成*NNH的电位决定步骤。Te和Se掺杂的C催化剂表现出较高的固有NRR活性,优于大多数金属基催化剂。该工作建立了碳基材料的电子结构与NRR性能之间的关系规律,为碳基催化剂在NRR的应用奠定了基础。

Tao Ling; Yuanyuan Yang; Lifu Zhang; Zhenpeng Hu; Yao Zheng; Cheng Tang; Ping Chen; Ruguang Wang; Kangwen Qiu; Jing Mao; Shi-Zhang Qiao. The crucial role of charge accumulation and spin polarization in activating carbon‐based catalysts for electrocatalytic nitrogen reduction. Angewandte Chemie International Edition, 2020.
DOI: 10.1002/anie.201915001
https://doi.org/10.1002/anie.201915001
5. AM:采用玻璃质M-Te (M = Ru, Rh, Ir)多孔纳米棒进行高效电化学N2固定的通用策略
电化学转化氮(N2)是增值氨(NH3)的非常理想的途径之一,但由于N2分子的极端惰性,这是一个巨大的挑战,开发一个强大的电催化剂是其途径可执行的先决条件。
近日,苏州大学的黄小青等人报道了一类新型的“子弹型”多孔玻璃质纳米棒M-Te( M = Ru, Rh, Ir)作为N2还原反应的催化剂。
本文要点:
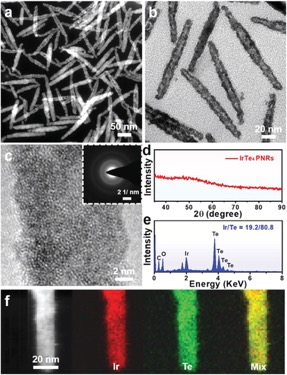
1)优化后的IrTe4 PNRs具有最高的NH3转化率(高达51.1 µgh-1 mg-1cat.)和法拉第效率(15.3%),以及长达20个连续循环的长期稳定性,是目前报道的最活跃的NRR电催化剂之一。
2)N2程序温度脱附和价带X射线光电子能谱数据均表明,N2的强化学吸附是增强NRR和抑制IrTe4 PNRs析氢反应的关键。
3)通过密度泛函理论计算,最终确定了IrTe4吸附作用中优异的吸附强度来源于富电子Ir与周围高电活性的Te原子的协同作用。在碱性介质中对N2和H2O的最佳吸附保证了连续NRR过程的优越性。
本工作为基于玻璃材料的高性能NRR电催化剂的设计开辟了新的途径。
Juan Wang, Bolong Huang, Yujin Ji, Mingzi Sun, Tong Wu, Rongguan Yin, Xing Zhu, Youyong Li, Qi Shao, and Xiaoqing Huang. A General Strategy to Glassy M-Te (M = Ru, Rh, Ir) Porous Nanorods for Efficient Electrochemical N2 Fixation. Adv. Mater. 2020.
DOI: 10.1002/adma.201907112
https://doi.org/10.1002/adma.201907112
6. Chem: 单原子突起引起的界面极化加速电催化氮还原合成氨
寻找绿色,低价位和可持续的方法合成氨对当今社会的发展至关重要。电催化氮还原合成氨是一种非常有潜力的办法。但是到目前为止,电催化剂仍然不能够有效的打开氮氮三键,从而造成了电催化合成氨反应的活性和选择性较低。
有鉴于此,华中师范大学Lizhi Zhang教授团队合成了一种新型的电催化剂:突出的单原子Fe修饰的MoS2纳米片。突出的单原子可以引起界面极化,从而大大提高电还原氮气合成氨的性能。
本文要点:
1)界面极化可以显著的提升电还原氮合成氨的效率。
2)MoS2纳米片上突起状的单原子可以触发电场,引起N2分子的计划。
3)极化场可以加速电子的注入,促进氮氮三键的打开。
4)使用此催化剂可以高效(在-0.2 V的标准电极电位下,产率高达36.1 ± 3.6 mmol g−1 h−1)和高选择性的合成氨。
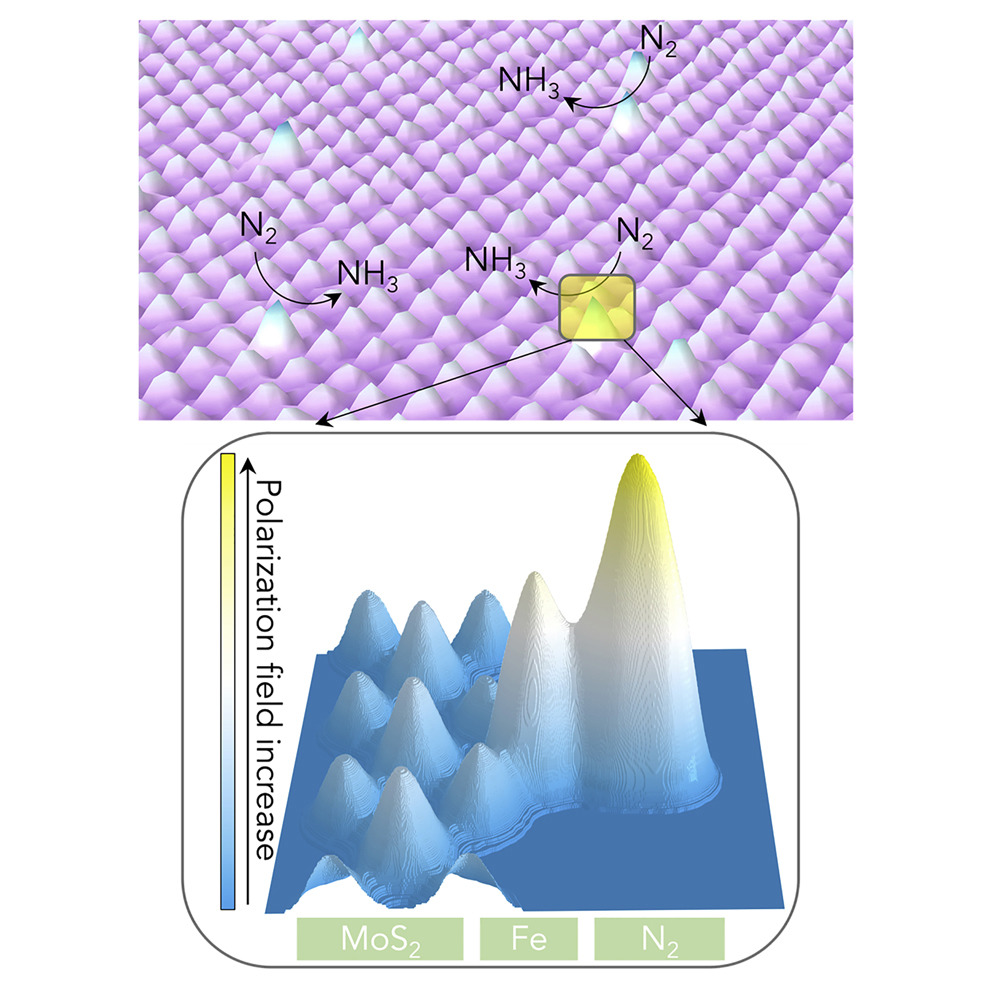
Jie Li et al. Accelerated Dinitrogen Electroreduction to Ammonia via Interfacial Polarization Triggered by Single-Atom Protrusions. Chem, 2020.
DOI: 10.1016/j.chempr.2020.01.013
https://doi.org/10.1016/j.chempr.2020.01.013
7. ACS Catal: Mo(IV)掺杂FeS2电化学还原N2
天津大学杜希文、董存库和天津师范大学杜淼等人报道了Mo(IV)掺杂FeS2电化学还原N2的工作。通过无机材料催化剂对N2进行通过电催化方法合成NH3能够实现氨化学的巨大进步。对生物固氮酶FeMo中心模拟,作者合成了Mo掺杂的FeS2。作者通过DFT计算发现Mo(IV)的掺杂有利于N2的吸附作用,FeS2基底能够抑制竞争性的分解水反应,通过这种作用Mo(IV)-FeS2催化剂在-0.2 V电压中工作实现了14.41 %的高法拉第效率。
本文要点:
(1)催化剂合成方法。Fe(NO3)3和TAA(硫代乙酰胺,thioacetamide)溶解在DMF中,加入不同量的MoCl5,90 ℃反应24 h。随后产物分散在DMF中在180 ℃中反应5 h。
(2)催化反应。通过吲哚酚蓝比色法(Indophenol blue colorimetry)测试,显示催化反应后的电极UV-Vis光谱显示在655 nm附近产生了吸收峰,说明反应中生成了大量NH3。比较峰强度,显示不同电压(-0.1~-0.5 V)下的UV-Vis中-0.2 V有最好的催化反应活性。发现反应在低于-0.5 V中,反应电流稳定。Mo(IV)-FeS2催化剂的催化反应活性显示,最高的NH3生成速率为25.15 μgh-1 mg-1。
(3)通过原位电化学FTIR红外测试对催化剂作用进行表征,发现在1230 cm-1附近的NH3红外吸收峰在催化反应过程中明显增强,与之相比未掺杂Mo的催化剂没有明显的NH3对应信号。通过密度泛函理论对催化反应过渡态和能量变化过程进行计算。优化后的催化过程显示,FeS2本征材料经过N2 → NN* → NNH* →NNH2* → N* → NH* → NH2* → NH3过程进行反应,掺杂Mo的FeS2材料经过N2 → NN* → NNH* →NNH2* → NHNH2* → NH* → NH2* → NH3过程进行反应。催化反应过程中NN* → NNH*是关键过程,通过Mo(IV)掺杂作用,这步关键催化反应的能量由1.24 eV降低为0.62 eV,对该催化反应过程更有利。
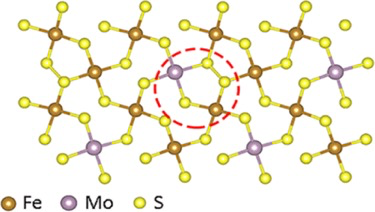
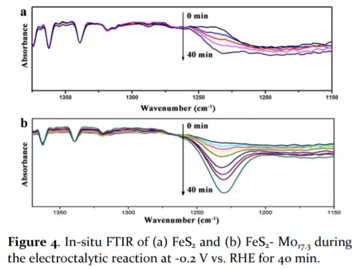
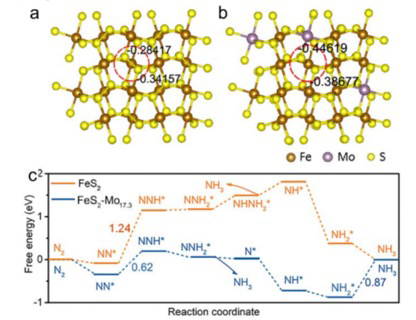
Hai-Bin Wang; Jia-Qi Wang; Rui Zhang; Chuan-Qi Cheng; Kang-Wen Qiu; Yi-jie Yang; Jing Mao; Hui Liu; Miao Du*; Cun-Ku Dong*; Xi-Wen Du*. Bionic Design of a Mo(IV)-Doped FeS2 Catalyst for Electroreduction of Dinitrogen to Ammonia,ACS Catal. 2020, 10, XXX, 4914-4921
DOI: 10.1021/acscatal.0c00271
https://pubs.acs.org/doi/abs/10.1021/acscatal.0c00271
8. Nat. Commun.: 立方CaFH固溶体催化剂50°C下高效催化N2和H2合成氨
在较低温度下(例如,50°C)催化N2和H2合成氨的高效催化剂的开发对实现零CO2排放的氨生产具有重要意义。
近日,东京工业大学Michikazu Hara, Hideo Hosono等报道合成了一种沉积有钌(Ru)纳米颗粒立方CaFH固溶体催化剂,实现了低温下(50°C)由N2和H2气体合成氨。
本文要点:
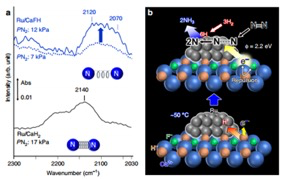
1)作者合成了一种稳定的供电子非均相催化剂,沉积有Ru纳米颗粒立方CaFH固溶体,实现了低温下氨的合成。
2)实验表明,该催化剂在50°C下由N2和H2气体合成氨,其活化能非常小,为20 kJ mol-1,比常规催化剂少一半。
3)进一步研究发现,该催化剂高的供电子能力来源于H-和F-空位之间的强电子排斥力,这极大地增强了电子穿过Ru的3d轨道向N2分子的π*轨道的提供电子的能力。此外,该催化剂高的性能可归因于固溶体中Ca2+和H-离子之间的弱离子键以及氢原子从H-位点的轻易释放。
Masashi Hattori, et al. Solid solution for catalytic ammonia synthesis from nitrogen and hydrogen gases at 50°C. Nat. Commun. 2020,
DOI: 10.1038/s41467-020-15868-8
https://www.nature.com/articles/s41467-020-15868-8
9. 李玉良院士/黄勃龙等Angew.: 石墨炔界面工程:高活性和选择性氨合成的新纪录
合成氨的出现为世界上数十亿人提供了食物。因此,合成氨的研究,特别是在室温和常压下的合成氨,一直是化学家们关注的焦点。在环境条件下将氮电还原为无碳氨是一种有望替代在工业上广泛使用的高耗能HaberBosch工艺的方法。电催化合成氨工艺中最关键的一步是高选择性和高效催化剂的合成。3d-过渡金属(TM)是一种高效的氮还原催化剂。然而,目前对三维过渡金属材料作为高效ECNRR催化剂的研究还没有引起广泛关注。而且已报道的ECNRR电催化剂的催化性能(如YNH3和FE)仍然很低,应用潜力非常低。均相催化剂被认为在环境条件下具有很大的选择性NRR潜力,但其稳定性和产率较低,不适合高效电催化。另一方面,多相催化剂在环境条件下对ECNRR具有较高的稳定性,且易配备能量转换装置,但面临ECNRR与析氢反应(HER)之间的竞争,造成严重的选择性损失。目前尚未发现具有高选择性、高效率、高YNH3和高稳定性的催化剂。将金属催化剂与碳材料结合形成的界面已被认为是提高催化性能的重要途径。石墨炔(GDY),一个新颖的二维碳同素异形体,具有独特的多孔结构,不均匀分布的表面电荷,(电)化学稳定性和高电导率,在催化,能量转换和存储方面的广泛应用受到越来越多的关注。值得注意的是,GDY可以在任意基底上生长,可以通过界面工程改善电荷转移并且增加活性位点数量,从而有望显着增强整体催化活性和稳定性。
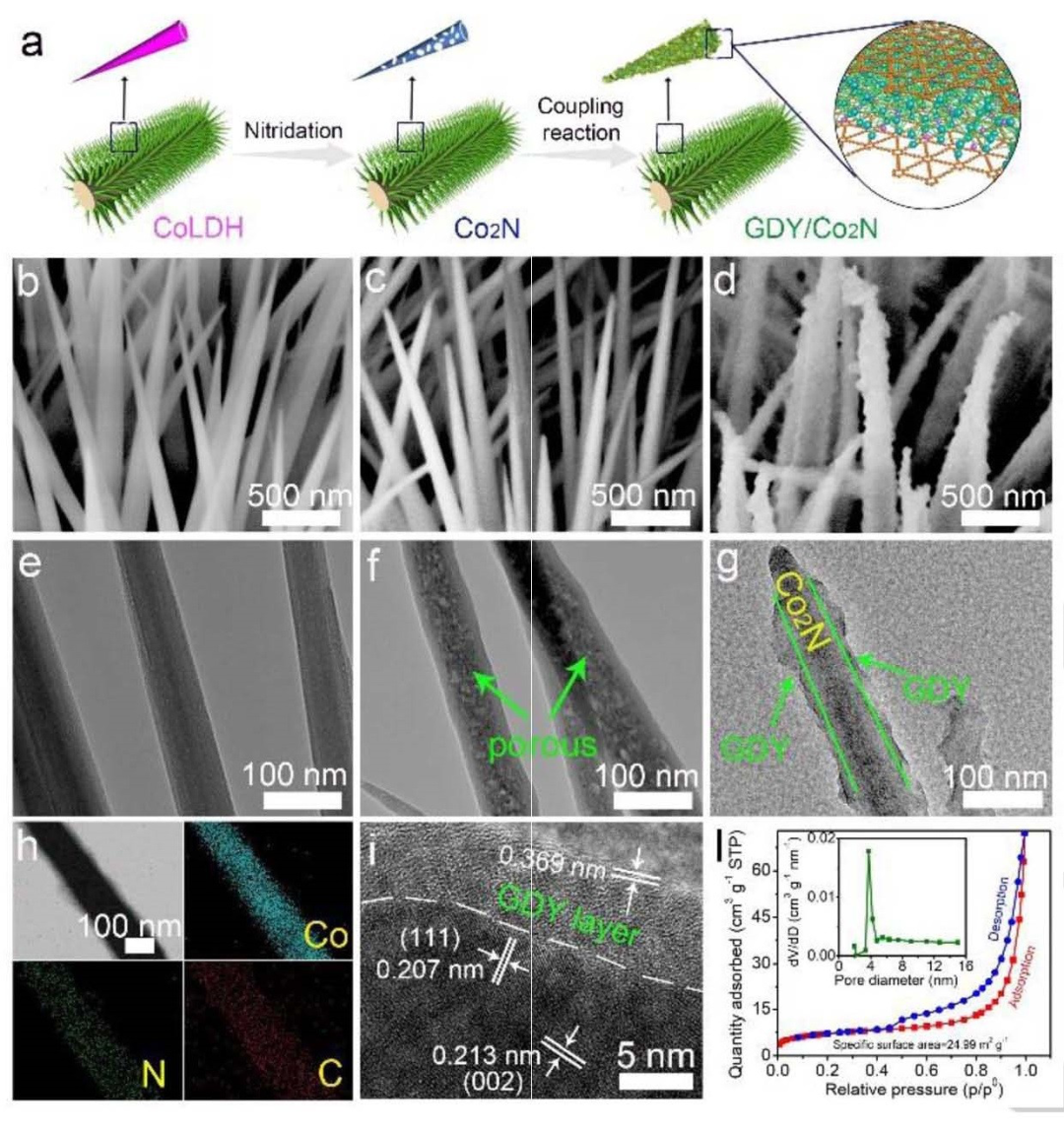
有鉴于此,中科院化学部的李玉良院士、Yongjun Li和Yurui Xue以及香港理工大学的黄勃龙教授等人,设计制备了一种具有高活性和选择性界面的自支撑3D石墨炔-钴氮化物(GDY/Co2N) 阴极,用于电化学氮还原反应(ECNRR)。
本文要点
1)3D自支撑GDY/Co2N阴极在酸性和中性条件下于环境压力和室温下对NH3合成具有很高的选择性和效率。实验上,在大气压和室温下,电催化剂在酸性条件下创造了219.72 μgh-1mgcat-1的氨产率(Y NH3)和58.60%的法拉第效率(FE)的新记录,高于已报道的其他电催化剂。
2)此外,这种优异的催化性能可分别在酸性和中性条件下维持114和144小时以上,表现出优异的催化稳定性。
3)密度函数理论(DFT)计算表明,界面键合的GDY提供了一个独特的p电子特性来优化Co‐N复合表面键合,从而在界面区域产生了NRR催化的优越电子活性,从d到pσ*态跃迁的反常减小将固N2的能垒最小化。
总之,该工作设计制备的催化剂有望为电催化研究带来新思路,推动电催化领域的快速发展。
Yuliang Li et al. Graphdiyne interface engineering: highly active and selective ammonia synthesis. Angew., 2020.
DOI: 10.1002/anie.202004213
https://doi.org/10.1002/anie.202004213











