新的一期为大家带来的是微/纳米马达,微软机器人在体内进行递送和治疗疾病的2020年来发表在顶刊上的最新论文!
1. Science Robotics:多功能表面microrollers,用于在生理血流中靶向输送货物
移动微型机器人为在人体内难以接近的区域以最小侵入性为目标的医疗治疗方法提供了广阔的前景。循环系统代表了理想的航行路线;但是,血流会削弱微型机器人的推进力,特别是对于整体尺寸小于10微米的微型机器人。此外,细胞和组织特异性靶向是有效识别疾病部位和在动态流动条件下长期保存微型机器人所必需的。于此,马克斯 · 普朗克智能系统研究所MetinSitti等人报道了受循环系统中白细胞启发的直径约3.0微米和〜7.8微米的细胞大小的多功能表面microrollers,用于将药物靶向递送至特定细胞并控制血流内的导航。
本文要点:
1)受白细胞启发的球形microrollers由磁响应的Janus微粒组成,该微粒具有靶向癌细胞(抗HER2)的靶向抗体功能和光可裂解的癌症药物分子(阿霉素)。
2)microrollers的磁性推进和操纵导致平移运动速度高达每秒600微米,每秒约76体长。通过在细胞单层上microrollers的主动推进和操纵,证明了在异种细胞群中能靶向癌细胞。
3)多功能microrollers被用于抵抗在平面微通道和内皮化微通道上的生理相关的血流(每平方厘米高达2.5达因)。此外,microrollers产生足够的上游推进,以在生理相关的血流中在倾斜的三维表面上运动。
此处描述的多功能microrollers平台为循环系统中的体内控制推进、导航和目标主动货物输送提供了一种生物启发的方法。
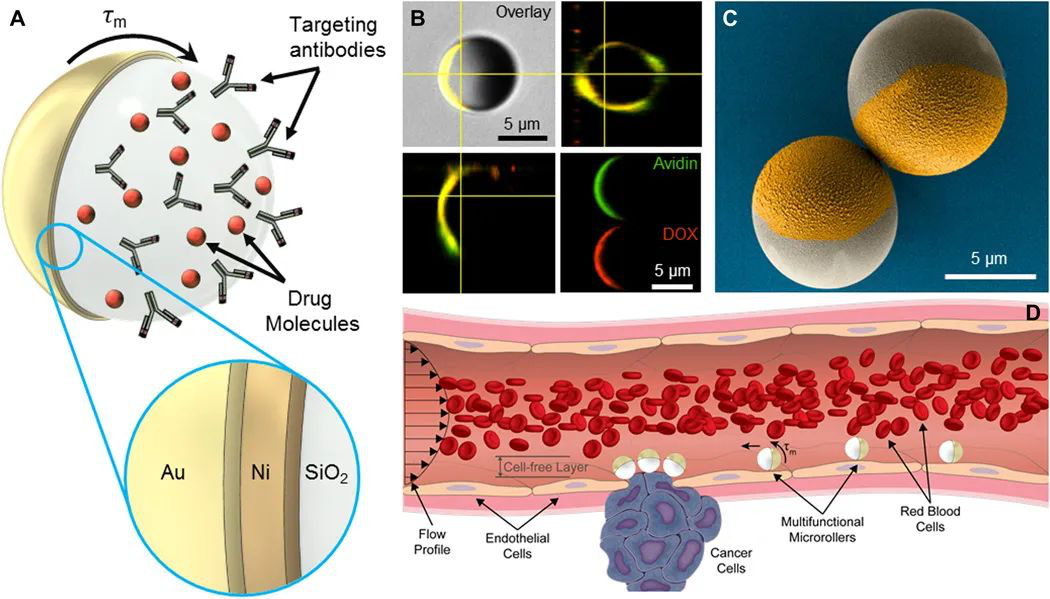
AlapanY, et al. Multifunctional surface microrollers for targeted cargo delivery inphysiological blood flow. Science Robotics. 2020;5(42):eaba5726.
https://robotics.sciencemag.org/content/5/42/eaba5726
2. AM:具有精确磁集体控制的仿生软微机器人用于微血管溶栓
用于生物医学应用的新时代软微机器人需要模拟自然界生物的基本结构和集体功能。生物相容性界面、智能功能和精确的运动控制是设计适应复杂生物环境的软微机器人的关键参数。在此,同济大学何斌、成昱、王启刚等人以趋磁细菌(MTB)为灵感,研制了一种运动响应快、定位准确的仿生磁性微机器人(BMM),用于靶向溶栓。
2)模拟结果表明,组装的程度和速度与场强成正比。BMM最大速度可达161.7µm s−1,在旋转磁场下实现精确定位控制,偏差小于4%。
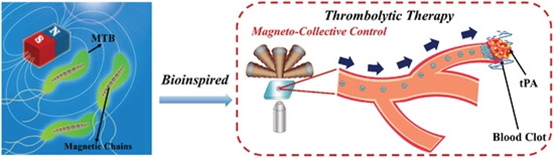
Meihua Xie, et al. BioinspiredSoft Microrobots with Precise Magneto‐CollectiveControl for Microvascular Thrombolysis, Adv. Mater., 2020.
3. AM: 多室管状微马达,以增强局部主动传递
具有空间分辨隔室的管状微电机被提供用于有效的特定地点货物输送,其具有后端锌(Zn)推进剂发动机段和预先装载货物的明胶段,其进一步由pH响应帽保护。多室微电机显示出强大的胃动力推进力,其寿命可调,具体取决于Zn段长度。这种推进通过推动和撞击前端货物段到胃壁上来显著增强马达在胃组织中的分布和保留。一旦微马达穿透胃粘膜(pH≥6),其pH响应帽溶解,促进了自主局部货物的释放。加州大学圣地亚哥分校Joseph Wang和张良方等人系统地测试和讨论了制造过程,物理化学性质和推进行为。
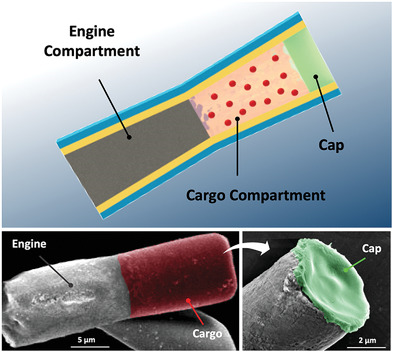
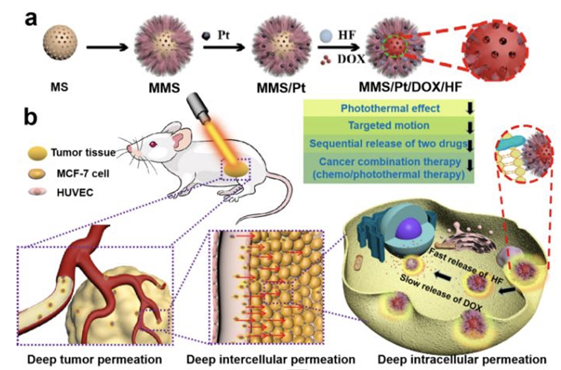
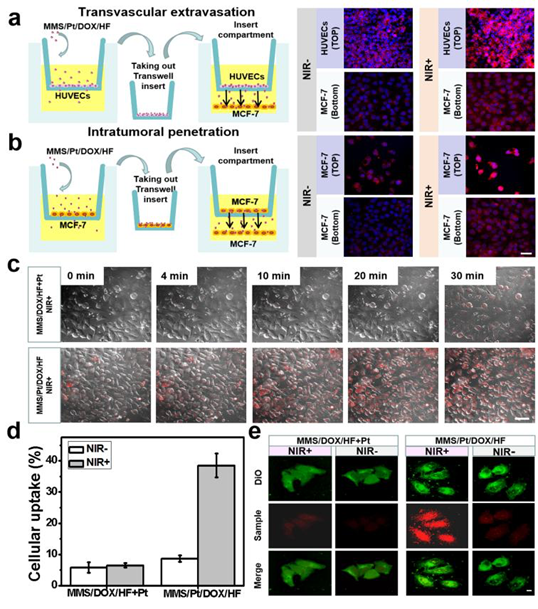
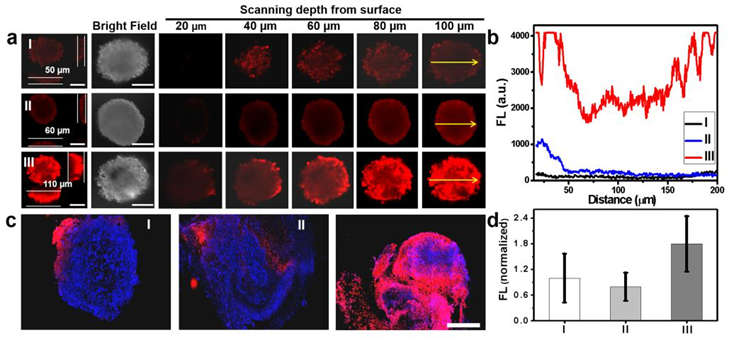
4. Angew:多功能纳米马达用于癌症联合治疗的研究
治疗药物有限的肿瘤渗透性是当前癌症治疗方法面临的巨大挑战,开发可在人体中移动的纳米马达一直是许多研究人员的方向,许多科学家为此做出了不懈的努力。另一方面,不同类型的纳米马达与细胞、肿瘤之间的相互作用也非常重要。再者,当前大多数载药的纳米马达只有单个孔状结构,缺乏携带不同功能药物的能力,这也是限制其应用的重要因素。
https://doi.org/10.1002/anie.202002452
5. ACS Nano:用于流动血液运送货物的精子微马达
在复杂的生物环境中,微马达被认为是无约束微操作和有针对性的物质运输的有前途的候选者。然而,它们在循环系统中的可行性受到限制,因为许多报道的合成微马达显示出低推力,不足以克服高流量和复杂的血液成分。有鉴于此,德国莱布尼兹纳米科学研究所的HaifengXu、Mariana Medina-Sánchez等研究人员,提出了一种混合精子微马达,它能主动逆着流动的血液(连续的和脉动的)游动,并执行肝素物质输送的功能。
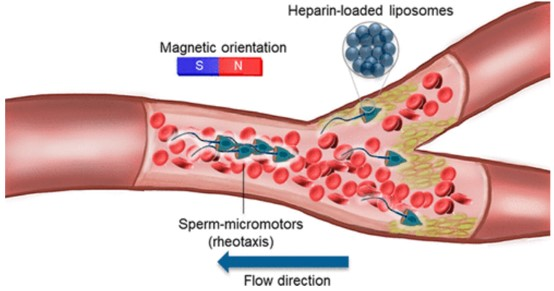
6. Small:病毒样纳米颗粒在小鼠卵巢肿瘤模型中的主动递送促进抗肿瘤活性
病毒样纳米颗粒(VLPs)因其独特的固有免疫刺激特性,已成为肿瘤免疫治疗的一种有吸引力的手段。然而,对于卵巢癌等腹膜转移性肿瘤,由于治疗的腹膜腔大,排泄快,需要多次注射治疗。在此,美国加利福尼亚大学圣迭戈分校Nicole F. Steinmetz、JosephWang等人报道了利用生物相容性Qβ VLPs负载Mg基微马达的活性VLP载体治疗腹膜卵巢肿瘤的的研究进展。
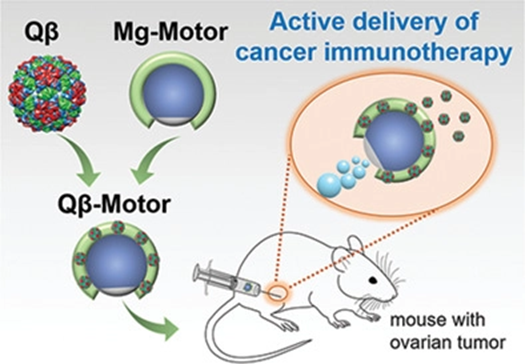
Chao Wang, et al. ActiveDelivery of VLPs Promotes Anti‐TumorActivity in a Mouse Ovarian Tumor Model, Small, 2020.