张良方,2002年进入美国伊利诺伊大学香槟分校化工系,在Steve Granick教授的指导下攻读博士学位。2006~2008年加入麻省理工学院化工系,在Robert Langer教授的研究组进行博士后工作。2008年7月,加入加州大学圣地亚哥分校纳米工程系任助理教授,于2012年3月晋升为终身副教授,2014年7月晋升为终身正教授。
2009年获得美国化学会的Victor K. LaMer奖;2013年被《麻省理工学院技术商评》杂志评为“2013年度世界最杰出青年创新专家”;2014年获美国化学工程师学会的Allan P. Colburn奖;2015年入选美国医学和生物工程学会会士。
奇物论编辑部针对张良方教授近期的研究成果进行归纳总结,供大家学习和交流!
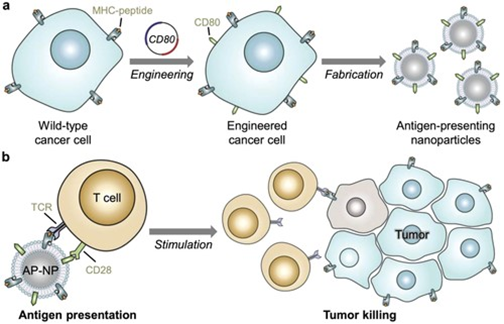
1. Advanced Materials:工程细胞膜包裹的纳米粒子直接呈递肿瘤抗原以促进抗癌免疫最近免疫疗法的成功突出了利用免疫系统对抗癌症的力量。为了使大多数以免疫为基础的治疗成功,必须调动具有正确肿瘤靶向特异性的T细胞亚群。当缺乏这种特异性时,为免疫系统提供处理和递呈的肿瘤抗原物质是刺激抗原特异性T细胞群的一种常见策略。虽然原则上很简单,但经验表明,抗原呈递过程的操作可能非常复杂,需要复杂的策略,而这些策略很难转化。有鉴于此,美国加利福尼亚大学圣地亚哥分校的Liangfang Zhang、RonnieH. Fang等研究人员,报道了一种仿生纳米颗粒平台的设计,该平台可用于直接刺激T细胞,而不需要专业的抗原提呈细胞。1)这些纳米粒子是使用从癌细胞中提取的细胞膜涂层制造的,该涂层是为了表达共刺激标记而设计的。2)与膜表面自然呈现的多肽表位结合,最终的配方包含了促进肿瘤抗原特异性免疫反应所需的信号,启动T细胞,可用于控制肿瘤生长。本文报道的方法代表了一种新兴的策略,可用于开发多抗原,个性化的癌症免疫疗法。
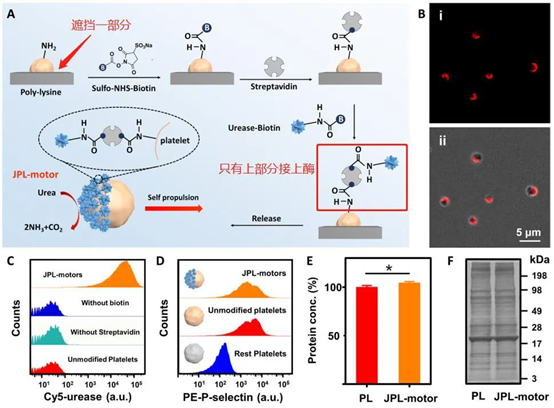
Yao Jiang, et al. Engineered Cell‐Membrane‐Coated Nanoparticles Directly Present Tumor Antigens to PromoteAnticancer Immunity. Advanced Materials, 2020.DOI:10.1002/adma.202001808https://onlinelibrary.wiley.com/doi/full/10.1002/adma.2020018082. 张良方/张学记院士等Science子刊 | 化被动为主动,天然血小板转身变成主动递药系统!(深度解读)美国加州大学圣地亚哥分校JosephWang、张良方教授联合北京科技大学张学记院士等人通过用尿素酶对血小板表面进行不对称功能化开发了一种独特的细胞机器人系统。当暴露于天然燃料(尿素)时,酶通过将底物燃料转化为不对称的驱动力来推动血小板机器人,从而起到微马达的作用。这种移动细胞被称为Janus血小板微马达(JPL马达)。
Tang S, et al.Enzyme-powered Janusplatelet cell robots for active and targeted drug delivery.Science Robotics.2020;5(43):eaba6137.具有空间分辨隔室的管状微电机被提供用于有效的特定地点货物输送,其具有后端锌(Zn)推进剂发动机段和预先装载货物的明胶段,其进一步由pH响应帽保护。多室微电机显示出强大的胃动力推进力,其寿命可调,具体取决于Zn段长度。这种推进通过推动和撞击前端货物段到胃壁上来显著增强马达在胃组织中的分布和保留。一旦微马达穿透胃粘膜(pH≥6),其pH响应帽溶解,促进了自主局部货物的释放。加州大学圣地亚哥分校Joseph Wang和张良方等人系统地测试和讨论了制造过程,物理化学性质和推进行为。1)增强保留。使用老鼠模型,装载有模型货物的多室马达与单室马达相比,显示出均匀的货物分布以及在胃衬里中大约四倍增强的保留,同时没有显示明显的毒性。2)组合治疗。除了基于明胶的隔室之外,治疗有效载荷还可以加载到pH响应性帽中,导致同时递送和顺序释放双重货物以进行组合治疗。总体而言,这种多室微马达系统提供了独特的功能和优势,将进一步推动合成微马达的开发,用于生物医学货物的主动运输和局部递送。
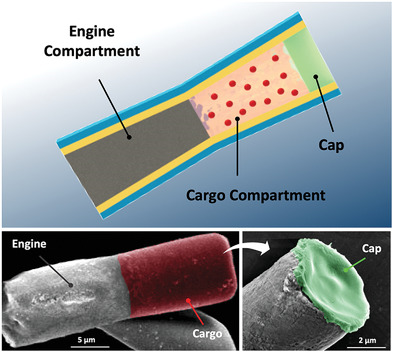
Esteban‐Fernández de Ávila, et al. Multicompartment Tubular Micromotors TowardEnhanced Localized Active Delivery. Adv. Mater. 2020, 2000091.
DOI: 10.1002/adma.202000091https://doi.org/10.1002/adma.202000091长期以来,人们一直认为抑制磷脂酶A2(PLA2)可用于治疗与PLA2活性升高有关的各种疾病。但是,仍然没有安全有效的PLA2抑制剂。于此,加州大学圣地亚哥分校张良方教授报告了一种仿生纳米颗粒设计,该设计可实现针对PLA2抑制的“引诱和杀死”机制(称为”L&K-NP“)。1)L&K-NP由包裹有修饰的红细胞膜的聚合物核制成,该膜具有两个插入的关键成分:蜂毒肽和油氧乙基磷酰胆碱(OOPC)。蜂毒蛋白可作为PLA2引诱剂,与膜脂质一起“诱引”进入的PLA2进行攻击。同时,OOPC充当抑制剂,可在酶攻击时“杀死” PLA2。两种化合物都被整合到L&K-NP结构中,从而消除了与自由分子相关的毒性。2)在研究中,L&K-NPs有效抑制PLA2诱导的溶血。在使用致死剂量的有毒PLA2的小鼠中,L&K‐NPs也能抑制溶血,并具有显著的生存效益。此外,L&K‐NPs对小鼠没有明显的毒性。该设计为一种安全有效的抗PLA2方法提供了平台技术。
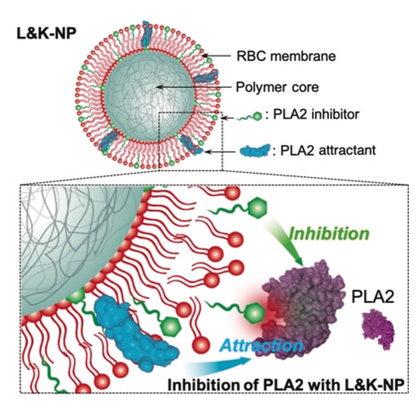
Zhang, Q., et al. (2020), ABiomimetic Nanoparticle to “Lure and Kill”PhospholipaseA2. Angew. Chem. Int. Ed..DOI:10.1002/anie.202002782https://doi.org/10.1002/anie.2020027825. Science子刊:血小板膜包裹MOF纳米粒体内靶向基因沉默小干扰RNA(SiRNA)是一种强有力的基因沉默工具,已被广泛应用于生物医学领域,但在体内的治疗应用面临诸多挑战。有鉴于此,美国加利福尼亚大学圣地亚哥分校的张良方教授、Ronnie H. Fang等研究人员,报道了一种血小板细胞膜包裹的金属-有机骨架(MOF)纳米递送平台,用于体内靶向递送siRNA。本文要点1)MOF核心具有很高的载药量,其对pH的敏感性使细胞摄取时的内体破坏成为可能。细胞膜涂层提供了一种与疾病底物进行生物接触的自然方式。
2)结果表明,在体外可以对多个靶基因获得较高的沉默效率。使用小鼠异种移植模型,观察到显著的抗肿瘤靶向性和治疗效果。总体而言,本文提出的仿生纳米递送系统提供了一种在体内实现基因沉默的有效手段,并可用于扩大siRNA在一系列与疾病相关的应用中的适用性。Jia Zhuang, et al. Targeted gene silencing in vivo by plateletmembrane–coated metal-organicframework nanoparticles. Science Advances, 2020.DOI:10.1126/sciadv.aaz6108https://advances.sciencemag.org/content/6/13/eaaz6108?rss=16. Small:仿生纳米海绵用于抑制全分泌致病蛋白细菌产生的体内杀伤性包裹完整红细胞膜的聚合物纳米颗粒可作为一种仿生纳米海绵(RBC-NS)去吸收和中和与许多细菌感染相关的细菌毒性因子。耐甲氧西林金黄色葡萄球菌(MRSA)的全分泌蛋白(wSP)在小鼠体内可以诱导产生致死性。wSP不仅保持了细菌毒性的复杂性,同时也解决了活细菌感染的复杂性和动态性问题。张良方等人分析了RBC-NS对MRSAwSP的体外中和能力。通过小鼠模型的体内研究进一步证明, RBC-NS可显著降低wSP诱导的致死率。此外,当小鼠服用亚致死剂量的MRSA上清液时,RBC-NS也可减少肺损伤并抑制脾脏核转录因子kappa B的活化。这些结果也为RBC-NS治疗MRSA感染(如MRSA菌血症和MRSA诱导的败血症)提供了系统的评价。
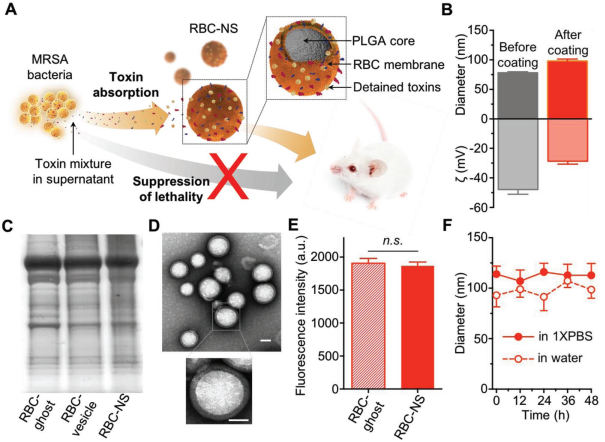
Chen, Y.J., Zhang, Y. et al. BiomimeticNanosponges Suppress In Vivo Lethality Induced by the Whole Secreted Proteinsof Pathogenic Bacteria.DOI: 10.1002/smll.201804994https://doi.org/10.1002/smll.201804994