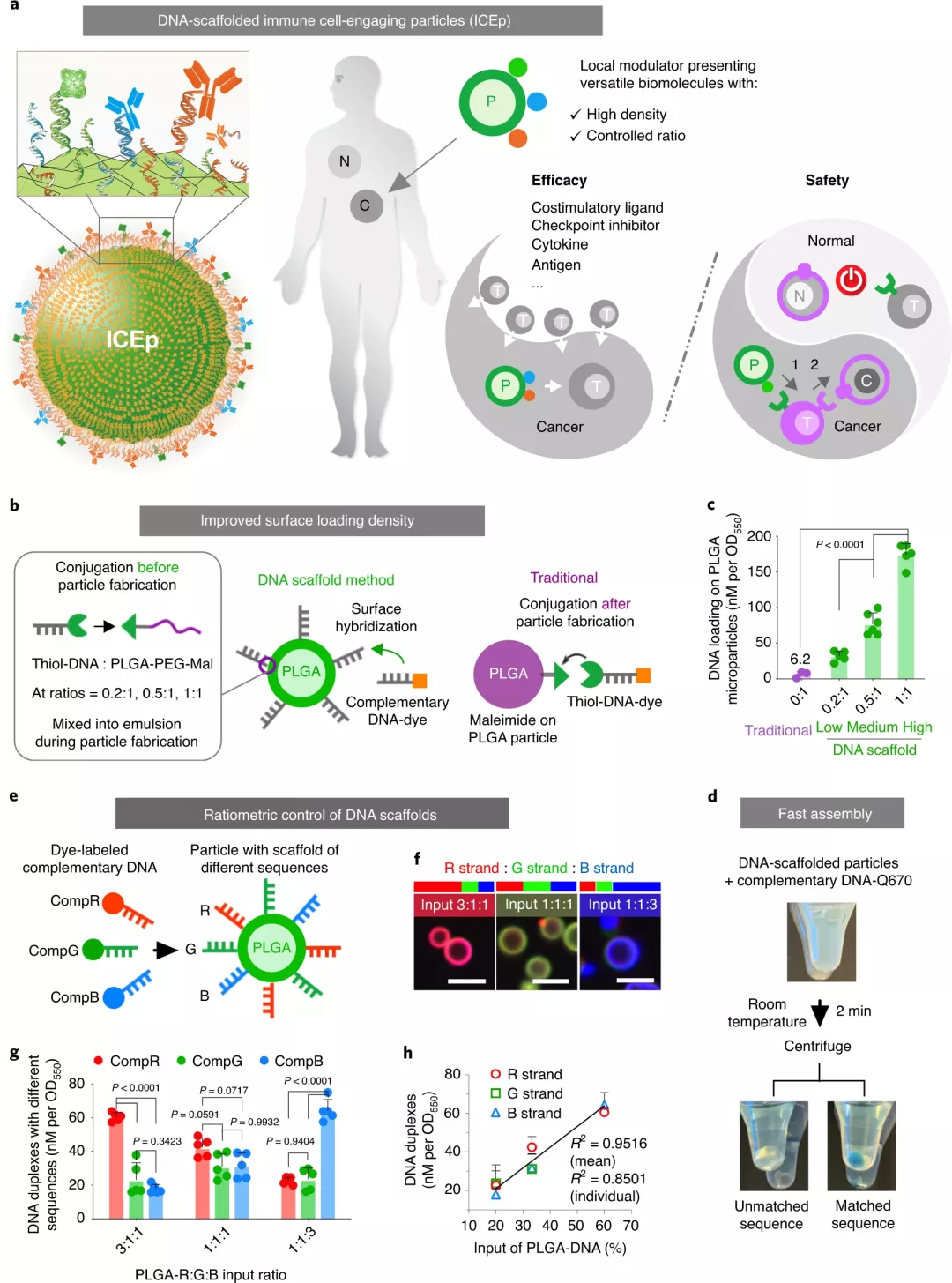
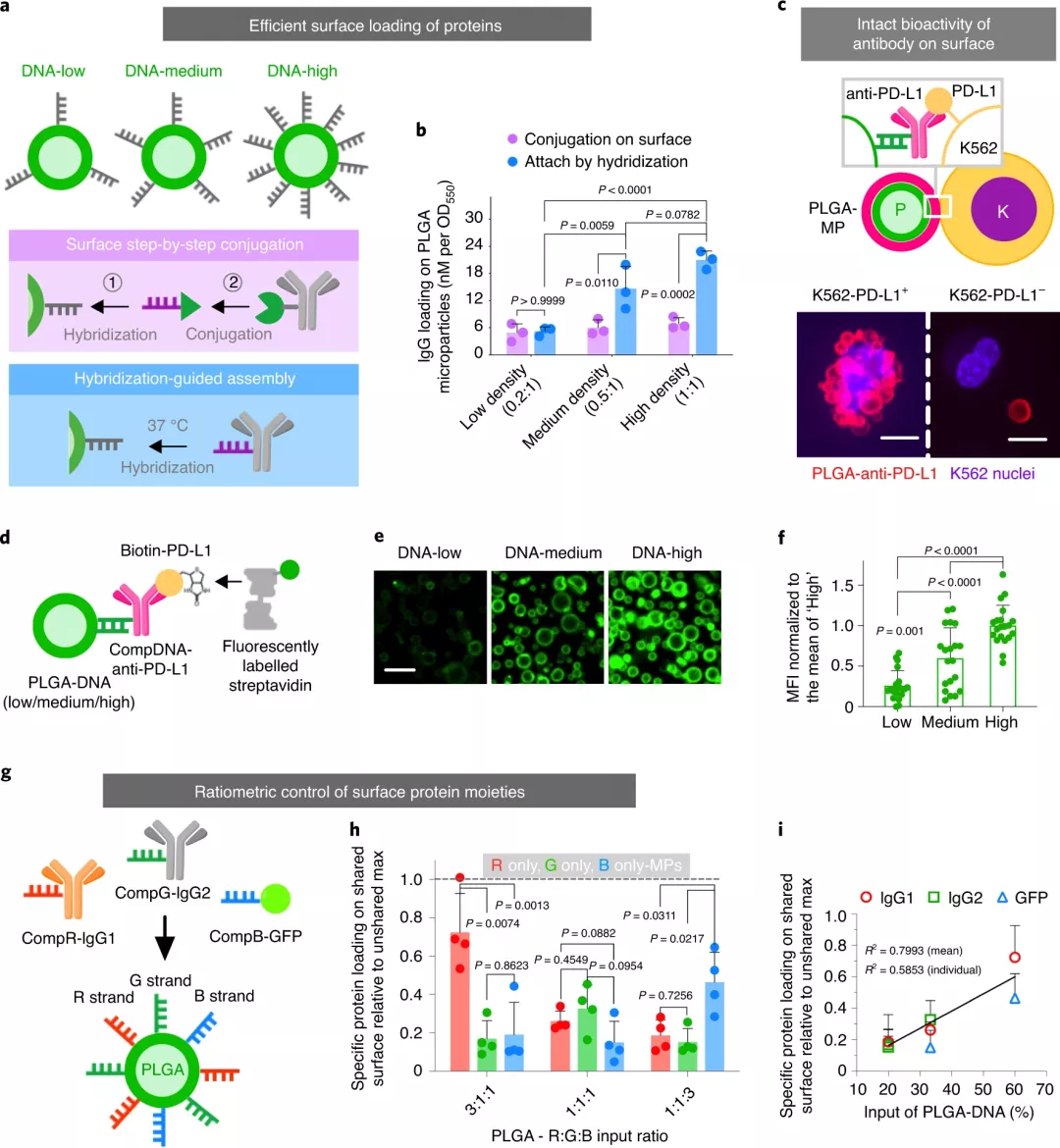
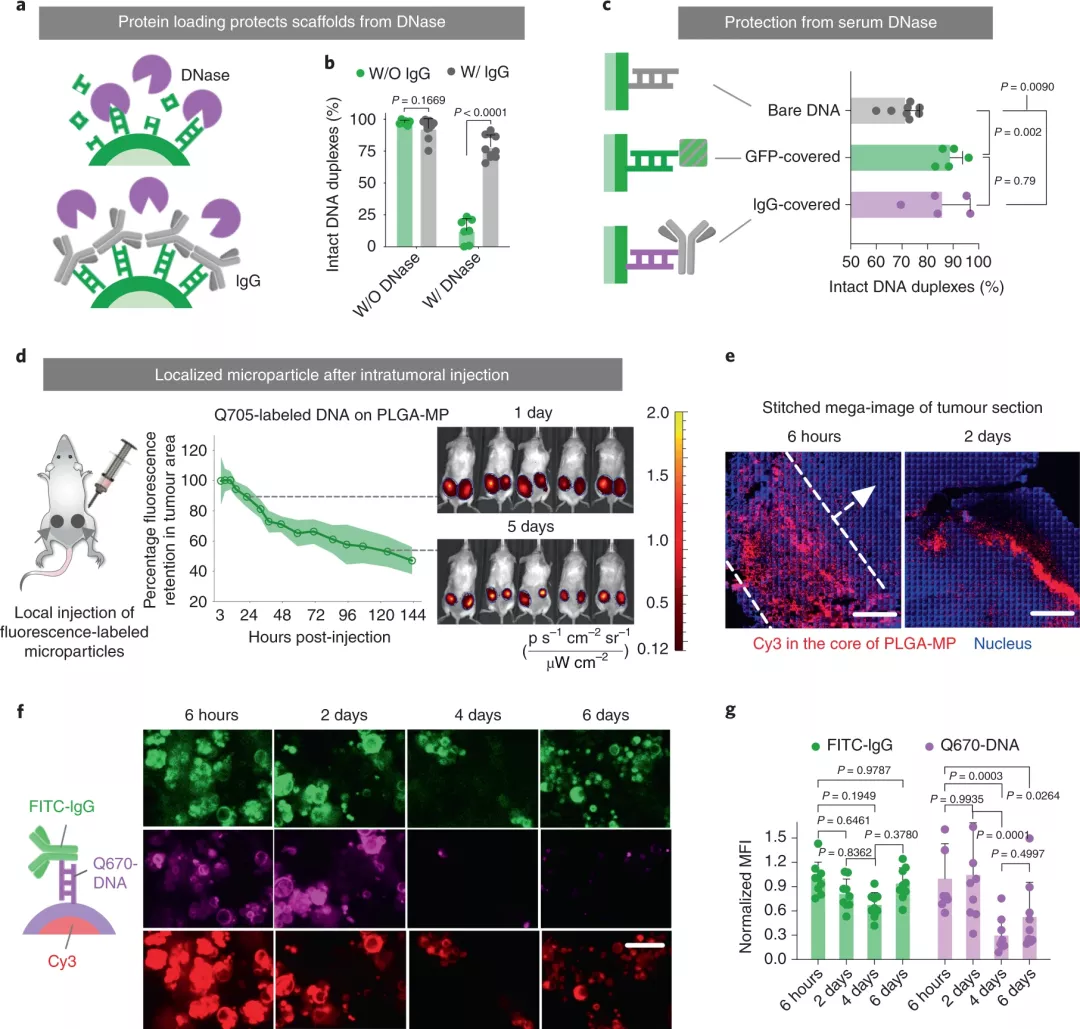
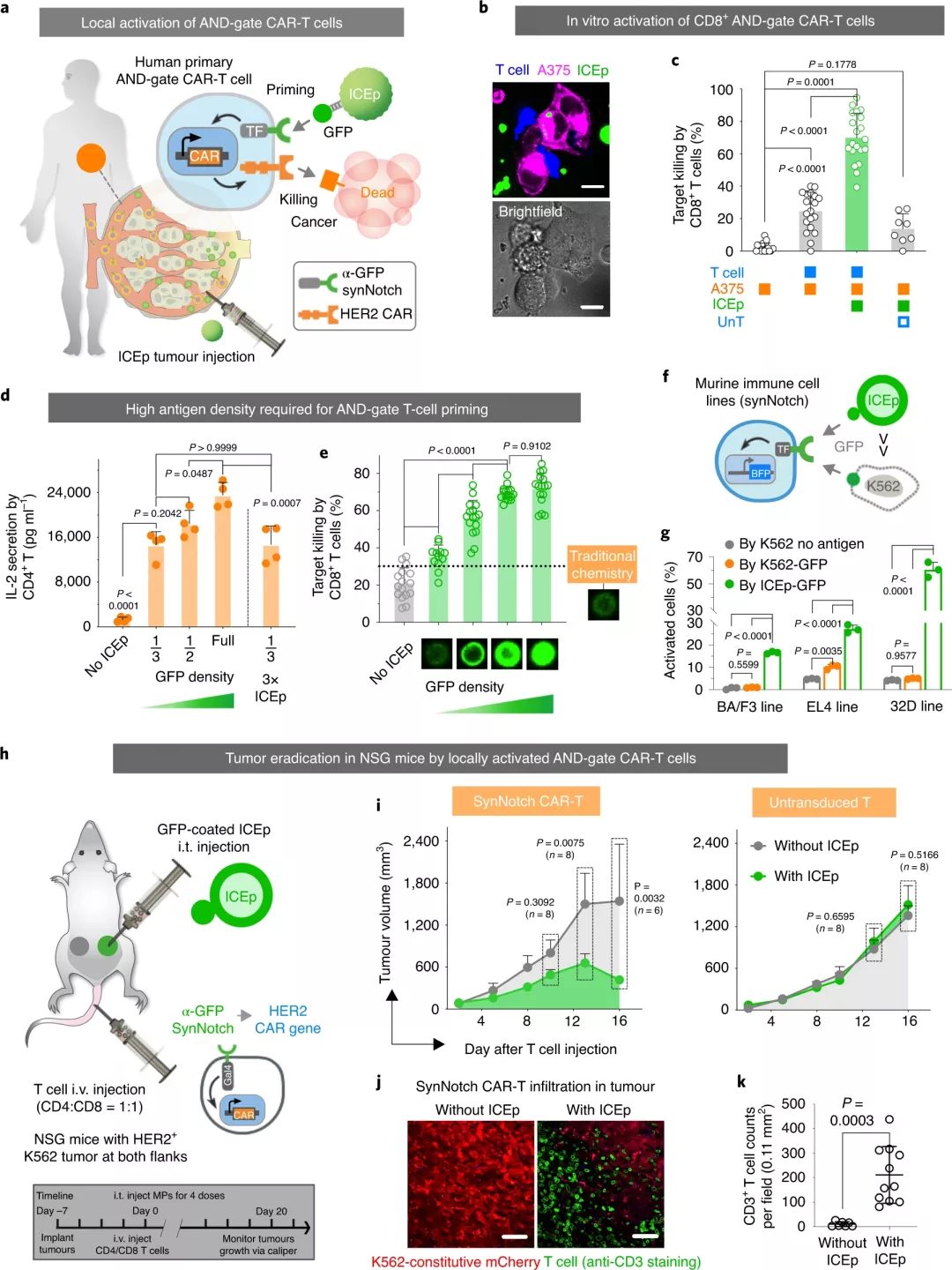
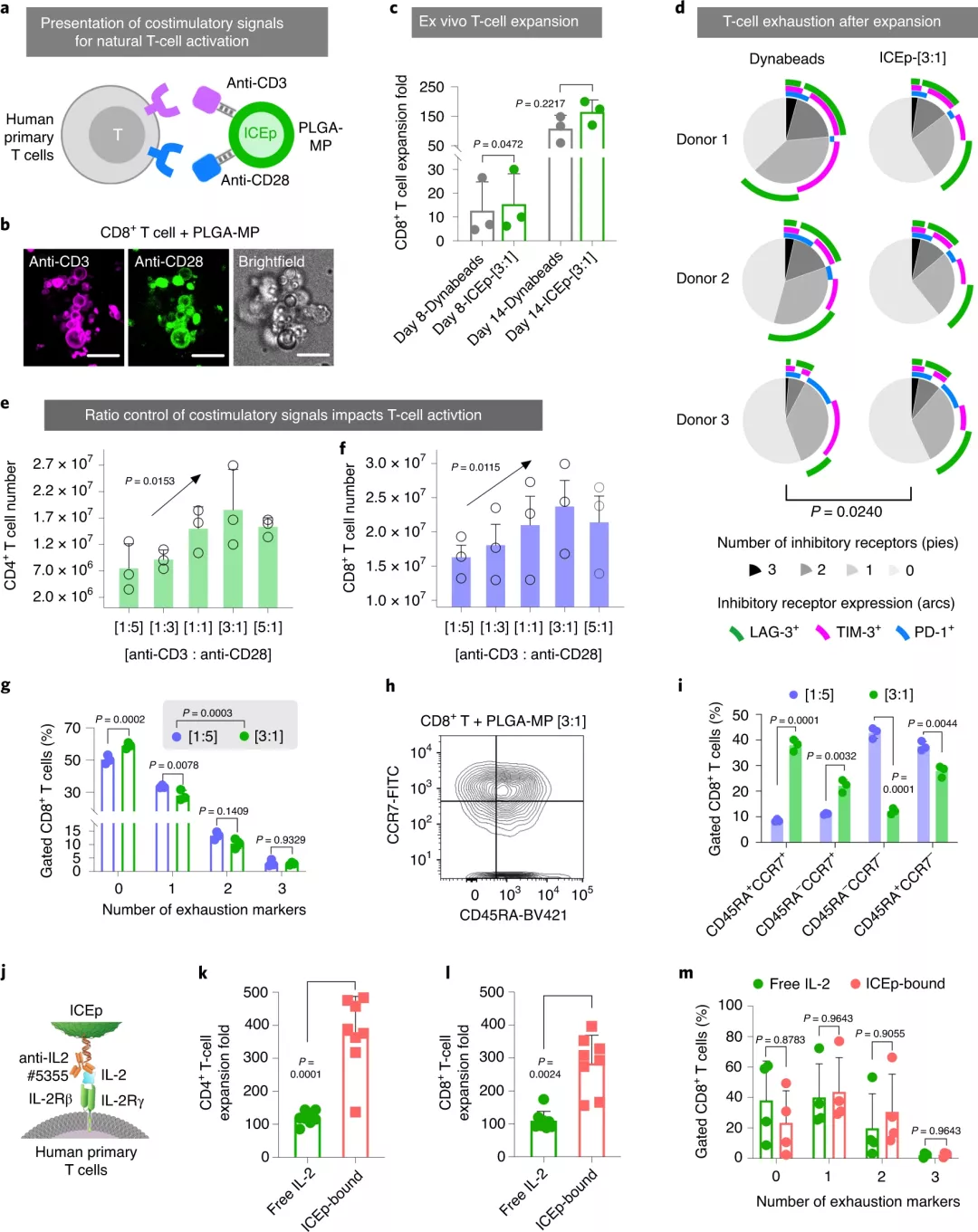
免疫细胞疗法在癌症治疗方面显示出巨大的潜力,但在治疗应用中仍面临着疗效和安全性方面的重大挑战,例如,针对广泛的患者和实体瘤进行嵌合抗原受体(CAR)T细胞治疗。免疫调节信号,包括共刺激配体、细胞因子和检查点抑制剂,被广泛用于增强免疫细胞活性和调节肿瘤环境以提高疗效。合成的生物相容性材料已被用作这些生物分子的载体,以促进体内的特异性定位和延长的稳定性,从而调节天然或工程免疫细胞的活性。为了增加肿瘤靶向特异性并避免脱靶效应,CAR T细胞经过工程改造成需要检测靶细胞上的两个抗原,即具有“与”门激活控制功能,第一种抗原激活CAR表达,然后第二种抗原启动靶标杀伤。但是,这种方法的临床应用需要了解有关控制T细胞活性的因素的知识,例如 “与“门启动或CAR靶向抗原的肿瘤相关抗原密度,这对于治疗很重要。生物材料以期望的密度呈现引发信号(天然或合成抗原)以激活此类工程化T细胞将减轻用于临床转化用途的双抗原设计的安全性问题。而且抗体-抗原结合在表面需要一个基于特定抗体的空间耐受性的空间阈值,因此高密度和可控的表面生物分子可以精确控制配体结合和细胞调节。目前,对生物降解材料表面的高密度生物分子(特别是蛋白质/抗体)进行功能化,并以精确控制的比例呈现多个部分,这一点尚未得到满足。那么,利用何种策略可以更好地对生物材料进行表面生物分子功能化呢?于此,加州大学旧金山分校Tejal A. Desai和Wendell A. Lim等人认为通过Watson-Crick碱基配对来合成具有可控序列和独特组装方式的天然短寡核苷酸天然聚合物将是生物分子受控表面功能化的理想连接体。因此,他们开发了生物相容性免疫细胞结合颗粒(ICEp),该颗粒使用合成的短DNA作为支架来有效和可调节地加载蛋白质,从而扩展了免疫调节的潜力。成果发表于Nature Nanotechnology上。研究人员使用生物相容性聚乳酸-乙醇酸共聚物(PLGA)聚合物制造了微米级的ICEp。通过乳液法将DNA链固定在聚合物颗粒的表面,形成一种可适应生物活性分子负载的支架。通过对聚合物、DNA长度、溶剂和反应条件的优化,合成了聚合物-DNA两亲分子,形成了具有致密DNA支架的稳定PLGA粒子。直接将反应混合物与增加聚合物-DNA共轭物结合在一起,可以使表面有效负载可附着的DNA支架密度不断增加。令人惊讶的是,颗粒上的最高平均表面负载密度可达到球形颗粒的理论极限值。特别地,这种杂交引导的负载比传统方法的负载效率高约27倍。这种杂交指导的组装方案具有生物相容性,方便且快速,因此在室温下孵育2分钟可达到最大载量的〜87%。带有表面DNA支架的聚合物微/纳米颗粒用于蛋白质呈递,可以对免疫细胞疗法进行多种调节此外,使用独特的DNA核苷酸序列可以独立控制将多个货物装载在同一材料表面上。该方法可以使用以下两种策略之一将生物分子加载到DNA支架颗粒的表面:(2)通过将互补的DNA-生物分子偶联物直接与支架杂交。使用PLGA颗粒上的比例控制序列,研究人员通过杂交引导组装共装载了三种蛋白质(GFP和两种抗体),每种蛋白质分别附着于三条独特的互补DNA链之一。每种蛋白质货物的分布与各自的支架种群相关,证明了使用该策略实现的稳健的比例控制。图|DNA支架可将多种治疗性蛋白质以精确可调的比例有效负载在颗粒表面通过表面修饰蛋白后,可降低DNA酶对DNA支架的降解作用,体内成像表明DNA支架微粒的注射可用于向体内治疗细胞发送局部的,持续的信号。且生化分析也证明了其安全性。研究人员将微米大小的ICEp上的正交抗原(GFP)束缚到启动用抗原识别回路改造的“与“门CAR-T细胞,从而将CAR T细胞毒性限制为局部注射微粒的肿瘤。这些“与“门 T细胞仅当两种抗原均呈递给T细胞时才诱导杀伤,一种激活synNotch受体以释放用于CAR表达的TF域,另一种激活CAR介导的细胞毒性。这就使得ICEp可以在体内为synNotch CAR-T细胞的局部激活和诱导肿瘤清除提供空间控制的信号,而与健康组织发生交叉反应的风险则被限制了。图|通过肿瘤内注射呈递抗原的ICEp局部激活AND门CAR-T细胞杀死肿瘤为了证明该平台对免疫细胞调节的多功能性,研究人员在可生物降解的PLGA微粒上设计了T细胞共刺激配体抗CD3和抗CD28和抗IL-2,以离体激活人原代T细胞。结果表明,协同刺激配体(抗CD3和抗CD28抗体)的比例控制以及ICEp上细胞因子(IL-2)的表面呈递会显著影响人类原代T细胞活化表型。这对于离体T细胞扩增和在肿瘤部位局部施用IL-2呈递的ICEp都可能是有益的,以激活体内免疫细胞。图|ICEp具有多功能且精确控制的调节信号,能够在离体扩增过程中调节T细胞特征本文展示了一个独特的平台,该平台使用合成的短DNA寡核苷酸作为可生物降解材料的表面支架,以特定比例和密度精确且受控地加载多个生物分子。研究证明:(1)可以将具有完整生物活性的多种免疫调节剂(例如抗原,共刺激配体,检查点抑制剂,细胞因子)加载到ICEp上;(2)抗原呈递ICEp可局部给药以控制体内 “与“门CAR-T细胞的活化和肿瘤清除。(3)共刺激配体(抗CD3和抗CD28)的比例控制以及ICEp表面IL-2的存在会影响离体T细胞的活化和扩增。通过这个高度模块化的平台,生物相容性材料可以作为多种调节性生物分子的基质,包括细胞因子、抗原、检查点抑制剂、激动剂或拮抗剂抗体、佐剂等,调节局部环境,提高免疫细胞在肿瘤免疫治疗中的疗效。关于先前DNA发表在Nature子刊上的报道,可参考:Huang, X., et al. DNA scaffolds enable efficient and tunable functionalization of biomaterials for immune cell modulation. Nat. Nanotechnol. (2020).https://doi.org/10.1038/s41565-020-00813-z