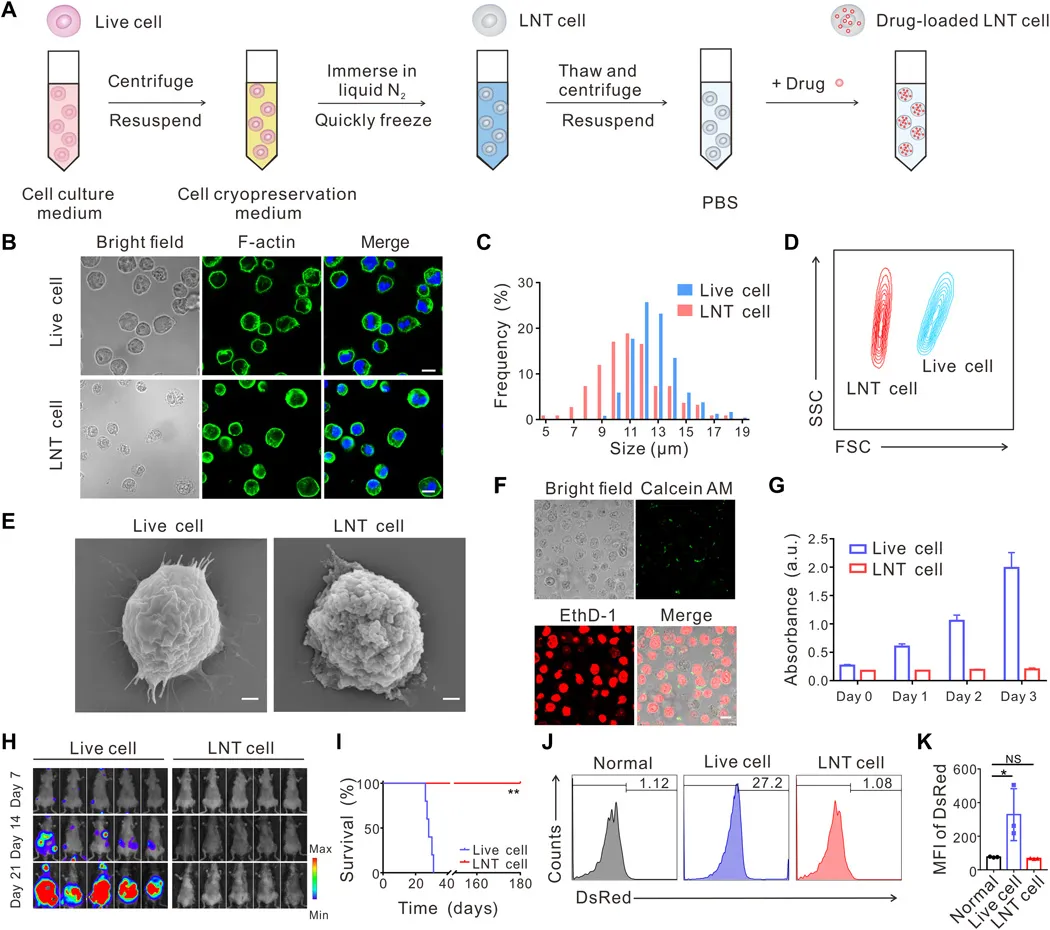
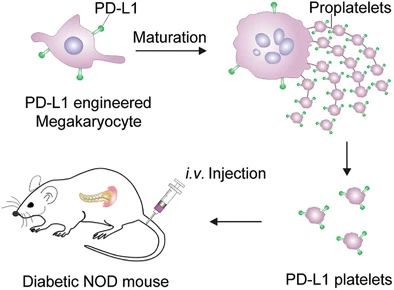
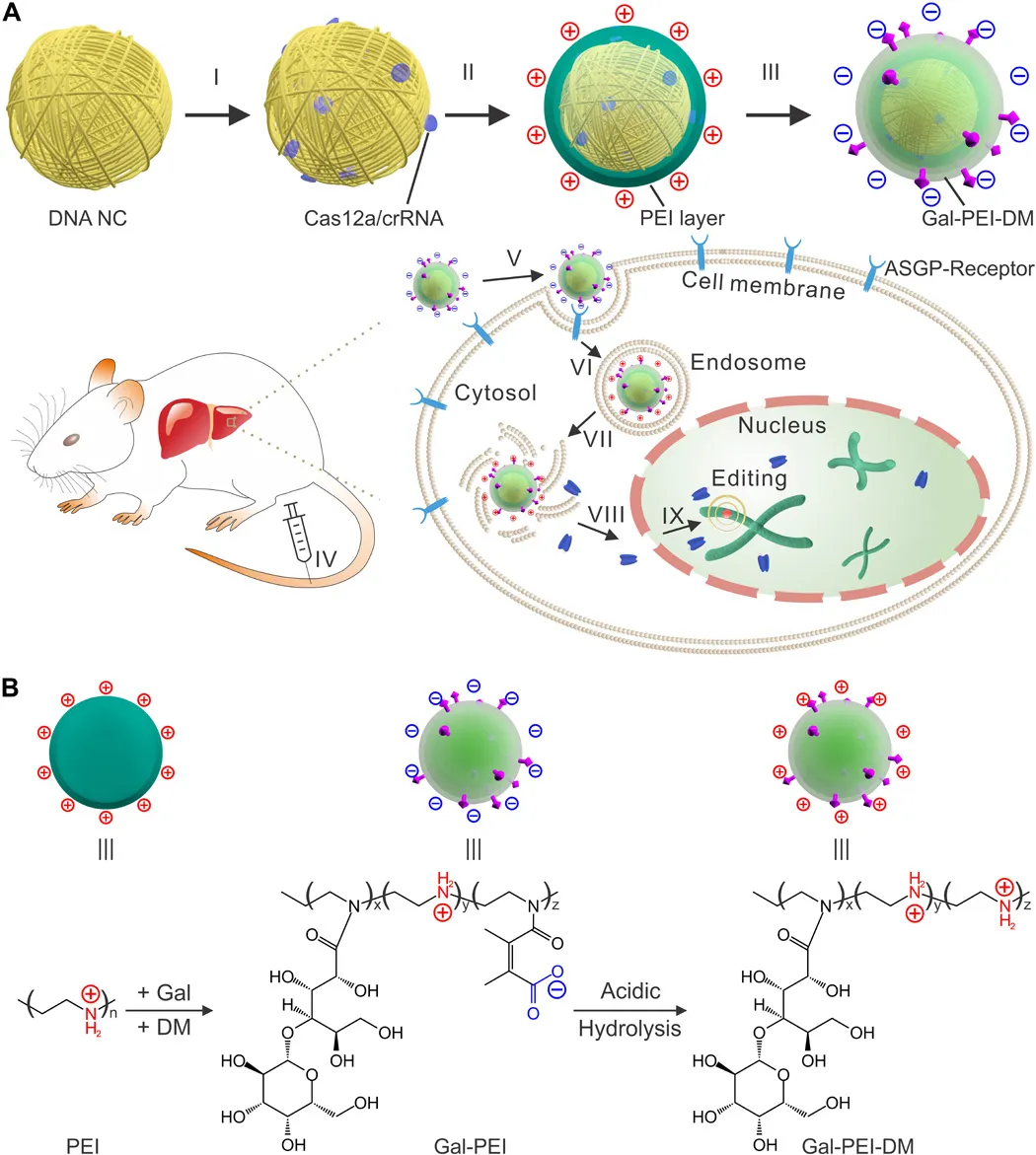
奇物论联合纳米人编辑部对2020年国内外重要科研团队的代表性成果进行了梳理,今天,我们要介绍的是浙江大学药学院院长顾臻教授课题组。顾臻,现任浙江大学求是讲席教授、药学院院长。顾臻团队致力于将生物材料设计,生物大分子工程以及微/纳米工程整合到新的药物输送策略中,且应用刺激响应系统以剂量、空间和时间控制的方式来输送和或释放治疗剂。目前已在Nature Nanotechnology、Nature Biomedical Engineering、Nature Chemical Biology、Science Translational Medicine等期刊发表学术论文200余篇,授权公司专利100余项。以下按照两个部分对顾臻团队2020年期间发表的部分成果进行归纳,供大家学习和交流。1. Science Advances封面,液氮冻死癌细胞,作药物载体!顾臻教授研究团队聚焦于AML细胞本身地归巢能力,开发了一种使用急性髓细胞性白血病细胞作为药物载体,同时消除其固有致病性的方法。该团队主要是利用液氮低温处理而获得治疗性死细胞,这些细胞可以保持完整的结构,从而保持其骨髓归巢能力,还可以包封药物,但失去了增殖能力和致病性。这种基于“死细胞”的递送载体,可实现快速制备,从而有望实现临床转化。成果发表在Science Advances期刊上,并被遴选为期刊封面。Tianyuan Ci, et al., Cryo-shocked cancer cells for targeted drug delivery and vaccination. Science Advances 2020.DOI: 10.1126/sciadv.abc3013https://advances.sciencemag.org/content/6/50/eabc30132. AM:工程化表达PD-L1的血小板逆转新发1型糖尿病1型糖尿病(T1D)的发病机制是胰岛特异性自身反应性T细胞破坏产生胰岛素的β细胞。抑制胰岛特异性自身反应性T细胞来拯救β细胞是治疗新发T1D的一种有前途的方法。免疫检查点信号轴程序性死亡-1/程序性死亡配体1(PD-1/PD-L1)可有效调节T细胞活性,防止自身免疫攻击。在此,美国加州大学洛杉矶分校顾臻、深圳大学黄鹏、德雷塞尔大学成昊等人使用巨核细胞前体细胞通过基因工程过表达PD-L1以产生免疫抑制的血小板。1)PD-L1过表达的血小板(称为PD-L1血小板)聚集在发炎的胰腺中,可能抑制新发高血糖非肥胖糖尿病(NOD)小鼠胰腺自身反应性T细胞的活性,从而保护产生胰岛素的β细胞不受破坏。2)此外,PD-L1血小板治疗还增加了调节性T细胞(Tregs)的百分比,并维持了胰腺的免疫耐受。结果表明,PD-L1血小板对β细胞的保护作用能有效维持新发高血糖NOD小鼠的正常血糖,逆转糖尿病。Xudong Zhang, et al. Engineered PD-L1-Expressing Platelets Reverse New-Onset Type 1 Diabetes, Adv. Mater., 2020.DOI: 10.1002/adma.201907692https://doi.org/10.1002/adma.2019076923. Science Advances:通过DNA介导的生物反应编辑递送CRISPR-Cas12a用于调节胆固醇CRISPR系统已成为功能强大的生物技术工具,在基础研究和药物学中发现了多种应用。然而,有效递送系统的可用性严重阻碍了CRISPR系统的治疗性转化。除广泛研究的CRISPR-Cas9外,CRISPR-Cas12a还是一种有效的基因组编辑工具。然而,为CRISPR-Cas12a开发有效的非病毒递送系统仍然具有挑战性。于此,加州大学洛杉矶分校顾臻教授、Wujin Sun等人展示了一种基于DNA纳米分子(NC)的载体,可用于传递Cas12a/CRISPR RNA(crRNA)核糖核蛋白(RNP)来调节血清中的胆固醇水平。DNA-NC可通过DNA-NC与crRNA的互补作用,有效地负载Cas12a/crRNA-RNP。阳离子聚合物层的加入使DNA模板核浓缩,并允许进一步涂覆电荷反转聚合物层,这使得该组装在生理pH下带负电,但在酸性环境下恢复为正电荷。当选择Pcsk9作为靶基因时,由于其在调节血清胆固醇水平方面的重要作用,体内可观察到有效的Pcsk9破坏(~48%),显著降低Pcsk9的表达,获得胆固醇控制的治疗效果(约有45%的胆固醇降低)。综上所述,这种载体提供了一种平台策略,可以通过应用适当的靶向配体而适于靶向其他器官。crRNA还可以被重新编程以靶向其它感兴趣的基因,用于治疗不同的疾病,并且CRISPR-Cas12a的高度多样性可以方便地同时靶向多个基因。Wujin Sun, et al. CRISPR-Cas12a delivery by DNA-mediated bioresponsive editingfor cholesterol regulation. Sci. Adv. 2020DOI:10.1126/sciadv.aba2983https://advances.sciencemag.org/content/6/21/eaba29834. Matter:通过使用血小板源性细胞外囊泡靶向递送TPCA-1来缓解肺炎中的细胞因子风暴由于肺组织炎症失控,肺炎可导致高发病率和高死亡率。平息细胞因子风暴可能是挽救重症肺炎患者生命的关键之一。有鉴于此,美国加利福尼亚大学的Zhen Gu和苏州大学的Chao Wang等研究人员,受血小板对炎症部位的内在亲和力的启发,设计了血小板衍生的细胞外小泡(PEV),用于肺炎靶向给药。1)在急性肺损伤(ALI)小鼠模型中,血小板活化后容易产生的PEV可以选择性地靶向肺炎。2)PEV通过负载可抑制炎症因子产生的[5-(对氟苯基)-2-脲基]噻吩-3-甲酰胺(TPCA-1),抑制肺部炎症细胞浸润,平息局部细胞因子风暴,明显提高治疗效果。3)此外,研究人员发现PEV可以作为一个广泛的平台,选择性地靶向各种炎症部位,包括慢性动脉粥样硬化斑块、类风湿性关节炎和与皮肤相关的伤口。Qingle Ma, et al. Calming Cytokine Storm in Pneumonia by Targeted Delivery of TPCA-1 Using Platelet-derived Extracellular Vesicles. Matter, 2020.DOI:10.1016/j.matt.2020.05.017https://www.sciencedirect.com/science/article/pii/S25902385203025025. ACS Nano:靶向给药Notch抑制剂可减轻肥胖引起的葡萄糖耐受不良和肝纤维化随着肥胖型2型糖尿病(T2DM)和非酒精性脂肪性肝炎(NASH)发病率的持续增加,对药物治疗的需求变得迫切。然而,为这些慢性疾病寻找和开发新的治疗策略的努力与安全性的需要相平衡,阻碍了临床翻译。这两种疾病的共同病理之一是肝脏中Notch信号通路的不适应性重新激活。γ-分泌酶抑制剂的缺口拮抗可有效抑制NASH的肝糖生成,减轻肝纤维化,但其肝外副作用,尤其是杯状细胞化生,限制了其治疗效果。有鉴于此,美国加利福尼亚大学的顾臻和美国哥伦比亚大学的LiQiang、Utpal B. Pajvani等研究人员,开发了一种纳米颗粒介导的递送系统来靶向肝脏γ分泌酶抑制剂(GSI NPs)。1)GSI NP的应用减少了饮食诱导的肥胖小鼠的肝脏葡萄糖的产生,并减轻了喂食NASH引起的饮食的小鼠的肝纤维化和炎症,没有明显的胃肠道毒性。2)通过改变给药方法,这些结果为改变以前不能耐受的药物的用途提供了概念验证,以解决肥胖引起的T2DM和NASH临床环境中未得到满足的需求。Lauren R. Richter, et al. Targeted Delivery ofNotch Inhibitor Attenuates Obesity-Induced Glucose Intolerance and LiverFibrosis. ACS Nano, 2020.DOI:10.1021/acsnano.0c01007https://pubs.acs.org/doi/abs/10.1021/acsnano.0c010076. Nature Biomedical Engineering: 胰岛素贴片:一天贴一次,全球4亿糖尿病患者的福音糖尿病——一种经常导致严重继发并发症的慢性疾病,影响全球超过4.25亿人。胰岛素治疗在1型糖尿病患者的生活中是必需的,并且通常用于胰岛β细胞功能减退的2型糖尿病患者。日常注射通常遇到很多痛苦,包括频繁监测血糖水平和每天多次皮下注射或输液。这种方法更是繁重且复杂,并且常常由于控制不当和由于错误计算的剂量而导致危及生命的低血糖。 有鉴于此,UCLA顾臻教授团队于近日开发出新一代的经皮智能胰岛素贴片——“智能胰岛素贴片2.0”。该胰岛素贴片只有硬币大小(5 cm2),易于工业生产制造,可实现临床相关剂量的和快速葡萄糖依赖性的胰岛素释放,调节葡萄糖释放时间可超过20h。葡萄糖响应制剂与基于微针的经皮胰岛素技术的结合,为改善葡萄糖水平的调节提供了广阔的前景。另外,在这项研究中开发的GR-MN贴片还为其他药物(如胰岛素类似物,类胰高血糖素肽1受体激动剂和胰高血糖素)的刺激响应性经皮递送系统的开发提供了技术。 据了解,该技术已被FDA的新兴技术计划接受,且研究人员正在为人类临床试验申请FDA批准,预计可以在几年内开始实施。 Yu,J., Wang, J., Zhang, Y. et al. Glucose-responsive insulin patch for theregulation of blood glucose in mice and minipigs. Nat Biomed Eng (2020).https://doi.org/10.1038/s41551-019-0508-y7. PNAS:经皮的冷大气等离子体介导的免疫检查点封锁疗法提高免疫检查点阻断(ICB)治疗的疗效和减少副作用的策略与临床应用息息相关。于此,顾臻等人描述了经皮的冷大气等离子体(CAP)介导的ICB治疗。CAP通过空心结构微针作为微通道的局部递送促进了CAP释放肿瘤相关抗原。随后的T细胞介导的免疫反应可以通过微针传递的免疫检查点抑制剂增强,从而增强局部和全身的抗癌免疫。CAP和ICB与微针的协同作用为肿瘤和其他疾病的治疗提供了一个平台Guojun Chen, et al., ransdermal cold atmospheric plasma-mediated immune checkpoint blockade therapy, Proceedings of the National Academy of Sciences U.S.A. (PNAS), 7(3687), 2020DOI:10.1073/pnas.19178911178. PNAS:混合贴片对胰岛素和胰高血糖素的双重自我调节递送目前用于逆转胰岛素缺乏症的糖尿病治疗方法的疗效往往受到急性低血糖症频繁发生的限制。为此,顾臻等人设计了一种混合型葡萄糖敏感释放贴片,通过在高血糖和低血糖状态下分别释放胰岛素和胰高血糖素,使其发挥合成人工胰腺的功能。开发了一种面膜介导的聚合方法来装载胰岛素和胰高血糖素模块,它们共享共聚基质但包含不同比例的关键单体。发现这两个模块的协同反调节可增强杂化贴片在血糖波动期间维持正常血糖的能力。这种平台策略有助于开发定制的治疗贴片,以精确的方式进行闭环递送。Dual self-regulated delivery of insulin and glucagon by a hybrid patch, Proceedings of the National Academy of Sciences U.S.A. (PNAS), 117(29512), 2020DOI:10.1073/pnas.20110991179. Nano Today:胶体晶体微针贴片用于监测血糖血糖监测是1型或2型晚期糖尿病患者的日常工作。为了提高患者的依从性,需要最小化侵入性,改善便携性以及增强现有葡萄糖监测装置的可持续性。于此,加州大学洛杉矶分校顾臻教授、东南大学顾忠泽等人描述了一种用于肉眼葡萄糖监测的微创胶体晶体微针(MN)贴片。1)葡萄糖反应性胶体晶体(GCC)-MN的设计采用聚合核来机械支撑GCC的外壳,以进行葡萄糖感测和报告。2)GCC-MN贴片可在5min内将葡萄糖浓度转化为肉眼可见的颜色变化,这种葡萄糖反应是可逆的。在1型糖尿病小鼠模型中,使用GCC-MN贴片可同时进行组织液提取、葡萄糖感应和葡萄糖相关的彩色显示程序。Yi Zeng, et al., Colloidal crystal microneedle patch for glucose monitoring. Nano Today 2020.https://doi.org/10.1016/j.nantod.2020.10098410. Biomaterials:透皮比色贴剂用于对糖尿病小鼠进行高血糖传感分析加州大学洛杉矶分校顾臻教授制备了一种可以用于检测小鼠高血糖的透皮比色贴剂。研究表明,3、3、5、5 -四甲基联苯胺(TMB)的显色变化可由葡萄糖氧化酶(GOx)和辣根过氧化物酶(HRP)在高的葡萄糖水平下通过级联酶反应而引起。实验利用磷酸钙(CaP)壳对该贴剂上层的HRP进行生物矿化反应,使其具有pH响应的特性,并可提高检测的敏感性以及防止发生非特异性反应。实验结果表明,该比色传感器可以对小鼠间质液进行微创提取,并将葡萄糖水平迅速转化为可见的颜色变化,而定量的红、绿、蓝(RGB)信息可以通过微针的扫描图像获得。因此,这种低成本的便携式比色传感器可以在不抽血的情况下对每日血糖水平进行检测。Zejun Wang, Zhen Gu. et al. Transdermal Colorimetric Patch for Hyperglycemia Sensing in Diabetic Mice. Biomaterials. 2020https://www.sciencedirect.com/science/article/pii/S0142961220300284此外,顾臻团队2020年还发表了其他相关的高水平研究论文,由于篇幅关系就不在此一一展示,感兴趣的读者可前往该课题组网站进行学习。课题组网站:https://imedicationlab.net/顾臻,江苏南通人,浙江大学求是讲席教授、药学院院长。本科、硕士毕业于南京大学化学系及高分子科学与工程系;2010年于加州大学洛杉矶分校(UCLA)获得工学博士学位;同年博士后获聘于麻省理工学院化工系/Koch癌症综合研究院、哈佛大学医学院,师从Robert Langer教授。2012-2018年任教于北卡罗莱纳大学教堂山分校/北卡州立大学联合生物医学工程系,领导药剂工程学科建设,并创建了 “创新转化学位”,以促进生物医药技术产业化人才的培养,2018年获评Jackson Family杰出讲席教授。2018-2020年任UCLA生物工程系正教授,并任生物技术/生物医学与工程培训中心主任。2020年9月全职受聘于浙江大学。其指导的“iMedication-智能医药实验室”研究方向包括蛋白质递药系统、生理响应材料、免疫治疗制剂、细胞治疗策略等。目前已发表学术论文200余篇,授权公司专利100余项。顾臻教授曾获“斯隆研究奖”、英国皇家化学会Felix Franks奖章、国际药物控释学会(CRS)“青年学者奖”、Small青年科学家创新奖、美国糖尿病学会(ADA) “Pathway”研究奖、美国生物医学工程学会(BMES)“细胞/分子生物工程创新者奖”等。《麻省理工科技评论》曾将其评为“TR35世界杰出创新家”。2019年当选美国医学与生物工程院会士。其课题组首次报道了血糖响应“智能胰岛素贴片”的原型,提出了闭路透皮递药系统的新概念,率先利用血小板的靶向性及脂肪细胞的代谢通路递送抗癌药物,并系统拓展了微针的生物医用创制,相关技术正在临床转化。顾臻教授目前担任《Science Advances》及《Nano Research》副主编,并任CRS中国代表。