奇物论联合纳米人编辑部对2020年国内外重要科研团队的代表性成果进行了梳理,今天,我们要介绍的是苏州大学功能纳米与软物质研究院刘庄教授课题组。
刘庄教授课题组近年来在生物材料与纳米医学领域从事研究,围绕肿瘤诊疗中的若干挑战性问题,发展了一系列新型纳米探针用于体外生物检测与活体分子影像,并探索了多种基于纳米技术和生物材料的肿瘤光学治疗、放射治疗、免疫治疗等新策略。共发表学术论文340余篇,论文总引用超过55,000次,SCI H-index =125。以下按照四个部分对刘庄团队2020年期间发表的部分成果进行归纳,供大家学习和交流。1. Nature Nanotech:个体化纳米疫苗获得新进展!

目前,作为癌症治疗主要技术之一的手术切除,面对的主要的问题是癌转移和复发。有报道称,术后进行免疫治疗,如免疫检查点阻断(ICB)治疗,可以降低癌症复发和转移的风险。然而,其治疗效果仍有待提高。为了制造有效的癌症纳米疫苗,至关重要的是开发既能充当免疫佐剂,还能够将抗原直接穿梭到APC细胞质中的抗原载体。
鉴于此,苏州大学刘庄教授、彭睿教授和华东师范大学程义云教授等人利用氟化树枝状大分子和聚乙烯亚胺(PEI)作为递送抗原的载体,来制备具有有效抗原交叉呈递的肿瘤纳米疫苗,并期望实现有效的针对患者的手术后免疫疗法。
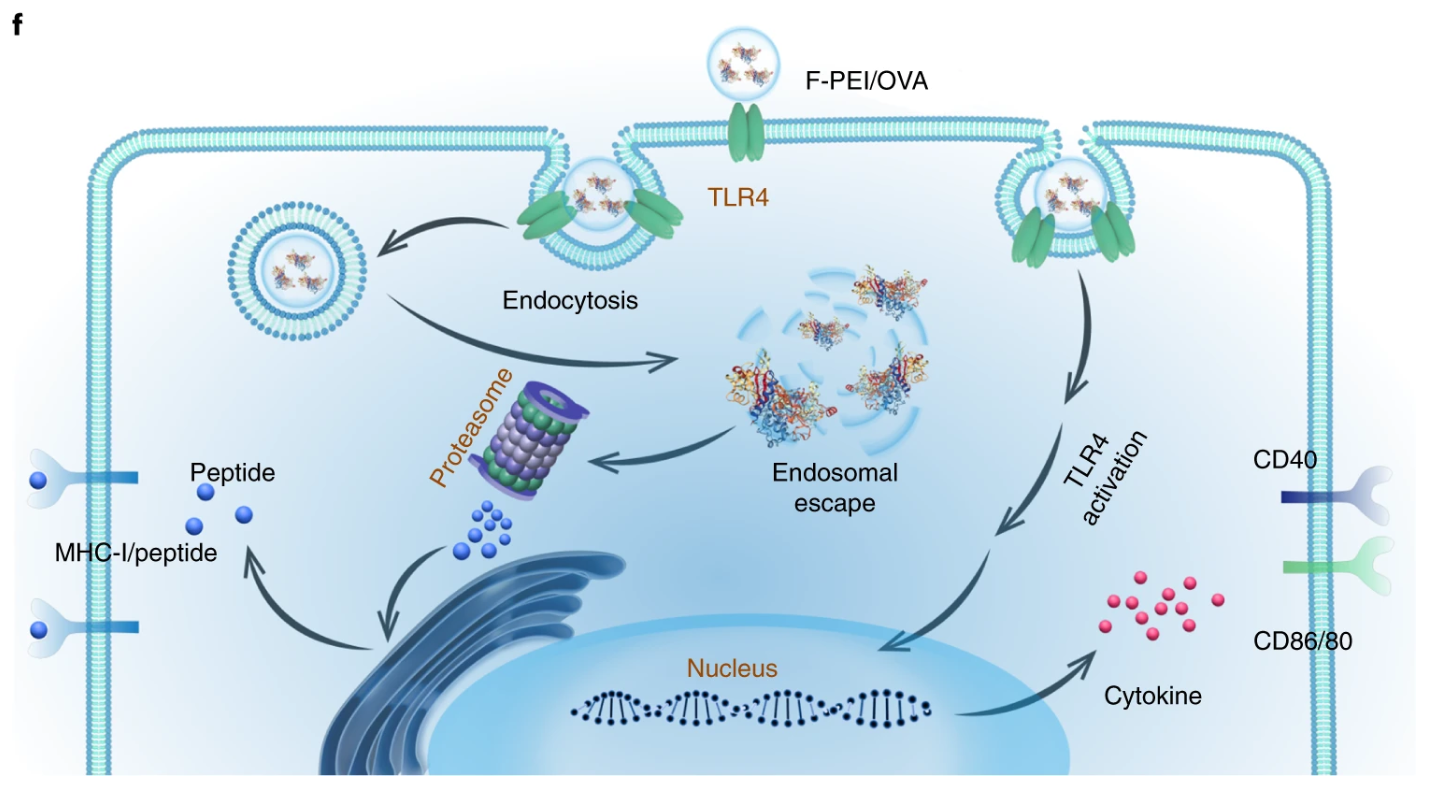
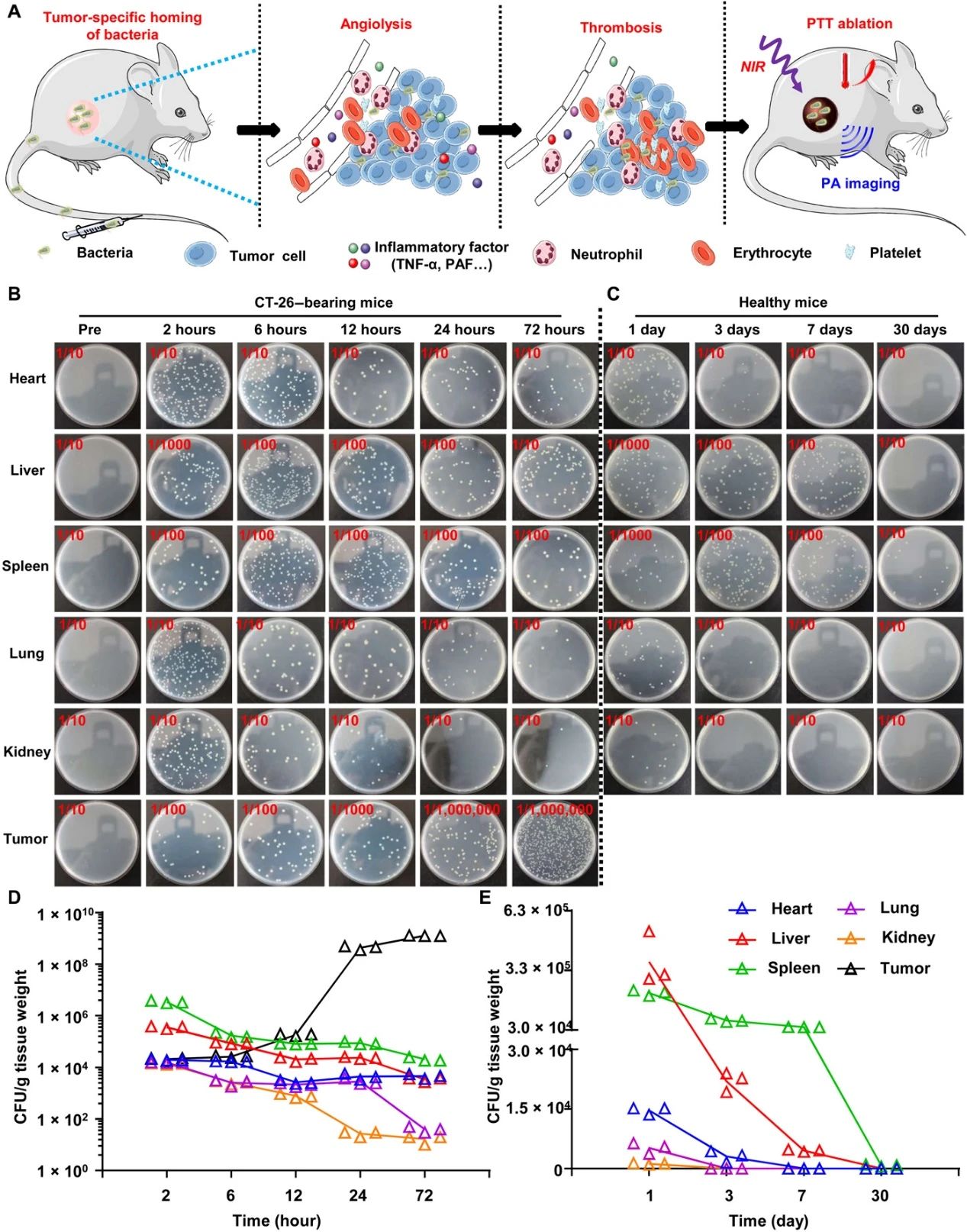
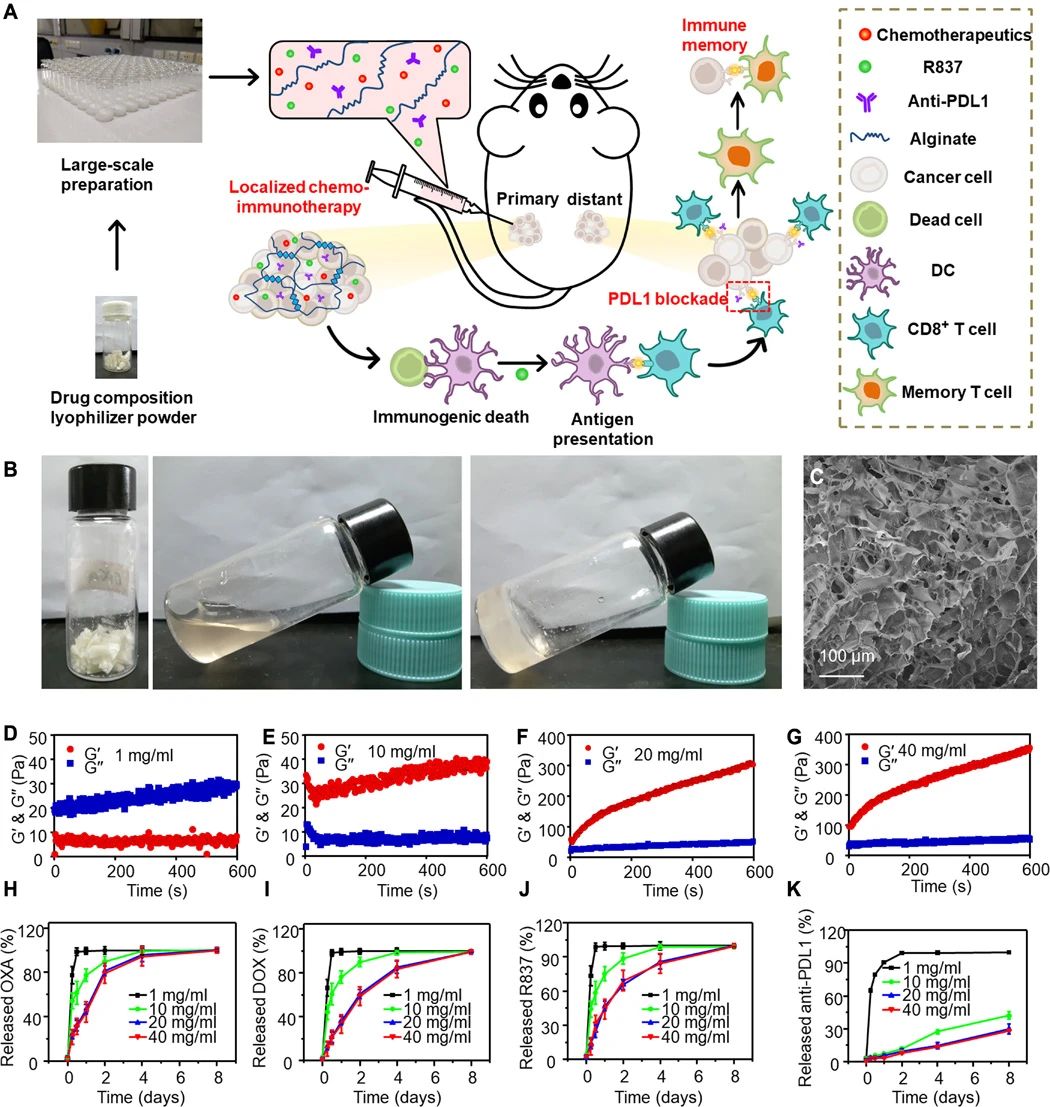
Xu, J., et al. A general strategy towards personalized nanovaccines based on fluoropolymers for post-surgical cancer immunotherapy. Nat. Nanotechnol. (2020).https://doi.org/10.1038/s41565-020-00781-42.Science Advances: 细菌触发的肿瘤特异性血栓形成可实现有效的癌症光热免疫治疗为了克服癌症的威胁,临床上已经应用或测试了基于不同机制的多种治疗策略。但是,常规的癌症疗法,例如化学疗法和放射疗法,在严重的副作用,治疗抗性和特异性有限方面存在局限性。包括光热疗法(PTT)和光动力疗法在内的光触发光疗法具有较低的侵入性和更高的特异性,但通常用于治疗局部肿瘤而不是远处转移的肿瘤。另外,已知单独的ICB治疗(不是肿瘤特异性治疗)的总体临床反应率相对较低。因此,近年来,ICB疗法与化学疗法,放射疗法,光疗等其他疗法的结合受到了广泛的关注。近日,苏州大学刘庄、杨凯等人发现,减毒沙门氏菌经静脉注射后可在各种类型的实体瘤中增殖,但在正常器官中表现出快速清除,而不会产生明显的毒性。1)细菌引起的炎症通过破坏肿瘤血管而引发肿瘤血栓形成。通过光声成像观察到,六种类型的肿瘤都会变成深色,具有强烈的近红外吸收。在激光照射下,细菌感染的肿瘤可以被有效地消融。2)基于细菌的光热疗法(PTT)由于具有免疫刺激功能,随后会引发抗肿瘤免疫反应,通过免疫检查点阻断进一步增强抗肿瘤免疫反应,从而有效抑制肿瘤的生长。基于细菌的PTT后,还观察到了强大的免疫记忆效应,可以抵抗再发的肿瘤。该研究表明细菌本身可以作为肿瘤特异性PTT试剂,使光免疫疗法能够抑制肿瘤的转移和复发。Xuan Yi, et al., Bacteria-triggered tumor-specific thrombosis to enable potent photothermal immunotherapy of cancer. Science Advances 2020.DOI: 10.1126/sciadv.aba35463. Science Advances:局部鸡尾酒化学免疫疗法以触发强大的全身性抗肿瘤免疫反应当前,迫切需要开发具有降低的全身毒性和有效功效以对抗具有扩散转移的晚期癌症的化学免疫疗法。于此,苏州大学刘庄等人报道了几种“鸡尾酒”治疗配方,即通过混合免疫原性细胞死亡(ICD)诱导的化学疗法和免疫佐剂以及藻酸盐(ALG)进行局部化学免疫治疗。1) 免疫检查点阻断(ICB)抗体可以包含在该鸡尾酒中以进行局部注射,也可以通过常规静脉注射使用。2) 将这种混合物注入实体瘤后,ALG的原位凝胶化将导致局部滞留和药物的持续释放,从而降低全身毒性。3) 化学疗法诱导的ICD在免疫佐剂的帮助下会触发肿瘤特异性免疫反应,ICB会进一步放大该免疫反应,从而在破坏局部肿瘤、消除转移并抑制癌症复发方面引发有效的全身性抗肿瘤免疫反应。研究人员结合临床上用于肿瘤局部化鸡尾酒化学免疫疗法的药物的策略具有巨大的临床转化潜力。
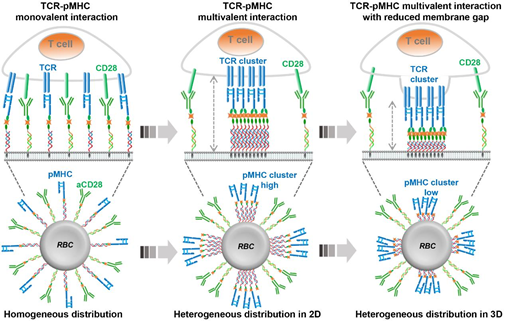
Chao Y, et al. Localized cocktail chemoimmunotherapy after in situ gelation to trigger robust systemic antitumor immune responses. Science Advances. 2020;6(10):eaaz4204.DOI: 10.1126/sciadv.aaz4204https://advances.sciencemag.org/content/6/10/eaaz42044. Angew:对红细胞上定位的配体进行DNA编辑以优化T细胞过继性免疫治疗表面锚定有T细胞活化配体的人工抗原呈递细胞(APCs)在过继性免疫治疗领域中具有巨大的应用潜力。然而,如何通过传统的生物偶联化学来精确控制这些平台上的配体定位仍然是一个很大的研究挑战。苏州大学刘庄教授利用DNA辅助的自底向上的自组装过错,实现了对T细胞激活配体在红细胞(RBC)上的横向和纵向分布的精确控制。1)研究发现,当RBC上的抗原肽-MHC分子复合物(pMHC)和细胞膜之间具有较短的垂直距离时更有利于实现有效的T细胞活化,这是由于它们可以更好地模拟了天然的APCs所导致的。2)这种优化的基于RBC的人工APCs可以通过过继性免疫治疗在体内刺激T细胞增殖,进而有效抑制肿瘤生长。因此,这一研究表明DNA技术可以精确地设计细胞膜界面和调整细胞与细胞之间的相互作用,有望在包括免疫治疗在内的更多领域实现广泛应用。
Lele Sun. et al. DNA-Edited Ligand Positioningon Red Blood Cells to Enable Optimized T Cell Activation for Adoptive Immunotherapy. Angewandte Chemie International Edition. 2020DOI: 10.1002/anie.2020033675.Nano Letters:注射用抗炎纳米纤维水凝胶实现局部给药后的全身免疫治疗尽管免疫检查点阻断(ICB)疗法在利用免疫系统对抗不同肿瘤方面已取得巨大进展,但诸如客观应答率低和不良反应等局限性仍有待解决。在此,苏州大学陈倩、刘庄等人开发了一种由类固醇药物自组装的抗炎纳米纤维水凝胶,用于局部递送抗程序性细胞死亡蛋白配体1(αPDL1)。1)这种基于类固醇药物的无载体系统一方面可以将促肿瘤免疫抑制的肿瘤微环境(TME)重新编程为抗肿瘤的TME;另一方面,它还可以作为αPDL1缓释的蓄水池,从而协同增强免疫系统。2)局部注射这种负载了αPDL1的水凝胶,在不经任何治疗的情况下,对局部肿瘤和异位肿瘤均有显著的抑制作用。综上所述,这项工作提出了一种独特的基于水凝胶给药系统,使用临床批准的药物,在提高ICB治疗的客观应答率和降低其全身毒性方面表现出潜力。
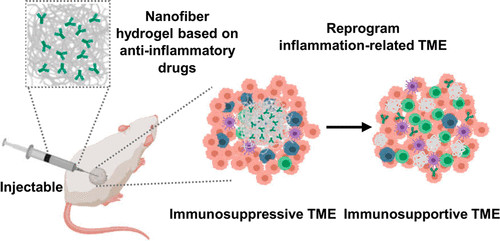
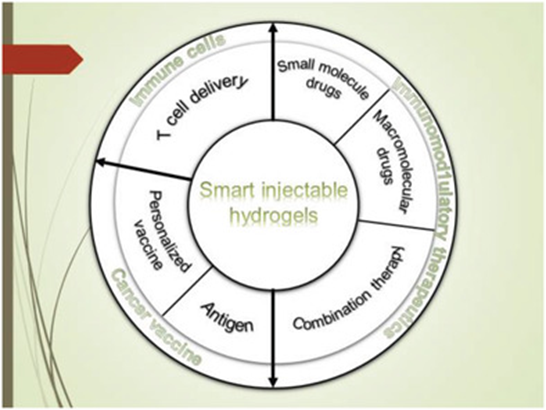
Muchao Chen, et al. Injectable Anti-inflammatory Nanofiber Hydrogel to Achieve Systemic Immunotherapy Post Local Administration. Nano Lett., 2020.DOI: 10.1021/acs.nanolett.0c02684https://doi.org/10.1021/acs.nanolett.0c02684最近,可注射智能水凝胶已证明其在局部免疫调节方面的潜力,以增强系统的抗癌免疫反应。刘庄教授总结了用于癌症免疫治疗的各种智能注射水凝胶的最新进展,并讨论了可注射水凝胶在下一代癌症治疗中的未来贡献。Yu Chao. et al. Smart Injectable Hydrogels for CancerImmunotherapy. Adv. Funct. Mater. 2020, 30, 201902785DOI: 10.1002/adfm.201902785https://doi.org/10.1002/adfm.2019027857.Nano Research:免疫可调节二维配位纳米片的声动力学疗法可增强抗肿瘤免疫疗法超声是目前临床上广泛使用的诊疗手段之一。肿瘤声动力治疗是通过使用超声刺激声敏剂催化肿瘤部位的氧气产生ROS,并同时产生空化气泡,共同作用引起肿瘤细胞凋亡,从而杀死肿瘤。据报道,与化疗,放疗,光学治疗类似,声动力治疗可以在引起肿瘤细胞凋亡的同时释放肿瘤相关抗原,刺激机体的免疫系统。另一方面,声动力治疗也可以刺激肿瘤免疫微环境,如逆转抗原呈递细胞如树突状细胞、巨噬细胞的被动特性,增强肿瘤活化T细胞的浸润通过自上而下的方法,苏州大学刘庄教授课题组将锌离子与声敏剂TCPP配位,合成了二维层状的金属有机纳米片,该纳米片可以高效吸附具有免疫佐剂作用的单链寡DNA,Toll样受体9的刺激剂CpG。基于该纳米片的声动力治疗可以诱导肿瘤细胞免疫原性死亡,产生肿瘤相关抗原,激活肿瘤部位T细胞活化与浸润,并产生相关活化的T细胞与记忆细胞,进一步杀死转移的肿瘤细胞。
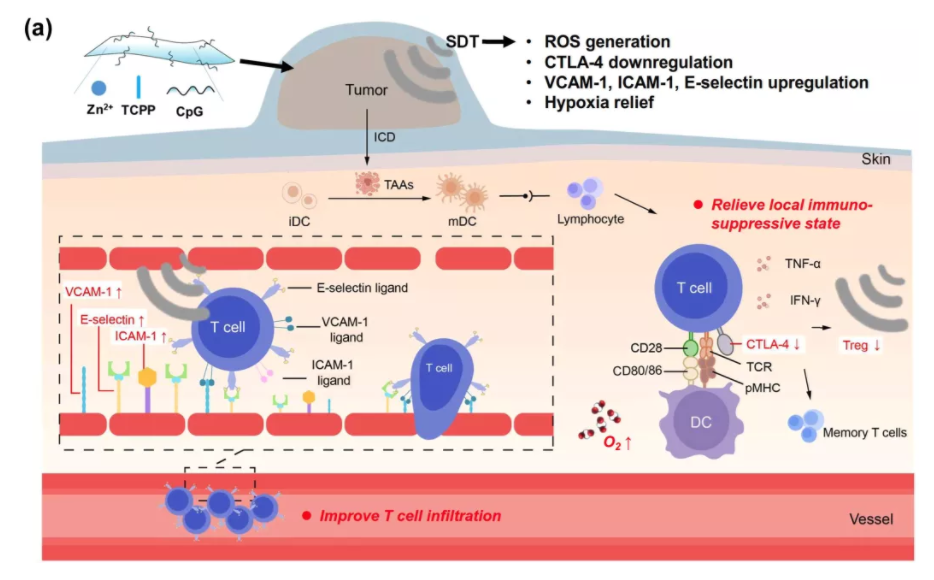
Wenjun Zhu et al. Sonodynamic therapy with immune modulatable two-dimensional coordination nanosheets for enhanced anti-tumor immunotherapy. Nano Research 2020.https://link.springer.com/article/10.1007/s12274-020-3070-88. JACS:超微一氧化钛纳米棒提高声动力治疗效果超声(US)触发的声动力学疗法(SDT)能够对较大的体内肿瘤进行无创治疗,引起了广泛的关注。为了改善对SDT的治疗反应,需要更有效和稳定的声敏剂。
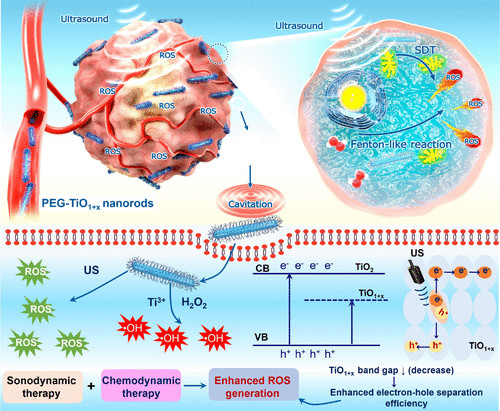
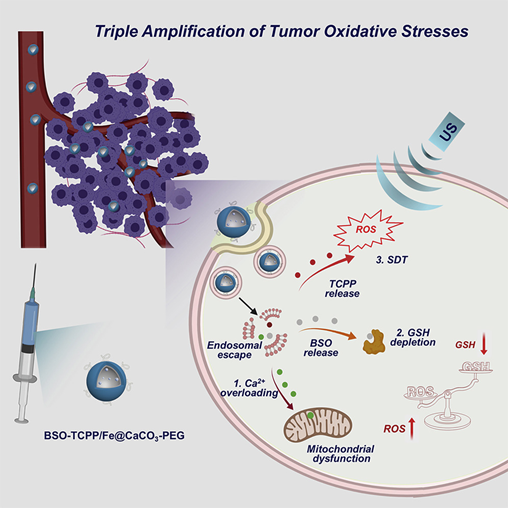
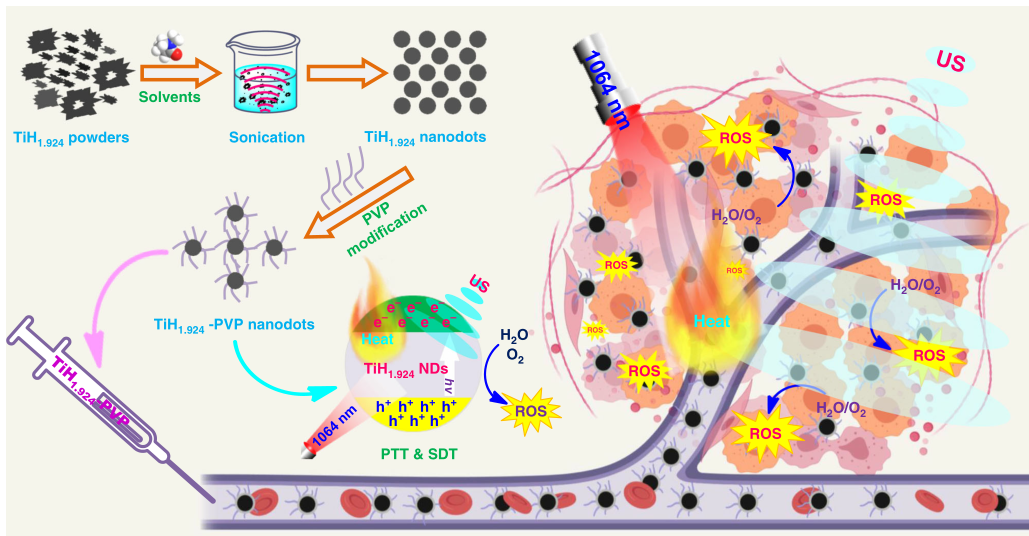
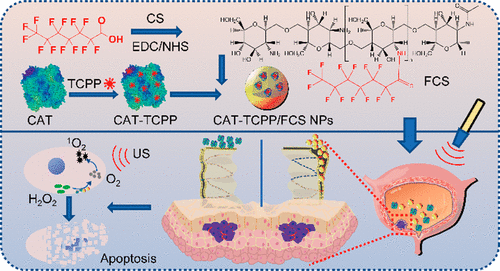
近日,苏州大学程亮教授和刘庄教授课题组制备了具有极大改善声敏性和类Fenton催化活性的超微一氧化钛纳米棒(TiO 1 + xNR),并应用于提高声动力疗法的治疗效果。1) 研究人员成功制备了具有超微棒状结构的TiO 1 + x 纳米粒,并用聚乙二醇(PEG)进行修饰。与传统的TiO 2纳米粒声敏剂相比,这种PEG-TiO 1 + x 纳米棒具有缺氧结构,从而更加有效地产生超声诱导的活性氧(ROS),因此它可以作为电荷陷阱,限制了超声触发的电子-空穴对的重组。2)这种PEG-TiO 1 + x 纳米棒还表现出类似辣根过氧化物酶的纳米酶活性,并且可以从肿瘤的内源H 2 O 2中产生羟基自由基(•OH),从而实现化学动力治疗(CDT)。3)这种PEG-TiO 1 + x 纳米棒在静脉注射后能有效地被动保留在肿瘤中,因此在超声治疗中可以用作声敏剂和化学动力治疗剂,可以高效消除肿瘤。小鼠模型实验结果显示,在治疗小鼠体内没有发现明显的长期毒性。综上,这项研究工作成功制备了一种新型的基于钛的纳米结构,具有良好的肿瘤声动力治疗效果。Xianwen Wang et al. Ultrafine Titanium Monoxide (TiO1+x) Nanorods for Enhanced Sonodynamic Therapy. J. Am. Chem. Soc. 2020.https://doi.org/10.1021/jacs.9b10228多功能刺激响应性纳米医学的发展吸引了有效的癌症治疗。于此,苏州大学刘庄和冯良珠等人利用生物相容性CaCO3纳米颗粒作为模板来指导pH分解的空心配位纳米结构的形成,其中声敏剂内消旋-四-(4-羧基苯基)卟啉(TCPP)作为有机桥连分子和三价铁离子充当金属中心。1)L-丁硫氨酸亚砜亚胺(BSO)是谷胱甘肽(GSH)生物合成的抑制剂,可以在制备TCPP-Fe@CaCO3期间同时加载,获得具有pH响应性解离的BSO-TCPP-Fe@CaCO3,以赋予Ca2+和BSO在酸性肿瘤微环境下快速释放2)这种BSO-TCPP-Fe@CaCO3通过细胞内Ca2+过载诱导的线粒体损伤,BSO介导的GSH消耗和TCPP介导的声动力疗法(SDT)赋予协同氧化应激扩增作用,导致显著的细胞死亡。用BSO-TCPP-Fe@CaCO3处理以及随后的超声暴露后的小鼠的肿瘤得以有效抑制。因此,该工作突出了一种简便的策略来制备可pH分离的纳米药物,可通过三重放大肿瘤氧化应激以有效地进行SDT治疗肿瘤。Dong Z, Feng L, Hao Y, Li Q, Chen M,Yang Z, et al. Synthesis ofCaCO3-Based Nanomedicine for Enhanced SonodynamicTherapy via Amplification ofTumor Oxidative Stress. Chem. 2020.https://doi.org/10.1016/j.chempr.2020.02.02010.Nature Commun.:液相剥离法制备TiH1.924纳米点用于增强声动力治疗金属氢化物在生物医学中的应用很少。在此,苏州大学刘庄、程亮等人通过液相剥离的方法从粉末状的氢化钛(TiH1.924)中制备出氢化钛纳米点,并将这些金属氢化物纳米点应用于有效的癌症治疗。1)液相剥离法是合成这些金属氢化物纳米材料的有效方法,其效率取决于溶剂与金属氢化物表面能的匹配程度。2)得到的TiH1.924纳米点在超声作用下能产生活性氧(ROS),表现出高效的声敏化效应。同时,TiH1.924纳米点具有很强的近红外(NIR)吸收,可以作为一种强大的光热剂。利用温和的光热效应增强肿瘤内的血流和改善肿瘤的氧合,在光热-声动力学联合治疗中取得了显著的协同治疗效果。3)重要的是,这些TiH1.924纳米点中的大部分都可以从体内清除。这项工作展示了功能性金属氢化物纳米材料在生物医学中的应用前景。Fei Gong, et al. Preparation of TiH1.924 nanodots by liquid-phase exfoliation for enhanced sonodynamic cancer therapy, Nat. Commun.,2020.DOI: 10.1038/s41467-020-17485-xhttps://doi.org/10.1038/s41467-020-17485-x11. ACS Nano:氟化壳聚糖促进超声敏化剂结合过氧化氢酶跨粘膜递送以实现声动力治疗膀胱癌声动力疗法(SDT)是一种非侵入性的超声触发治疗策略,用于深度穿透性肿瘤的定位治疗。目前,用于膀胱灌注后SDT治疗膀胱癌(BCa)的纳米声敏剂的设计尚未见报道。在此,苏州大学刘庄、深圳大学吴松等人开发了一种跨粘膜自产氧SDT纳米平台,以实现高效的SDT抗BCa。1)在该系统中,合成了氟化壳聚糖作为一种高效、无毒的跨粘膜递送载体,然后与中-四(4-羧基苯基)卟吩结合的过氧化氢酶(CAT-TCPP)组装。2)经膀胱灌注后形成的CAT-TCPP/FCS纳米粒子具有良好的跨粘膜和瘤内穿透能力,可通过过氧化氢酶催化肿瘤内源性H2O2产生O2,有效地缓解肿瘤组织中的缺氧,从而进一步提高SDT在超声作用下消融原位膀胱肿瘤的疗效。该工作提出了一种含有FCS的纳米超声增敏剂配方,以增强跨粘膜传递和瘤内扩散,并以CAT改善肿瘤的氧合,有望以滴注为基础的SDT治疗膀胱肿瘤,而不考虑全身毒性。Guangzhi Li, et al. Fluorinated Chitosan ToEnhance Transmucosal Delivery of Sonosensitizer-Conjugated Catalase for SonodynamicBladder Cancer Treatment Post-intravesical Instillation, ACS Nano, 2020.https://doi.org/10.1021/acsnano.9b0668912.ACS Nano:超小型Fe-TiO2 NDs增强癌症声动力和化学动力治疗声动力疗法(SDT)是在超声(US)作用下,利用声敏剂产生的活性氧(ROS)来杀死肿瘤细胞,是一种组织穿透深度高的、非侵入性治疗手段。在此,苏州大学程亮、刘庄等人采用热分解法制备了超小的铁掺杂二氧化钛纳米点(Fe-TiO2 NDs),作为一种声敏剂来增强SDT。1)这一体系中的铁掺杂似乎不仅在增强超声触发纳米点产生ROS方面起着至关重要的作用,而且还能为纳米点提供Fenton催化功能,以从肿瘤内源性H2O2中产生ROS,用于化学动力治疗(CDT)。2)聚乙二醇(PEG)修饰后的Fe-TiO2-PEG NDs具有良好的生理稳定性和生物相容性。3)体内磁共振(MR)和荧光成像显示,Fe-TiO2 NDs在静脉注射后具有有效地肿瘤滞留能力,由于CDT和SDT的结合,Fe-TiO2 NDs在体内表现出比商业TiO2纳米粒子更好的治疗性能。此外,这些超小的Fe-TiO2 NDs大多能在一个月内有效排泄,对实验小鼠没有明显的长期毒性。综上所述,此工作提供了一种多功能声敏剂,通过简单地将金属离子掺杂到二氧化钛纳米结构中,可以高效地治疗癌症。
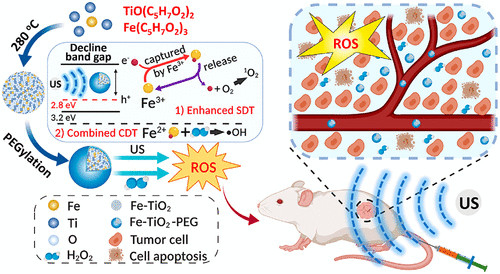
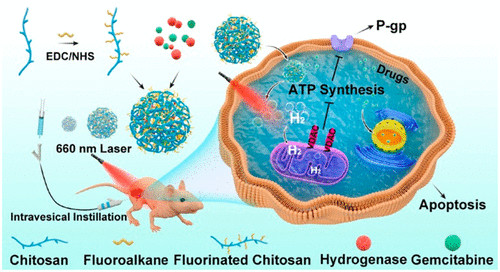
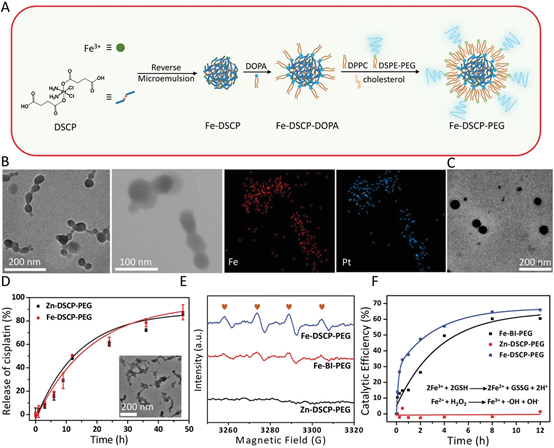
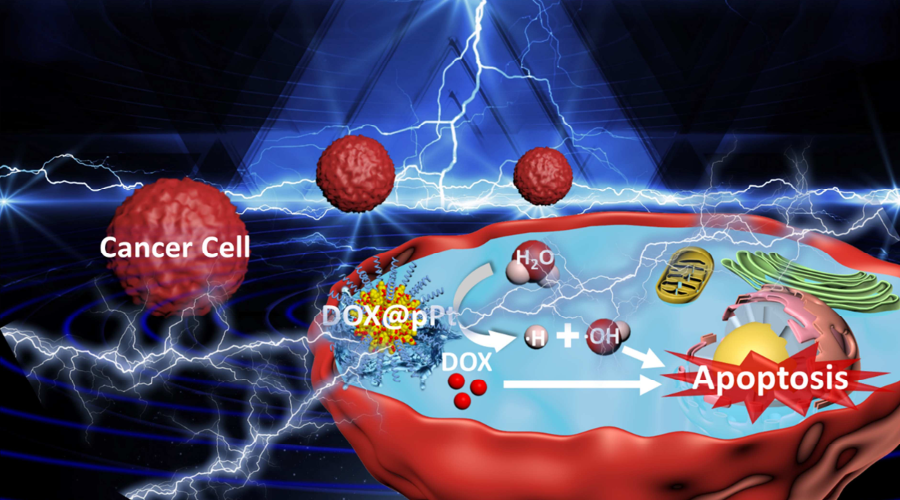
Shang Bai, et al. Ultrasmall Iron-Doped Titanium Oxide Nanodots for Enhanced Sonodynamic and Chemodynamic Cancer Therapy. ACS Nano, 2020.DOI: 10.1021/acsnano.0c05235https://doi.org/10.1021/acsnano.0c0523513. ACS Nano:光激活H2纳米发生器在膀胱癌化疗中的应用氢气可以减轻许多疾病中的氧化应激,被认为是安全的,没有副作用。受到多种微生物中的金属酶的启发,深圳大学吴松、苏州大学刘庄等人提出了一种光激活的H2纳米发生器,它包括氟化壳聚糖(FCS)、化疗药物(吉西他滨,GEM)和H2产生催化剂([FeFe]TPP),可以形成自组装的[FeFe]TPP/GEM/FCS纳米颗粒(NPs)。1)经膀胱灌注后,[FeFe]TPP/GEM/FCS NPs表现出良好的穿透粘膜和肿瘤细胞的能力,并能在660 nm激光照射下原位高效产生H2气体,显著提高了体内外肿瘤氢化疗的疗效。2)此外,还发现氢化疗中的H2气体可以抑制线粒体功能,阻碍ATP合成,导致P-gp外排泵功能降低,最终使癌细胞中P-gp蛋白的药物转运能力减弱。这种通过光激活原位产氢技术提高膀胱癌化疗的疗效,可能为肿瘤治疗提供一种有效的氢化疗策略。Rui Sun, et al. Photoactivated H2 Nanogenerator for Enhanced Chemotherapy of Bladder Cancer, ACS Nano, 2020.DOI: 10.1021/acsnano.0c01300https://doi.org/10.1021/acsnano.0c0130014. AFM:可生物降解的纳米级配位聚合物用于靶向性肿瘤联合治疗和氧化应激放大如今,已设计出多种基于金属离子的类Fenton催化活性而产生高反应性羟基自由基(·OH)的无机纳米颗粒,用于化学动力学治疗。然而,癌细胞中高水平的适应性抗氧化剂[谷胱甘肽(GSH)]可以有效地消耗·OH,从而降低这些无机纳米颗粒的治疗效率和生物安全性,这是化学动力学治疗中普遍关注的问题。于此,新加坡国立大学刘斌教授联合苏州大学刘庄教授等人通过逆微乳液法整合顺铂前药(DSCP)和铁(III)离子,开发了一种新的可生物降解的纳米级配位聚合物(NCP)。1)NCP中的DSCP可与GSH反应释放游离顺铂,而铁(III)离子可被GSH还原为铁(II)以使Fenton反应,随后导致细胞内氧化应激扩增。2)经过聚乙二醇(PEG)和环[Arg-Gly-Asp-D-Phe-Lys(mpa)]肽(cRGD)的表面修饰后,Fe-DSCP-PEG-cRGD对过表达αvβ3整合素的肿瘤表现出出色的靶向作用细胞。3)此外,与相对单一疗法相比,Fe-DSCP-PEG-cRGD可以实现显着的化学和化学动力学治疗,并显着提高治疗效率。重要的是,Fe-DSCP-PEG-cRGD可以在注射后7天通过粪便和尿液有效清除。在这项工作中提出的NCP简单且经济,显示出巨大的生物降解性和生物安全性,可用于潜在的临床转化。Liu, J., et al., BiodegradableNanoscale Coordination Polymers for Targeted Tumor Combination Therapy with Oxidative Stress Amplification. Adv. Funct. Mater. 2020, 30, 1908865.DOI: 10.1002/adfm.201908865https://doi.org/10.1002/adfm.20190886515. Biomaterials:负载阿霉素的多孔铂纳米颗粒用于化学-电动力学协同治疗p糖蛋白(P-gp)会将化疗药物泵出肿瘤细胞,其过表达也被认为是肿瘤细胞对常规化疗产生耐药的重要原因。浙江大学李翔副教授和苏州大学刘庄教授开发了一种多孔铂纳米颗粒(pPt NPs),并将其用于化学-电动力学协同治疗。1)实验利用聚乙二醇(PEG)对pPt NPs进行包覆,并利用其多孔结构负载了抗癌药物阿霉素(DOX)。pPt-PEG NPs可在电场作用下通过触发水分解以产生活性氧(ROS),并且这一过程不依赖于肿瘤中的O2和H2O2的水平。2)此外,EDT过程中产生的ROS可诱导p -糖蛋白(P-gp)受到抑制,从而促进药物在细胞内的积累,进而提高化疗药物的疗效。体内外实验结果表明,DOX@pPt-PEG NPs可通过化学-EDT联合治疗表现出良好的肿瘤治疗效果。因此,这一研究也为实现肿瘤的高雄联合治疗提供了一个新的策略。
Tong Chen. et al. Porous Pt Nanoparticles loaded with Doxorubicin to Enable Synergistic Chemo-/Electrodynamic Therapy. Biomaterials. 2020https://www.sciencedirect.com/science/article/pii/S014296122030448816. Adv. Mater.:用于癌症治疗的2D纳米材料苏州大学刘庄和程亮等人综述了二维纳米结构的独特特性(石墨烯片以及具有可调电子和光学特性以及可改变的表面化学性质的一系列结晶异质结构)。Cheng,L., et al., 2D Nanomaterials for Cancer Theranostic Applications. Adv. Mater.2020, 32, 1902333.https://doi.org/10.1002/adma.20190233317.Small:光敏剂修饰的二氧化锰纳米颗粒用于治疗脓肿可增强光动力治疗和免疫保护作用耐药菌的出现和易复发一直是细菌(如金黄色葡萄球菌)感染性皮肤脓肿临床治疗中的难题。在此,苏州大学刘庄、彭睿等人设计了一种能够调节脓肿微环境的抗菌纳米制剂,以增强皮肤脓肿的光动力,并随后激活免疫系统,有效地防止脓肿复发。1)在该体系中,利用光敏剂Ce6对二氧化锰纳米颗粒(MnO2 NPs,对H2O2具有高催化活性。)进行改性,并用聚乙二醇(PEG)对其进行包覆。2)所获得的Ce6@MnO2-PEG NPs通过触发病灶内源性H2O2的分解,能够有效缓解金黄色葡萄球菌感染过程中的缺氧脓肿微环境。因此,光触发的光动力杀菌效果可以显著增强,从而对金黄色葡萄球菌引起的皮肤脓肿进行有效的体内治疗。3)有趣的是,经过这种治疗后,由于光动力疗法(PDT)后细菌抗原的释放以及锰离子激活宿主免疫系统的佐剂样功能,诱导了显著的病原体特异性免疫记忆效应,以对抗未来由同一种类的细菌感染。这项工作提出了一种新型的光动力纳米制剂,特别是在高效的光触发脓肿治疗和预防脓肿复发方面前景看好。Chenya Wang, et al. Photosensitizer‐Modified MnO2 Nanoparticles to Enhance Photodynamic Treatment of Abscesses and Boost Immune Protection for Treated Mice, Small, 2020.DOI: 10.1002/smll.20200058918. Biomaterials:一种可清除ROS的水凝胶促进细菌感染糖尿病伤口的愈合细菌感染对皮肤创面,尤其是难以愈合的糖尿病创面构成了极大的威胁。众所周知,伤口或细菌感染产生的活性氧(ROS)会进一步阻碍伤口愈合。在此,苏州大学刘庄、苏州大学儿科医学研究所汪健等人利用活性氧响应性连接物交联聚乙烯醇(PVA),研制了一种清除活性氧的水凝胶。1)所得水凝胶可作为一种有效的ROS清除剂,通过降低创面周围ROS水平,上调M2表型巨噬细胞,促进创面闭合。2)重要的是,在伤口中形成的这种水凝胶可以释放治疗药物,包括杀菌的莫匹罗星和加速伤口闭合的粒细胞-巨噬细胞集落刺激因子(GM-CSF),以响应伤口微环境中存在的内源性ROS。值得注意的是,该载药活性氧清除水凝胶可以有效地治疗各种类型的伤口,包括难以愈合的糖尿病合并细菌感染的伤口。因此,本研究提出了一种基于活性氧清除水凝胶的各种并发症下创面愈合的有效策略。He Zhao, et al. ROS-scavenging hydrogel to promote healing of bacteria infected diabetic wounds. Biomaterials, 2020.https://doi.org/10.1016/j.biomaterials.2020.120286此外,刘庄团队2020年还发表了其他相关的高水平研究论文,由于篇幅关系就不在此一一展示,感兴趣的读者可前往该课题组网站进行学习。课题组网站:http://nano.suda.edu.cn/lz/刘庄,苏州大学纳米科学技术学院教授,博士生导师。国家杰青。2004年北京大学化学与分子工程学院获理学学士学位;2008年美国斯坦福大学(Stanford University)获得化学博士学位;2008年至2009年在斯坦福大学化学系以及医学院从事博士后研究。2009年6月加入苏州大学功能纳米与软物质研究院,被聘为教授,博士生导师。近年来在生物材料与肿瘤纳米技术领域从事研究,围绕肿瘤诊疗中的若干挑战性问题,发展了一系列新型纳米探针用于体外生物检测与活体分子影像,并探索了多种基于纳米技术和生物材料的肿瘤光学治疗、放射治疗、与免疫治疗新策略。共发表学术论文340余篇,论文总引用超过55,000次,SCI H-index = 125。2014年起连续入围Elsevier出版社发布的“中国高被引用学者榜单”(材料科学类);2015年起连续入选美国美国科睿唯安(原汤森路透集团)公布的“全球高被引科学家名单”(Highly Cited Researchers)(化学、材料)。担任Biomaterials副主编。