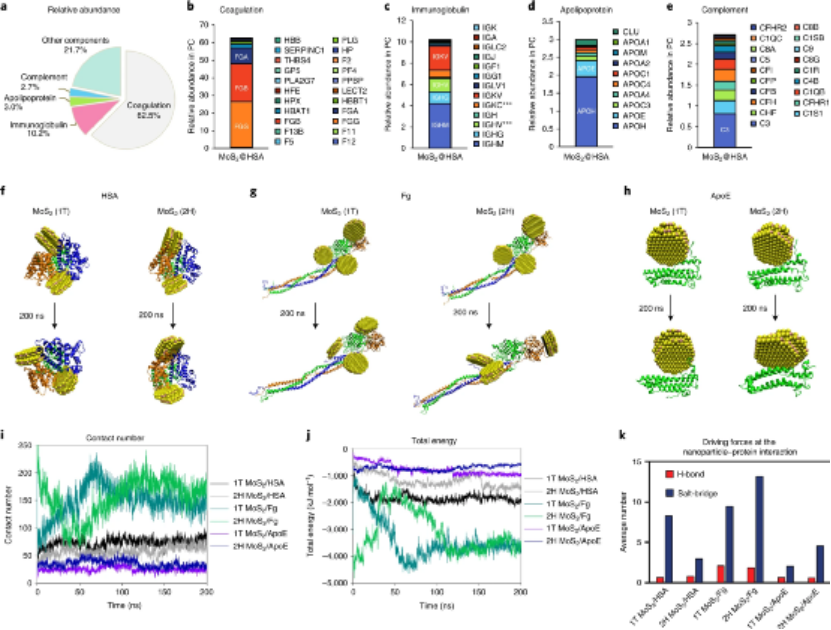
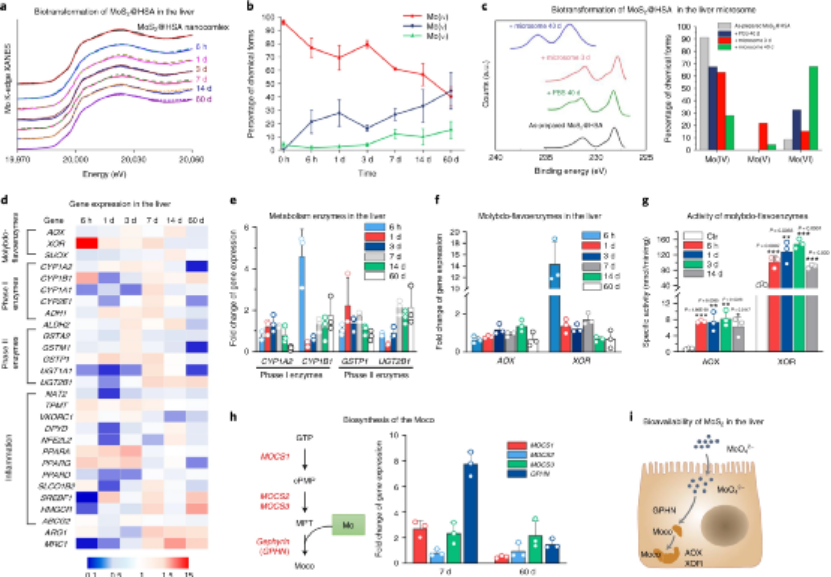
具有多种表面化学性质的过渡金属硫化物纳米材料已经成为有前途的纳米平台,可用于药物输送、癌症治疗、生物成像和生物传感。过渡金属硫化物的不同化学性质使其对环境因素敏感;例如,氧气的存在会导致其氧化。微量元素钼对几乎所有生物都是必不可少的。因此,从MoS2纳米材料中降解的钼可能诱导独特的生物学过程和体内命运,涉及生物分布、生物转化和生物利用度。生物医学纳米材料的行为所基于的几个基本原理仍然不清楚,包括纳米颗粒如何与生物屏障相互作用以及长期的生物效应。从给药到清除的体内运输过程仍然是一个“黑匣子”。血液中形成的蛋白质电晕是纳米材料与生物相互作用的第一个明确指示。但是,需要全面了解纳米颗粒与器官和组织的基本相互作用。为了阐明血液中纳米粒子与蛋白质相互作用的作用,国家纳米科学中心陈春英研究员等人开发了分别缺乏载脂蛋白E(ApoE),纤维蛋白原(Fg),补体3(C3)和免疫球蛋白M(IgM)的转基因小鼠,从复杂的蛋白质晕中剥离这些重要蛋白质,并揭示其主要驱动力,然后通过体内实验和分子动力学模拟的结合描述了MoS2纳米材料的在体内的运输,转化和生物利用。成果发表在Nature Nanotechnology上。

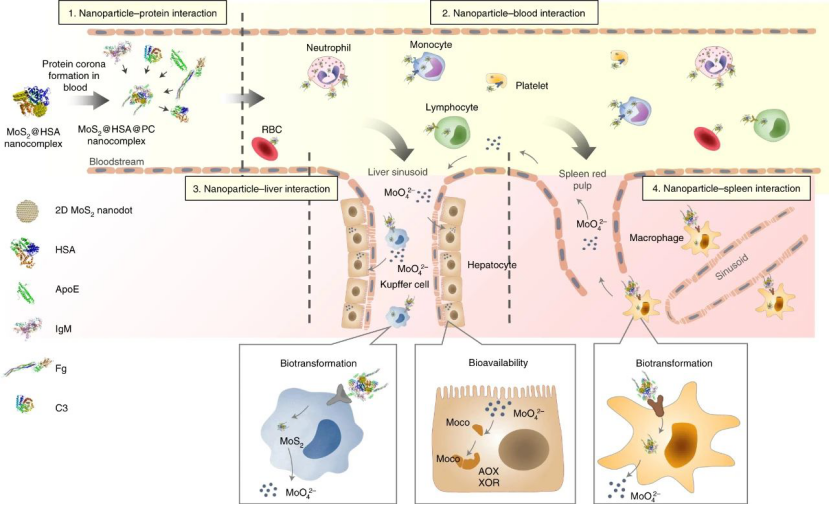
整体架构如下,纳米粒子-蛋白质界面(蛋白质晕)发生的相互作用在决定体内转运过程中起着至关重要的作用。位于肝窦和脾红髓中的大多数隔离的MoS2纳米材料经历氧化,随后降解为钼酸盐,可用于肝脏中Moco生物合成,以增强钼酶的特定活性。也就是说,纳米粒子与生物系统之间的基本相互作用是通过蛋白质电晕桥联的运输-转化-生物利用链实现的。
通过静脉内注射施用纳米材料后,它们遇到的第一个生物屏障是生物分子(主要是蛋白质)和血液中的细胞。结果表明,MoS2 @ HSA纳米复合物的分布和清除半衰期分别为3.5和56.7 min。定量测定不同血液成分中的钼含量:注射后5分钟,血浆中总钼的含量为69.6%±11.5%。其余的被血细胞吸收了。注射后30分钟,血浆中钼的百分比下降到3.9%±1.0%。其中,PBMC和中性粒细胞内化量最高。随后研究了在MoS2@HSA纳米复合物上形成的蛋白质晕的组成。由于蛋白质晕具有很高的动态性,因此原始的HSA中约32%的蛋白质被血液中的蛋白质交换。蛋白质电晕中蛋白质的相对丰度按以下顺序排列:凝结蛋白>免疫球蛋白>载脂蛋白>补体。
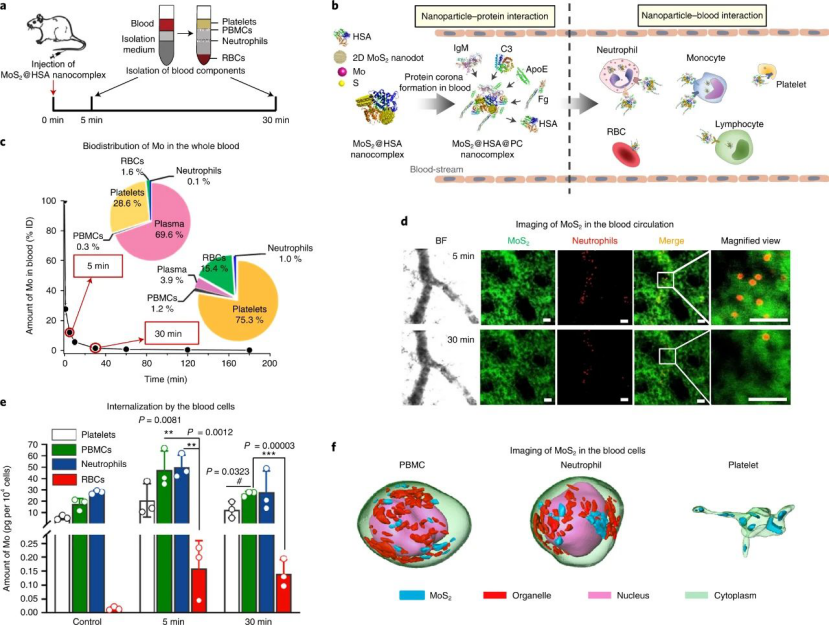
图|MoS2 @ HSA纳米复合物与血液蛋白和免疫细胞快速相互作用
为了确定纳米粒子与蛋白质界面相互作用的机理,研究人员进行了分子动力学模拟,以分析MoS2纳米点与Fg、HSA和ApoE之间的相互作用。结果表明,与HSA和ApoE相互作用相比,MoS2纳米点与Fg之间的相互作用更为优先。不出所料,MoS2-Fg相互作用具有最低的能量,反映出更稳定的吸附。为了研究MoS2@HSA纳米复合物的运输过程,研究人员量化了钼在几个阶段的生物分布。结果表明,即使在60 天后,MoS2@HSA纳米复合物仍被螯合在单核吞噬细胞系统(主要是肝脏和脾脏)中。静脉注射后,MoS2@HSA纳米复合物在脱氧的血液中在最初的30分钟内从心脏转移到肺部,初始摄取量很高。由于肺毛细血管系统,纳米颗粒直接通过血液循环迅速离开肺。它们被MPS吞噬,该过程支持纳米颗粒在更长的时间内转运到其他器官,例如肝脏和脾脏。
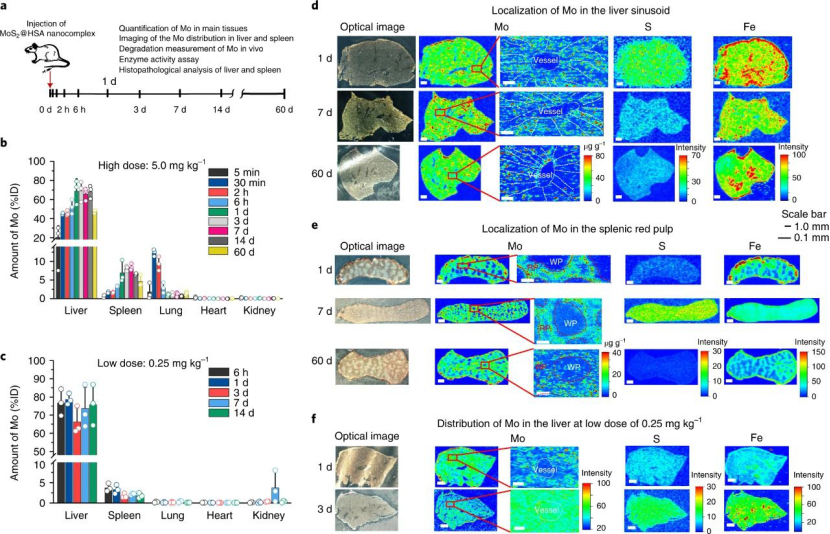
大量研究表明,免疫球蛋白,载脂蛋白和补体成分是决定纳米颗粒转运的关键蛋白。但是,本文结果表明这三种蛋白质对MoS2 @HSA纳米复合物的生物分布没有影响。简而言之,血源性MoS2 @HSA纳米复合物位于肝窦和脾红髓的常驻巨噬细胞,它们受冠状动脉ApoE调节。
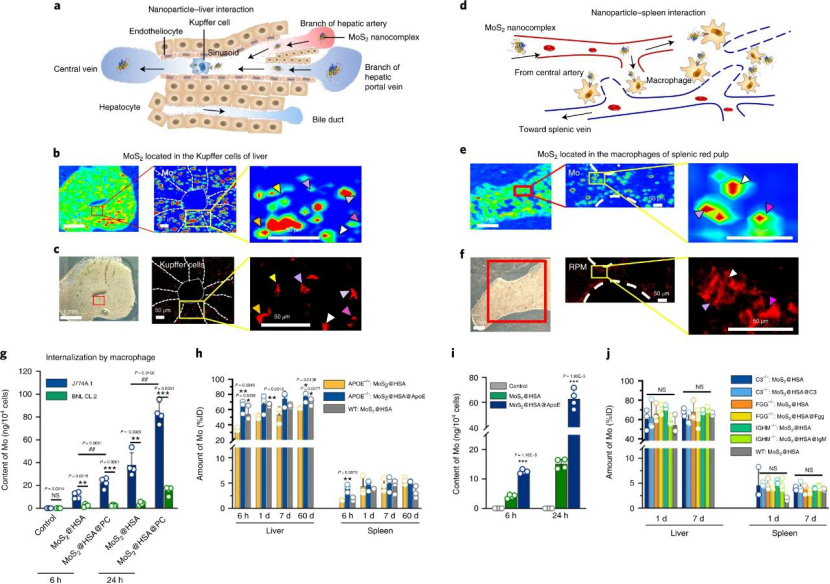
图|肝窦和脾红髓中的常驻巨噬细胞隔离MoS2 @HSA纳米复合物
接下来,研究人员研究了MoS2 @ HSA纳米复合物在肝脏中的生物转化过程。研究表明,MoS2在肝脏中被氧化,钼从Mo(IV)化学转化为Mo(VI)。在肝脏中,异源生物的生物转化是由I相和II相酶进行的,它们分别负责I相(即氧化,还原和水解反应)和II相(即共轭反应)的代谢。结果显示,肝微粒体将MoS2氧化为MoO42-,这暗示着I相酶(肝微粒体中的主要氧化酶)有助于MoS2的氧化。此外,在与MoS2@HSA纳米复合物孵育的巨噬细胞中检测到了活性氧,这可能有助于脾中MoS2的生物转化。此外,用HSA和小鼠血浆蛋白修饰的纳米点可保护MoS2免受氧化。钼是唯一的第二行过渡金属,是当以钼酸盐形式存在时可生物利用的必需微量元素。它被掺入到钼辅助因子中,这是许多酶催化重要化学转化的活性位点。醛氧化酶(AOX)和黄嘌呤氧化还原酶(XOR)是哺乳动物中的两种主要的黄酮类黄酮酶。同样,结果显示,由MoS2@HSA纳米复合物衍生的氧化钼在掺入钼辅因子(Mocos)后明显增强AOX和XOR的活性。XOR和AOX的比活增加表明,螯合在肝脏中的MoS2衍生的钼很容易被生物利用。图|MoS2作为肝脏中的钼辅助因子的生物转化和生物利用度总体而言,研究人员评估了体内MoS2纳米点的生物动力学和分布,以及MoS2纳米点与生物系统(纳米粒子-蛋白质、纳米粒子-血液、纳米粒子-肝脏和纳米粒子-脾脏)的基本相互作用。该课题组揭示了ApoE是负责组织之间MoS2 @ HSA纳米复合物的运输。经过对体内纳米材料的运输-转化-生物利用度链的全面研究,证明MoS2 @ HSA纳米复合物在肝窦和脾脏红髓中被截获,并且MoS2降解产生的氧化成分最终并入肝中的钼酶中,影响其新陈代谢。因此,本文提出了关于带有必需微量元素的纳米材料的独特体内命运。Cao, M., Cai, R., Zhao, L. et al. Molybdenum derived from nanomaterials incorporates into molybdenum enzymes and affects their activities in vivo. Nat. Nanotechnol. (2021).https://doi.org/10.1038/s41565-021-00856-w