特别说明:本文由米测技术中心原创撰写,旨在分享相关科研知识。因学识有限,难免有所疏漏和错误,请读者批判性阅读,也恳请大方之家批评指正。
研究背景
Haber–Bosch工艺被认为是20世纪最重要的科学发明,可以在Fe和Ru催化剂上将N2和H2大规模转化为NH3,被广泛用于肥料生产。
关键问题
然而,Haber-Bosch工艺的研究仍存在以下问题:目前研究认为Haber-Bosch工艺实现转化的催化剂活性组分可能是氧化物、氮化物、金属相或表面氮化物,限速步骤可能为N2解离、吸附态氮反应或NH3脱附,其反应机理仍不明确。Haber-Bosch过程在高温高压下运行,而可能区分不同机理方案的表面敏感技术需要真空条件,相应地,机理研究长期以来仅限于理论计算。
新思路
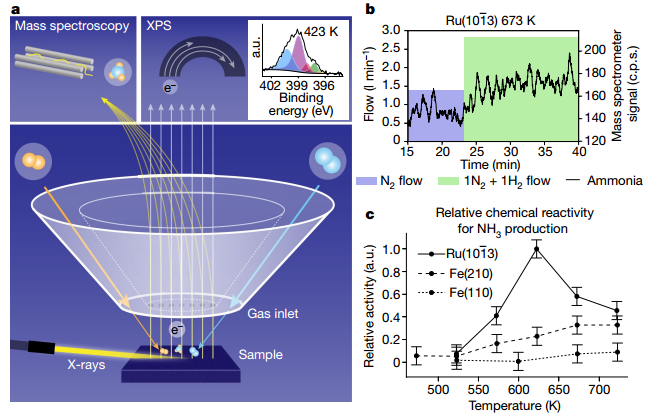
有鉴于此,瑞典斯德哥尔摩大学Anders Nilsson、Christopher M. Goodwin等人使用X射线光电子能谱(能够揭示催化表面的化学状态,并且最近适用于甲醇和费托合成的操作研究)来确定在压力高达1 bar和温度高达723 K的NH3生产过程中Fe和Ru催化剂的表面组成。作者发现,虽然扁平和阶梯状的Fe表面和Ru单晶表面都保持金属性,但后者几乎不含吸附物,而Fe催化剂保留少量吸附的N并在较低温度下在台阶表面形成了高胺(NHx)覆盖率。这些观察结果表明Ru的限速步骤始终是N2解离。相比之下,正如理论所预测的那样,在Fe催化剂上,吸附的N原子的氢化效率较低,以至于限速步骤随着温度降低从N2离解切换到表面物种的氢化。 作者展示了Haber-Bosch过程中测量表面敏感原位XPS及反应产物检测,并通过质谱仪跟踪了NH3的产生,计算了相对周转频率。作者分别在纯N2和1:1 N2:H2条件下监测了Fe和Ru表面氮化物的形成,显示了催化剂表面N2和H2解离速率的差异。 作者通过原位监测表明金属Fe在573K后被完全还原,而Ru在所有条件下均以金属形式存在。作者观测了两种金属表面吸附氮物质随着温度、压力的变化趋势,提出了基于两种金属表面的反应机制,表明Ru表面的限速步骤始终是吸附的N2的解离,而Fe上限速步骤随温度的降低由解离转化为氢化。1、通过XPS实现了经典Haber-Bosch催化过程的直接观测作者通过差动泵方案实现了XPS的原位研究,确定了在压力高达1 bar和温度高达723 K的NH3生产过程中Fe和Ru催化剂的表面组成。作者通过原位监测催化反应过程中Fe表面和Ru单晶表面组成,表明Ru的限速步骤始终是N2解离,而Fe催化剂的限速步骤随着温度降低从N2离解切换到表面物种的氢化。作者展示了如何在POLARIS仪器中实现Haber-Bosch过程中测量表面敏感原位XPS及反应产物检测。Fe和Ru单晶表面安装在电子能谱仪前面,气体通过电子透镜的前锥体注入,形成一个具有快速气流的高压局部虚拟催化反应器。通过入射能量设置实现了高表面灵敏度。作者通过质谱仪跟踪了NH3的产生,计算了每个表面位点每秒形成的氨分子数,然后将其进一步归一化为任何表面在任何温度下显示的最高活性。结果表明,反应速率随着温度的升高而增加,并且阶梯状Fe(210)表面的反应速率高于平坦Fe(110) 表面,Ru(1013)表面的速率最高。
图 实验设置和相对周转频率测量
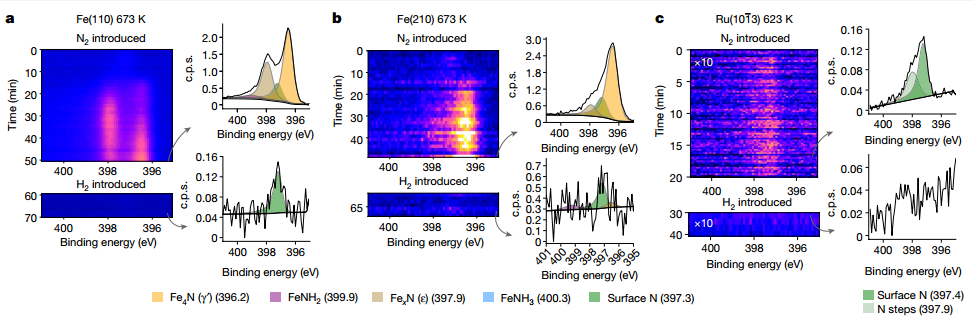
当暴露于150 mbar的纯N2中时,两个Fe表面的N1s强度出现延迟但最终快速增加,显示出块状氮化物的形成,Fe(210)表面上的氮化物形成速度更快,特别是γ'-氮化物,而在 Fe(110) 表面上,两种氮化物的数量相等且生长速度较慢。氮化物层的厚度大于十单层;精确的定量取决于反应时间。Ru(1013)的反应完全不同。在N2暴露后几乎立即达到N1s 强度饱和并保持恒定。Ru表面上的少量N2表明N-金属相互作用比Fe上弱得多。当在300 mbar下用1:1 N2:H2代替纯N2气体时,两个Fe表面在第一次光谱扫描(90s)内发生显着变化,氮化物的快速去除显示了H2的强大还原能力。Ru(1013)表面上吸附的N原子覆盖率也显着降低,并且随着NH3的产生。
图 氮化物的形成和耗尽
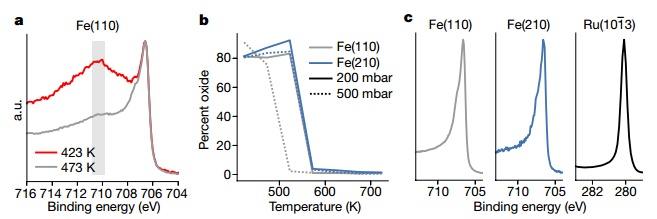
接下来,作者解决了由于气相中水或CO2的痕量污染,在原位操作条件下氧化物可能无法在Fe上还原的问题。已知铁在室温下会在微量的水或CO2中氧化,但氧化铁在500 K以下时不易被还原,因此,即使在纯氢气下,铁也会在高流量下氧化。作者展示了在500 mbar、1:3 N2:H2和各种温度下收集的数据,金属铁的Fe 2p2/3峰在706.5eV和707.4eV处由于与铁磁价电子的交换相互作用而分裂,并且在710.8-709.8eV处有一个宽的Fe氧化物峰。当温度在 500 毫巴下达到 523 K 时,Fe(110)样品完全还原,而Fe(210)表面需要573 K,这是由于Fe(210)阶梯表面上的氧结合力更强。而Ru在所有条件下都是金属。
图 氧化物和金属
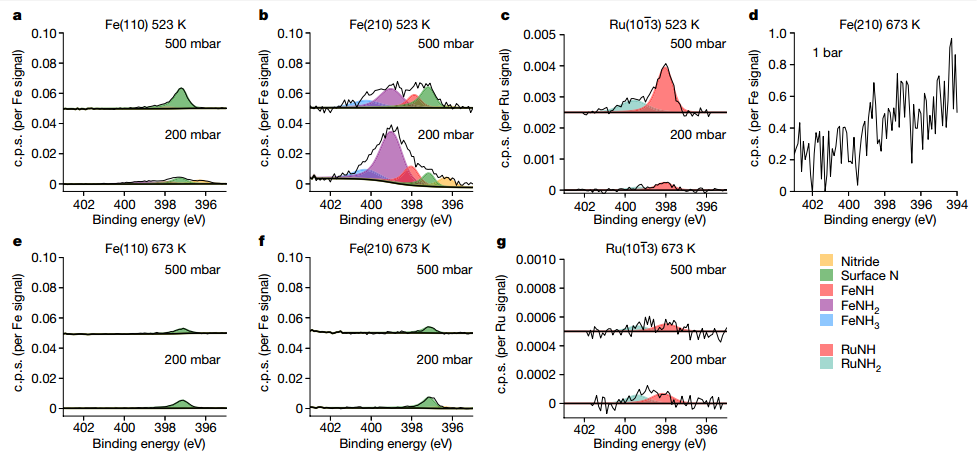
当NH3产生时,可以测量吸附的氮物质。作者首先关注了两个Fe单晶表面,发现随着压力的增加,覆盖率略有下降,表明表面的氢化能力随着总压力的增加而增加。在高温下,Ru表面在高反应速率条件下,几乎完全清除了任何物质,吸附的N物质对Ru的反应性比对Fe的反应性要高得多。作者证明了氮化物的形成比氮化物的还原慢得多,并且表面态都是金属态,原子氮的覆盖率较低。基于研究结果,作者提出了NH3合成中的不同反应步骤,在Ru表面NH3产生的限速步骤是吸附的N2的解离,在Fe上限速步骤随着温度的降低由解离转化为氢化。
尽管低压氨合成作为替代方案已被广泛研究,但Haber-Bosch工艺仍将是多年来氨生产的主要方法来。更好地了解其作用机制可能有助于进一步提高效率,从而降低这一重要工业过程对环境的影响。本工作提出的XPS原位监测方法将有助于进一步解析Haber-Bosch机制,使探索在促进剂存在下与氨形成相关的表面化学成为可能。 Goodwin, C.M., Lömker, P., Degerman, D. et al. Operando probing of the surface chemistry during the Haber–Bosch process. Nature 625, 282–286 (2024). https://doi.org/10.1038/s41586-023-06844-5