对复杂金属酶的深刻机理表征需要多种互补技术。有鉴于此,德国柏林工业大学的Ingo Zebger等研究人员,通过一种针对溶剂化、冻干化和晶体化金属酶的先进实验手段,研究了镍铁氢化酶氧化还原中间体的结构和功能。
本文要点
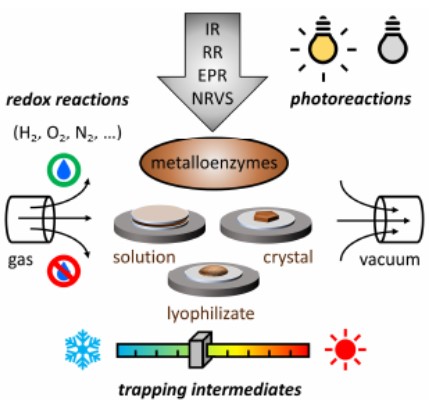
1)研究人员开发了一种新的实验装置,可以对催化中间体进行可控制备,以通过各种光谱学技术对其进行表征。
2)对于气体交换时酶的冻干粉、晶体或溶液,还可以在广泛的温度范围内通过红外光谱原位监测其氧化还原转变。
3)研究人员用两种耐氧气的镍铁氢化酶作为模型系统进行研究。首先,利用他们的平台制备了处于顺磁态且含有桥氢的高浓度氢化酶冻干粉。这一过程被证明有利于57Fe核共振振动光谱,结合密度泛函理论计算,该催化中间体的振动指纹得到了揭示。
4)结合共振拉曼光谱,同样的原位红外装置对酶晶体的氧化还原化学提供了详细的了解,这再一次说明了用光谱学分析补充X射线晶体学数据的普遍必要性。
参考文献:
Christian Lorent, et al. Exploring structure and function of redox intermediates of [NiFe]‐hydrogenases by an advanced experimental approach for solvated, lyophilized and crystallized metalloenzymes. Angewandte Chemie, 2021.
DOI:10.1002/anie.202100451
https://onlinelibrary.wiley.com/doi/10.1002/anie.202100451


















